Schéma de l`essai multicentrique de phase II évaluant
publicité

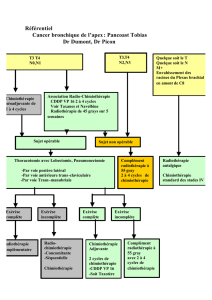
Schéma de l’essai multicentrique de phase II évaluant en néo-adjuvant l’association Docetaxel plus Cisplatine chez des sujets atteints d’un carcinome indifférencié de type nasopharynge Objectif primaire : Evaluer le taux de réponses objéctives clinique en RECIST obtenu après 3 cycles d’une stratégie thérapeutique néo-adjuvante de DOCETAXEL à la dose de 75mg/m² en association avec Cisplastine à la dose de 75mg/m², et après radiothérapie conventionnelle, dans le carcinome indifférencié de type nasopharyngé Objectifs secondaires : - Evaluation de la réponse radiologique après chimiothérapie et radiothérapie - Evaluer le temps jusqu’à progression - Evaluation de la réponse pathologique - analyse de survie globale Cycle 2 J-28 J-7 J1 J22 Cycle 3 J43 J36 J14 Evaluation post radiothérapie Evaluation post chimiothérapie J64 J71 J85 J106 J57 J127 J148 Radiothérapie Chimiothérapie Pré- inclusion Tous les 3 mois jusqu’au décès 3 à 6 semaines après la chimiothérapie 3 Cycles de 21 jours Cycle 1 - Evaluation de la durée de réponse - Analyse de la tolérance Follow-up Début de l’étude Fin de l’étude Critères d’inclusion - Consentement éclairé daté et signé. - Carcinome nasopharyngé OMS II-III histologiquement prouvé sur biopsie du cavum. - UNCT stade III, IVA, IVB selon classification UICC/AJC 1997 avec N2 ou N3 et adénopathies > 3cm et sans métastases à distance. - Age ≥ 20 et ≤ 75 ans. - Statut de performance ≤ 1 ou indice karnofsky ≥ 70%. - Espérance de vie > 3 mois. - Sujet jamais traité antérieurement pour ce cancer. - Fonctions hématologiques, hépatique et rénales normales, réalisées 7 jours avant l’inclusion. - Fonction cardiaque normale. Critères de non-inclusion Inclusions : 22 patients/centre J-28 Consentement éclairé Examen physique Examen du cavum Indice de performance Biopsie du cavum - Reçu précédemment pour son UCNT, une chimiothérapie et/ou radiothérapie et/ou chirurgie curatrice. - UCNT stade III, IVA, IVB, avec N0 et N1, N2, N3 ≤cm (classification UICC/AJC 1997). - Localisation métastasique à distance. - Carcinome nasopharyngé histologiquement prouvé (biopsie du cavum). - Diagnostic histologique fait sur biopsie ganglionnaire. - Antécédents d’une tumeur cancéreuse sauf carcinome in situ du col utérin ou cancer basocellulaire cutané ou autre cancer traité curativement durant les 5 dernières années. - Femmes enceintes ou allaitant et sujet en âge de procréer (mis sous contraception) - Antécédents de défaillance organique majeure - Traitement concomitant par corticoïdes ≥ 20mg de méthyle-prednisolone dans les 6 mois précédents l’étude - Autre traitement anticancéreux durant l’étude - Pas de traitement anticancéreux pendant l’étude. - Traitement expérimentale 30 jours avant l’étude - Participation à une autre étude - Etat social ou psychique ne permettant pas une bonne compliance au traitement et au suivi médical - Allergie au polysorbate 80 Scanner du cavum J-7 J1 x x x x x x x Echographie cardiaque Biopsie médullaire Optionnelle Hématologie x x x Echographie abdominale Scintigraphie osseuse ECG Biochimie Evènements Indésirables J22 J36 x x x J43 J57 x x x J64 x x x x x x x x x x Rx du thorax J14 J64-J71 J127-J148 x x x x x Follow-up x x Tous les 3 mois x 1 fois/ an Tous les 3 mois 1 fois/an 1 fois /an 1 fois / an x x x x x x x x x x x x x x x x x x x x x x