L Carcinome radio-induit de la langue, secondaire au traitement

CAS CLINIQUE
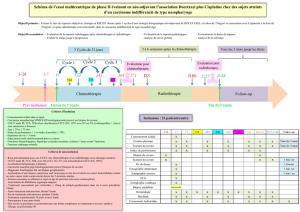
◀ Figure 1. TDM
du cavum en coupe
coronale montrant
le cancer du cavum
infiltrant les parois
postéro-supérieure
et latérales avec lyse
osseuse.
◀ Figure2. IRM
en coupe sagittale
montrant la tumeur
de la base de la langue
infiltrant le plancher
buccal.
26 | La Lettre d’ORL et de chirurgie cervico-faciale • n° 320 - janvier-février-mars 2010
Mots-clés
UCNT – Cancer radio-induit – Chimiothérapie
Keywords
UCNT – Radiation-induced carcinoma – Chimiotherapy
Carcinome radio-induit de la langue,
secondaire au traitement
d’un carcinome indifférencié du cavum
Tongue cancer after primary radiotherapy for nasopharyngeal carcinoma
A. Elboukhari*, M. Toiti*, K. Nadour*, N. Erami*, A. Eljalil*, A. Zouhair**
* Service ORL, hôpital militaire Mohamed-V de Rabat, Maroc.
** Service ORL, hôpital militaire Moulay-Ismaïl, Meknes, Maroc.
L
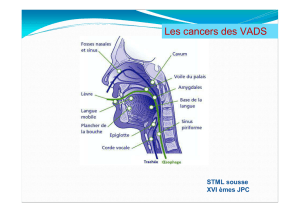
a première localisation des cancers des voies aéro-diges-
tives supérieures est représentée au Maroc par le cancer
du cavum. Il s’agit essentiellement de cancers indifféren-
ciés (undifferentiated carcinoma of nasopharyngeal type
[UCNT]) qui touchent les deux sexes avec une répartition
bimodale : un premier pic de fréquence est constaté entre
10 et 25 ans, et un deuxième pic au-delà de 60 ans. Le trai-
tement fait appel à la chimio-radiothérapie. Des tumeurs
malignes secondaires, de type épidermoïde, survenant dans
le champ d’irradiation ont été rapportées dans la littérature
(1, 2). Le risque de développer un cancer de la langue après
une radiothérapie pour cancer nasopharyngé était de 0,13 %
par an, mais semble en augmentation (1).
Observation
Il s’agit d’un patient âgé de 43 ans, traité en 1996 pour UCNT
du cavum de stade III, infiltrant au scanner les parois postéro-
supérieure et latérales du rhinopharynx avec adénopathie
cervicale gauche (figure 1). Le patient a reçu une chimiothé-
rapie en 3 cures à base de cisplatine 100 mg/ m2 et épirubicine
70 mg/m
2
. Puis, une radiothérapie lui a été délivrée en 1 dose
de 70 Gy sur le cavum et sur les aires ganglionnaires cervicales.
Dix ans plus tard, dans le cadre du suivi post-thérapeutique,
on a constaté l’apparition d’une tumeur bourgeonnante de la
moitié gauche de la base de la langue, infiltrant la vallécule
gauche, le sillon amygdaloglosse gauche et les muscles mylo-
hyoïdien et génioglosse (figure 2). Cette lésion était isolée,
sans adénopathie cervicale satellite, et le cavum était libre.
L’étude histologique de la tumeur a permis le diagnostic de
carcinome épidermoïde infiltrant, moyennement différencié.
Le patient a refusé le traitement chirurgical, mais a accepté

CAS CLINIQUE
La Lettre d’ORL et de chirurgie cervico-faciale • n° 320 - janvier-février-mars 2010 | 27
une chimiothérapie, qui a commencé avec 4 cures à base de
cisplatine à la dose de 60 mg/j pendant 3 jours et fluoro uracile
(5-FU) à la dose de 950 mg/j pendant 4 jours. Une nette amélio-
ration clinique a été constatée, avec une régression importante
de la masse tumorale ; seule une petite induration persistait à la
palpation du lit tumoral.
Trois mois plus tard, le patient est revenu pour une dysphagie
et une réduction importante de la mobilité linguale. L’examen
endobuccal a révélé une reprise évidente de l’évolution tumorale.
Une deuxième série de 3 cures de chimiothérapie a été instaurée, à
base de cisplatine (120 mg), docétaxel (130 mg) et 5-FU (1 700 mg)
répartis sur 4 jours.
Les suites ont été marquées par une altération importante de l’état
général, avec une anémie sévère et une cachexie. Le patient est
décédé dans les 2 mois qui ont suivi la fin de la chimiothérapie.
Discussion
Les effets carcinogènes de l’irradiation ionisante ont été décrits
chez les survivants de l’attaque à la bombe atomique et chez
les patients ayant reçu une radiothérapie. Le mécanisme exact
dans la genèse tumorale reste encore mal connu (3). Les tumeurs
secondaires survenant en territoire irradié sont rares. Dans les
séries publiées, leur fréquence varie entre 0,15 et 0,75 % (1, 4).
Tous les types tissulaires peuvent être transformés par l’irradia-
tion (5) ; la radiosensibilité est différente selon l’organe irradié.
Seule l’épidémiologie permet de révéler le risque de tumeurs
radio-induites. Il n’y a pas actuellement de différence cytologique
ni histologique entre une tumeur spontanée et une tumeur radio-
induite (6). Au niveau des voies aérodigestives supérieures, la
cavité buccale et l’oropharynx sont les plus touchés, avec une
fréquence élevée des carcinomes de la base de la langue (1, 4).
Les tumeurs secondaires radio-induites de la langue sont une
complication exceptionnelle de la radiothérapie des UCNT. Elles
surviennent en moyenne 10 ans après l’irradiation (1), et leur
incidence augmente avec l’amélioration de la survie des patients
après la radiothérapie d’un cancer du cavum. Ces tumeurs secon-
daires de la langue surviennent typiquement au niveau de la
base de la langue après une dose d’irradiation significativement
importante (estimée à environ 60 Gy). Une relation inverse entre
la dose d’irradiation et la période de latence des cancers solides
est en voie d’être établie pour les cancers secondaires de la
langue (1). Le diagnostic histologique est parfois difficile à poser
à cause de la fibrose et de la nécrose tumorale, et il est nécessaire
de recourir à l’immunohistochimie pour affiner le diagnostic (2).
Il s’agit le plus souvent d’un carcinome épidermoïde qui s’ob-
serve chez des sujets jeunes, sans aucun des facteurs de risque
classiques des cancers des voies aérodigestives supérieures.
L’origine radio-induite de la tumeur secondaire ne peut être
confirmée que par une étude cytogénétique montrant beaucoup
d’anomalies du caryotype avec délétions/réarrangements de
gènes et mutations des gènes suppresseurs de tumeurs (2, 7).
En effet, l’évolution la plus souvent observée dans la plupart des
cancers radio-induits, excepté le cancer de la thyroïde, se fait
selon un mode monosomique par perte de gènes suppresseurs de
tumeurs (8, 9). Plusieurs facteurs de risque semblent influencer
l’apparition de ces tumeurs secondaires, en particulier la dose
d’irradiation, paramètre variable en fonction des organes irradiés,
le type de chimiothérapie qui semble potentialiser l’effet de la
radiothérapie, le jeune âge (les enfants sont particulièrement
sensibles à la radio-oncogénèse) et une prédisposition génétique
aux tumeurs multiples (2, 3).
Le traitement des cancers secondaires de la langue diagnostiqués
à un stade avancé donne de mauvais résultats. La chimiothérapie
peut représenter une alternative thérapeutique à la chirurgie si le
malade est inopérable ou s’il refuse l’intervention. Le pronostic
est défavorable, la survie moyenne étant inférieure à 1 an (2).
Le risque de radio-oncogenèse de la langue doit être minimisé
en utilisant la radiothérapie moderne conformationnelle tridi-
mensionnelle en l’absence d’un envahissement oropharyngé ou
parapharyngé de l’UCNT (1). Le cancer radio-induit de la langue
survenant après une longue période de latence, le suivi après radio-
thérapie ne doit subir aucune relâche afin d’aboutir au diagnostic
dans les meilleurs délais.
Conclusion
Les tumeurs radio-induites de la langue secondaires à
l’irradiation thérapeutique d’un cancer du cavum sont rares.
Leur diagnostic est difficile et tardif. L’incidence croissante
des complications inhabituelles des cancers du cavum impose
le recours à des protocoles mieux adaptés utilisant, dans la
mesure du possible, une chimiothérapie moins cancérigène et
une radiothérapie conformationnelle. Le mauvais pronostic
des tumeurs secondaires de la langue invite à établir une
surveillance régulière prolongée après toute radiothérapie
pour tumeur du cavum. ■
1. Teo PML, Chan ATC, Leung SF et al. Increased incidence of tongue cancer
after primary radiotherapy for nasopharyngeal carcinoma – the possibility of
radiation carcinogenesis. Eur J Cancer 1999;35(2):219-25.
2. Boussen H, Kochbati L, Oueslati Z et al . Cancers métachrones après traite-
ment des carcinomes indifférenciés du cavum. Ann Otolaryngol Chir Cervico-
Fac 2004;121(5): 282-5.
3. Chauveinc L, Lefevre S, Malfoy B, Dutrillaux B. Actualités sur les tumeurs
radio-induites : les études génétiques. Bull Cancer 2002; 89: 181-96.
4. Wang CC, Chen ML, Hsu KH et al. Second malignant tumors in patients with
nasopharyngeal carcinoma and their association with Epstein-Barr virus. Int J
Cancer 2000;87:228-31.
5. Chauveinc L, Giraud P, Dahnier S, Mounier N, Cosset JM. Les tumeurs so-
lides induites par une radiothérapie : revue de la littérature et évaluation des
risques. Cancer Radiother 1998;2:12-8.
6. Robinson E, Barderoma R, Rennert G, Neugut AL. A comparison of the cli-
nical characteristics of second primary and single primary sarcoma: a popula-
tion based study. J Surg Oncol 1992;50:263-6.
7. Sigurdson AJ, Irene MJ. Second cancer after radiotherapy: any evidence for
radiation-induced genomic instability? Oncogene 2003;22:7018-27.
8. Chauveinc L, Dutrillaux A, Validire P et al. Cytogenetic study of eight
new cases of radiation-induced solid tumors. Cancer Genet Cytogenet
1999;114:1-8.
9. Zattara-Cannoni H, Roll P, Figarella-Branger D et al. Cytogenetic study
of six cases of radiation-induced meningiomas. Cancer Genet Cytogenet
2001;126:81-4.
Références bibliographiques
1
/
2
100%