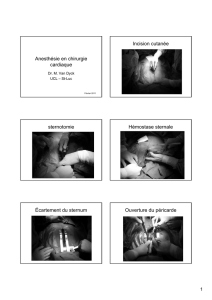
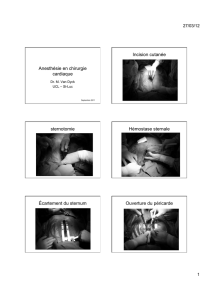
clampage aortiques prolongés

Clampages aortiques
prolongés
Ahmed Aziz KHALIFA
service de chirurgie
cardiaque, thoracique et
vasculaire
CHU BREST

INTRODUCTION

De nombreux travaux fondamentaux ont
permis de comprendre les lésions
tissulaires dues à l’ischémie et à la
reperfusion et ainsi, de développer les
bases biochimiques théoriques de la
protection du myocarde.
Cependant, aujourd’hui, personne ne peut
répondre à cette question : “quelle est la
meilleure protection myocardique ? ”.
Jusqu’à présent, une longue durée de
clampage aortique était considérée
comme un facteur de risque prédictif de
la mortalité et de la morbidité opératoires

L’efficacité
d’une technique de protection
myocardique n’est pas toujours facile
à évaluer d’autant que les études
cliniques prospectives randomisées
ne sont pas toujours ni réalisables ni
réalisées.

La fin des années 90 a vu augmenter
l’incidence de l’athérome coronaire
extensif diffus dans notre
recrutement développement de la
reconstruction coronaire
Leur nombre, la longueur de
l'artériotomie nécessaire, la difficulté
de l'éventuelle endartériectomie et le
contrôle de la paroi résiduelle
ont demandé du temps.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
1
/
30
100%