(préparation de l`allyl-2

Travaux Pratique
Chimie Organique
Semestre d’hiver 1997-98
(préparation de l’allyl-2-phénol)
Mars 1998 Julien Hutin

I. Introduction :
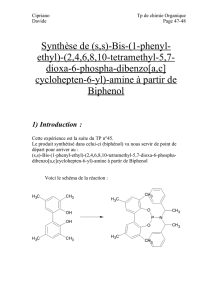
Nous allons synthétiser l’allyl-2-phénol à partir de l’allylphényléther.
◊ Schéma de la réaction :
II. Théorie :
◊ Mécanisme :
Le réarrangement de Claisen est une réaction concertée où intervient le mouvement de six
électrons. Cette réaction insolite est enclenchée par l’existence de la liaison phényle-oxygène.
L’intermédiaire formé est un isomère à haut contenu énergétique, celui-ci s’énolise pour
donner le produit final.
III. Partie pratique :
◊ Mode opératoire :
Nous plaçons 4,5 g d’allylphényléther, 5 pierres à ébullition dans un ballon surmonté d’un
réfrigérant. Nous chauffons à reflux (200°C) pendant 6h½, voici les mesures de l’indice de
réfraction (dès que l’on a atteint 1,544, la réaction s’est déroulée). Nous n’avons pas pu mesurer
les indices de réfraction entre 210 et 590 min, car le laboratoire était fermé, un assistant a éteint
le bain d’huile à 20h. Le dernier indice a été mesuré le lendemain
OH
O
OO
H
OH

Temps (minutes) Indice de réfraction
0 1,522
30 1,522
60 1,522
90 1,524
120 1,526
150 1,528
180 1,531
210 1,536
590 1,547
.
Notre solution a eu le temps de refroidir pendant toute la nuit, donc nous pouvons
dissoudre le produit 10 ml de NaOH 5M, on extrait avec 2 portions de 20 ml de pentane. On
acidifie la phase aqueuse avec une solution de HCl 6M et on extrait avec trois portions de 25 ml
d’éther. On sèche les phases organiques sur le sulfate de magnésium, on filtre la solution avec un
papier plissé et on évapore le solvant.
Finalement, le produit est distillé sous pression réduite (133°C, 20mmHg).
♦ Spectre Infrarouge :
IR (cm-1) 3672, 3076, 1588, 1497, 1327, 1264, 1207, 917
En comparant le spectre obtenu à la référence, on a de la peine à voir des similitudes,
pourtant nous avons les pics les plus importants, mais les deux spectres n’ont pas la même allure,
elles sont vaguement similaires.
D’abord, on peut dire que les pics successifs allant de 1327 à 1588 ppm représentent le
cycle aromatique et la double liaison. La double liaison se voit aussi par les pics à 917 et 3076
ppm, il ne reste plus que les pics à 3672 ppm pour la fonction alcool. A première vue, nous
avons obtenu le bon produit.
♦ Spectre RMN :
En comparant notre spectre à la référence, on peut remarquer qu’ils sont identiques. Les
quatre hydrogènes bleus sont exprimés par les pics multiplets à 7,2 (bleu foncé) et à 6,8 (bleu
clair) ppm. Le pic de l’hydrogène de la fonction alcool et les pics des hydrogènes roses sont
confondus, ils se trouvent à 5,2 ppm. L’hydrogène rouge est dans le pic multiplet à 6,0 ppm et
les hydrogènes verts sont dans le doublet à 3,4 ppm.
Il ne reste plus qu’à vérifier ces hypothèses à l’aide «des mesures » des intégrales, on peut
remarquer immédiatement que les proportions sont respectées, sauf pour les hydrogènes du cycle
aromatiques, ils sont au nombre de quatre et l’intégrale indique qu’il y en a cinq.
H H
OH
H
H
HHH
HH

Nous avons certainement de l’acétone dans notre échantillon, car son pic se situerait dans
cette zone, à part cela nous avons le bon produit.
RMN 1H (CDCl3) δ 3,4(d, 2H) ; 5,2 (t, 3H) ; 6,0 (m, 1H) ; 6,8 (m, 2H) ; 7,2 (m, 2H)
♦ Rendement :
Nous avons obtenu 0,8 g d’allyl-2-phénol, ce qui nous fait un rendement de 18%.
C’est un résultat assez satisfaisant, car on a gaspillé un ou deux ml de notre produit en
mesurant l’indice de réfraction et notre matériel n’est pas adéquat pour de si petite quantité (pour
l’extraction et la distillation).
IV. Annexes :
¾ Feuille de toxicité.
¾ Spectre infrarouge de l’allyl-2-phénol avec spectre de référence.
¾ Spectre RMN de l’allyl-2-phénol avec spectre de référence.
V. Bibliographie :
¾ Aldrich Library of IR Spectra
¾ Aldrich Library of NMR Spectra
¾ Catalogue Fluka, édition 1996/97
¾ Index Merck, édition 1996
¾ Handbook
¾ Traité de Chimie Organique, Vollhardt, Schore, 2ème édition, DeBoeck Université,
p.884 et suivante
1
/
4
100%