accès à la ressource

Thème : OBSERVER : Analyse spectrale
COMPRENDRE : Lois et modèles : Structure et transformation de la matière
Type de ressources : spectre infrarouge et RMN
Notions et contenus :
- Spectre IR : identification de liaisons à l’aide du nombre d’onde correspondant ;
détermination de groupe caractéristique
- Spectre RMN du proton : Identification de molécules organiques (déplacement chimique,
courbe d’intégration, multiplicité du signal)
- Transformation en chimie organique : modification de groupe caractéristique, les grandes
catégories de réaction : substitution, addition, élimination.
Compétences travaillées ou évaluées :
- Exploiter un spectre IR pour déterminer des groupes caractéristiques à l’aide de tables de
données ou de logiciels.
- Associer un groupe caractéristique à une fonction dans le cas des alcool, aldéhyde, cétone,
acide carboxylique, ester, amine, amide.
- Connaître les règles de nomenclature de ces composés ainsi que celles des alcanes et des
alcènes.
- Relier un spectre RMN simple à une molécule organique donnée, à l’aide de tables de
données ou de logiciels.
- Identifier les protons équivalents. Relier la multiplicité du signal au nombre de voisins.
Nature de l’activité : Classe entière
Résumé : Identifier le produit d’hydratation du but-1-ène dans des conditions différentes en
réinvestissant les connaissances de spectroscopie IR et RMN
Montrer que la spectroscopie infrarouge est idéale pour confirmer la présence de groupements
fonctionnels et que la RMN valide la structure même de la molécule.
Mots clefs : addition, hydratation, RMN, infrarouge, groupes caractéristiques, alcool, alcène.
Académie où a été produite la ressource : NANTES
http://www.pedagogie.ac-nantes.fr/02021464/0/fiche___pagelibre/

Sciences physiques et chimiques
Analyse spectrale-Structure et transformation de la matière
Table des matières
1. Situation de l'activité dans la progression
2. Activité possible
3. Exemple de questionnement
4. Analyse des spectres
1. Progression et situation de l’activité
- PARTIE : COMPRENDRE / STRUCTURE ET TRANSFORMATION DE LA MATIERE.
Représentation spatiale des molécules
- PARTIE : COMPRENDRE / TEMPS, MOUVEMENT ET EVOLUTION
1. Temps et évolution chimique : cinétique et catalyse
2. Transformation chimique en chimie organique
- PARTIE : OBSERVER / ondes et matière
Analyse spectrale : UV, Infrarouge et RMN.
Cette activité se situe après avoir traité l’ensemble de ces notions.
Il s’agit de réinvestissement et d’approfondissement :
Reconnaître les groupes caractéristiques dans les alcools, acide carboxylique,
ester, aldéhyde, cétone, amine et amide.
Utiliser le nom systématique pour en déterminer les groupes caractéristiques
et la chaîne carbonée.
Déterminer la catégorie d’une réaction (substitution, addition, élimination) à
partir de l’examen de la nature des réactifs et des produits.
Exploiter les spectres RMN et IR.
Objectif : Exploitation de spectre IR et RMN autour de différente transformation
Site ressource pour les spectres IR et RMN :
http://riodb01.ibase.aist.go.jp/sdbs/cgi-bin/direct_frame_top.cgi

2. Activité possible :
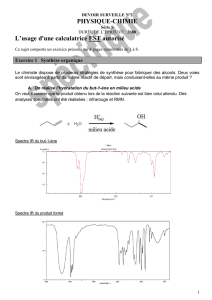
Le chimiste dispose de plusieurs stratégies de synthèse pour fabriquer
des alcools. Deux voies sont envisagées à partir du même réactif de
départ, mais conduisent-elles au même produit ?
A. On réalise l’hydratation du but-1-ène en milieu acide
Comment s'assurer que le produit obtenu lors de la réaction suivante est bien celui
attendu ? Des analyses spectrales ont été réalisées : infrarouge et RMN.
Spectre IR du but-1-ène
Spectre IR du produit formé

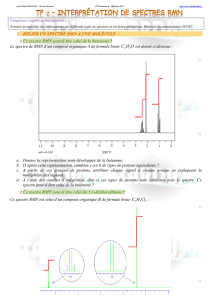
Spectre RMN du produit 1 obtenu.
En rouge on a les résultats de la courbe d’intégration.
B. La réaction est réalisée dans d’autres conditions (hydroboration
BH3 puis action de H2O2 en milieu basique).
La chaine carbonée n’est pas modifiée. Obtient-on le même produit ?
s= singulet / t= triplet /M= multiplet
Spectre RMN :
(ppm)
0,94
1,39
1,53
2,24
3,6
intégration
3H
2H
2H
1H
2H
signaux
t
M
M
s
t

3. Exemple de questionnement possible.
A. On réalise l’hydratation du but-1-ène en milieu acide
- De quel type de réaction s’agit-il ? Justifier.
- La réaction ne se fait pratiquement pas si le milieu n’est pas acidifié, quel est
le rôle des ions H+(aq) ?
- Quelle sont les fonctions présentes sur le réactif et le produit de la réaction ?
- Rechercher dans les tables les bandes caractéristiques de chacune de ces
fonctions.
- Que doit-on observer sur le spectre Infrarouge du produit attendu ou, que ne
doit-on plus observer ?
- A partir de l’étude des spectres infrarouges du but-1-ène et du produit obtenu
que pouvez-vous conclure ?
- Interpréter le spectre RMN du produit, confirme-t-il les conclusions
précédentes ?
B. La réaction est réalisée dans d’autres conditions (hydroboration BH3 puis action
de H2O2 en milieu basique).(la chaine carbonée n’est pas modifiée)
- Quels renseignements nous donne le spectre infrarouge ci-dessous du
produit formé.
- S’agit-il du même produit que dans la réaction 1 ? Justifier.
- Proposer une formule développée pour ce composé isomère du précédent.
- Cette structure est-elle compatible avec le spectre RMN du composé
obtenu ?
- Conclure sur l’influence des conditions opératoires lors d’une synthèse ?
 6
6
 7
7
1
/
7
100%