DS2 analyse spectrale

1
DEVOIR SURVEILLE N°2
PHYSIQUE-CHIMIE
Série S
DURÉE DE L’ÉPREUVE : 2h00
L’usage d'une calculatrice EST autorisé
Ce sujet comporte un exercice présenté sur 4 pages numérotées de 1 à 8.
Exercice 1 Synthèse organique
Le chimiste dispose de plusieurs stratégies de synthèse pour fabriquer des alcools. Deux voies
sont envisagées à partir du même réactif de départ, mais conduisent-elles au même produit ?
A.
On réalise l’hydratation du but-1-ène en milieu acide
On veut s’assurer que le produit obtenu lors de la réaction suivante est bien celui attendu.
Des
analyses spectrales ont été réalisées : infrarouge et RMN.
Spectre IR du but-1-ène
Spectre IR du produit formé

2
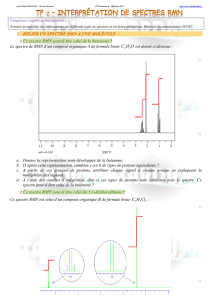
Spectre RMN du produit 1 obtenu.
Les chiffres correspondent aux résultats de la courbe d’intégration.
Questions :
- 1. Quelle sont les fonctions présentes sur le réactif et le produit de la réaction ?
- 2. Rechercher dans les tables les bandes caractéristiques de chacune de ces fonctions.
- 3. Que doit-on observer sur le spectre Infrarouge du produit attendu ou, que ne doit-on
plus observer ?
- 4. A partir de l’étude des spectres infrarouges du but-1-ène et du produit obtenu que
pouvez-vous conclure ?
- 5. Interpréter le spectre RMN du produit, confirme-t-il les conclusions précédentes ?
B.
La réaction est réalisée dans d’autres conditions (hydroboration BH
3
puis action
de H
2
O
2
en milieu basique).
La chaine carbonée n’est pas modifiée. Obtient-on le même produit ?
La réaction est réalisée dans d’autres conditions (hydroboration BH
3
puis action de H
2
O
2
en
milieu basique).(la chaine carbonée n’est pas modifiée)
Questions :
-
6. Quels renseignements nous donne le spectre infrarouge ci-dessous du produit
formé.
-
7. S’agit-il du même produit que dans la réaction 1 ? Justifier.
-
8. Proposer une formule semi-développée pour ce composé isomère du précédent.
-
9. Cette structure est-elle compatible avec le spectre RMN du composé obtenu ?
- 10. Conclure sur l’influence des conditions opératoires lors d’une synthèse ?

3
s= singulet / t= triplet /M= multiplet
Exercice 2 Synthèse de la vanille
δ (ppm)
0,94 1,39 1,53 2,24 3,6
intégration 3H 2H 2H 1H 2H
signaux t M M s t

4

Exercice 3
On considère la molécule de formule brute
On examine son spectre IR
On considère la molécule de formule brute
C
5
H
10
O
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%