Traitement médical des rechutes (récidives) précoces

Traitement médical des rechutes (récidives)
précoces
B. Weber
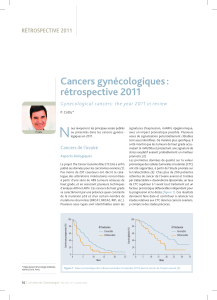
Quelques définitions
La rechute ou la récidive d’un cancer de l’ovaire se traduit par une ou des
masses tumorales cliniques et/ou radiologiques avec ou sans symptômes
(douleurs, occlusion intestinale…), voire uniquement par l’élévation persis-
tante du taux de Ca-125 (élévation du marqueur à plus de deux fois la normale
confirmée par un deuxième prélèvement un mois plus tard (1). La progression
tumorale peut s'observer en cours de chimiothérapie.
La définition du caractère précoce de la rechute n’est pas univoque : moins
de douze, six, quatre ou trois mois après la dernière cure de chimiothérapie
selon les auteurs. Ceci rend particulièrement difficile l’interprétation des
données de la littérature.
La rechute précoce est interprétée comme une résistance à la chimiothé-
rapie. Il s’agit d’une résistance au platine et/ou aux taxanes qui sont le plus
souvent utilisés en association lors du traitement initial, même si on parle
abusivement de « résistance au platine ».
Il faut noter qu'une poursuite évolutive sous traitement ou une reprise évolu-
tive moins de six mois après le dernier cycle de chimiothérapie n’ont pas la
même signification surtout si, dans ce dernier cas, une réponse partielle clinico-
radiologique ou biologique (décroissance du taux de Ca 125) a été observée.
La population des patientes « rechutant précocement » est donc hétérogène
sur le plan tumoral.
On distingue un peu artificiellement : les tumeurs dites « réfractaires » au
platine qui progressent sous traitement, les « résistantes » qui ne répondent pas
ou récidivent moins de trois ou quatre mois après la dernière cure de chimio-
thérapie et les tumeurs de « sensibilité intermédiaire » qui répondent de façon
fugace au traitement, la récidive survenant entre quatre et six voire douze mois
après la dernière cure.
Cette terminologie n’est pas utilisée dans toutes les publications et la
nuance entre réfractaire et résistante n’est pas toujours établie, les termes sont
parfois synonymes.

Pour résumer, les rechutes dites précoces concernent les tumeurs résistantes ou
réfractaires au platine regroupant les situations cliniques suivantes : progression
d'emblée sous platine, ou absence totale de réponse, ou réponse fugace et progres-
sion, ou réponse tumorale suivie d'une rechute dans un délai de moins de six mois.
Réversion de la résistance au platine
De nombreux travaux ont été réalisés dans le but de lever ou contourner la
résistance au platine (2) et au paclitaxel (3) en sachant que les mécanismes de
cette résistance ne sont pas totalement élucidés : la glycoprotéine 170 de la
pompe MDR a été impliquée, conduisant à des tentatives thérapeutiques d'in-
hibition (voir chapitre « Nouvelles tentatives médicamenteuses »).
Certains produits ont été proposés pour contourner la résistance au platine :
gemcitabine (4), topotecan (5), celocoxib (6), mifepristone (7). L’association
du tamoxifène au carboplatine ne permet pas de lever la résistance MDR (8).
D’autres produits sont en expérimentation (9, 10).
On a également proposé pour contourner une résistance relative de modifier
le rythme d’administration du cisplatine ou du paclitaxel (en hebdomadaire par
exemple) ou d'augmenter la dose de cisplatine (200 mg/m2toutes les trois
semaines (11)) Ces moyens se révèlent peu efficaces et souvent très toxiques.
Quels médicaments en cas de rechute précoce?
Le traitement de la première rechute d’une tumeur résistant au platine et/ou
paclitaxel fait appel à des molécules en principe sans résistance croisée avec le
platine : en particulier, il ne semble pas y avoir de résistance croisée entre platine
et paclitaxel comme en témoigne l’efficité du paclitaxel après échec du platine
(12) et l’efficacité du platine après échec du paclitaxel en monothérapie (13).
Il n’y a pas de standard reconnu pour le traitement des tumeurs « résistant »
au platine. Les produits les plus fréquemment utilisés sont : topotecan, pacli-
taxel, etoposide, gemcitabine doxorubicine liposomale pégylée et docetaxel.
Topotécan, paclitaxel et doxorubicine liposomale pégylée ont montré leur
intérêt dans des essais randomisés de phase III (17, 36) : à ce sujet on peut citer
les recommandations anglaises du National Institute for Health and Clinical
Excellence (http://www.nice.org.uk) : le paclitaxel est recommandé en mono-
chimiothérapie en cas de tumeur réfractaire ou résistante au platine ou en cas
d'allergie au platine, la doxorubicine liposomale pégylée est recommandée en
option en cas de tumeur réfractaire, résistante ou partiellement sensible (inter-
valle libre de 6 à 12 mois) au platine ou en cas d'allergie au platine, le
topotécan est recommandé en cas de tumeur réfractaire ou résistante au platine
ou en cas d'allergie au platine pour les malades où paclitaxel et doxorubicine
liposomale sont considérés inappropriées.
406 Les cancers ovariens

Les taux de réponse à différentes molécules sont rapportés dans le tableau I,
où a été précisé chaque fois que possible : le type de résistance au platine ou
Traitement médical des rechutes (récidives) précoces 407
Tableau I – Taux de réponse à différentes drogues selon l'état de résistance au platine.
PRODUIT Chimio Nb Réfr. Rés. Délai RÉPONSE Réf
thérapie ptes Rechut. /DURÉE
Docetaxel Pt Px 30 + < 3 10% dr 3-6 m 14
Doxo liposomale pégylée Pt Px 49 + 9% 15
Doxo liposomale pégylée Pt Px 78 + 13,7% 16
Doxo liposomale pégylée Pt 130 + 12% ssp 9 sem 17
Doxo liposomale pégylée Pt 14 + 23% 18
Capecitabine Pt 29 + multi- 29% ssp 3,7 m
traitées sg 8 m 19
Capecitabine Pt 35 + 9% ssp 2,3 m
sg 7,1 m 20
Oxaliplatine* Pt 23 + + 4,3% 6 m 29
Oxaliplatine Pt +/- Px 29 + 5,6% 30
Oxaliplatine Pt + 6% 31
Etoposide PO Pt 41 + + < 6 26,8% ssp 5,7 m
(Pt Px) (25) sg 10,8 m 21
Gemcitabine Pt Px 51 + < 3 16% dr 4 m 22
Gemcitabine Pt Px 35 + 42,9% ssp 6 m
dr 11 m sg 12 m 4
Gemcitabine Pt 21 + multi- 9,5% RC 23
traitées 38% R CA125
Hexaméthylmélamine Pt 30 + + 10 % 24
Hexaméthylmélamine Pt 26 + < 6 9,7% ssr 10 sem 25
sg 34 sem
Ifosfamide Pt 32 + + 28 % 26
Irinotecan Pt 31 + + 17 % 27
Melphalan Pt 22 + < 6 0 28
Paclitaxel Pt 1000 + (3 lignes) 22 % ssp 4,5 m 12
Paclitaxel hebdomad. Pt Px 51 + + 25% 32
Tamoxifène 568, multi- 10 % 33, 34
623 traitées
Topotecan Pt Px 43 + 11,6% ssp 2,7 m 35
sg 6 m
Topotecan Pt 124, + 6% ssp 19 sem 17
113 sg 63 sem 36
Topotecan hebdo. Pt 10 + 52 % ssp 4,9 m 37
Vinorelbine** Pt 28 + + < 12 21% ssp 3 m 38
* testé sur patientes considérées résistantes au platine après plusieurs lignes (39).
** testé sur patientes multitraitées (40).

l’association platine-paclitaxel (réfractaire ou résistante), la durée de l’intervalle
libre de chimiothérapie, le taux de réponse, la durée de réponse, la survie sans
progression et la survie globale de la population.
Les taux de réponse ne dépassent pas 20 à 30% pour une durée générale-
ment inférieure à douze mois, les taux de réponse sont les plus bas pour les
tumeurs réfractaires progressant sous chimiothérapie.
Après monothérapie (topotecan, doxorubicine liposomale pégylée, gemcita-
bine, docetaxel), les patientes n'ayant pas répondu au traitement ou rechutant
moins de trois mois après la dernière cure ont une médiane de survie de six mois
(1-37 mois) avec exceptionnellement des survivantes à « long terme » (un an)
dont il est difficile de dire si cela traduit l’efficacité des chimiothérapies ou « l’in-
dolence » de la maladie (41).
Mono- ou polychimiothérapie?
Le taux élevé de rechutes des cancers aux stades III-IV incite à considérer cette
maladie comme chronique. Des traitements successifs utilisant différents
produits sur un mode séquentiel sont une option envisageable, l'objectif étant
de contrôler le mieux possible les effets secondaires de la chimiothérapie et de
préserver la qualité de vie des malades : doxorubicine liposomale pégylée puis
docetaxel (42), topotecan puis doxorubicine (43)…
Mais l’occlusion intestinale par évolution de la carcinose péritonéale est une
menace fréquente qui encourage l'utilisation des drogues en associations pour
augmenter la probabilité de réponse, comme on peut le constater dans le
tableau II, ceci souvent au prix d’une augmentation de la toxicité. Cependant,
rares sont les études randomisées (44), encore plus rares les preuves de la supé-
riorité d'une association sur une monochimiothérapie, la plupart des
comparaisons étant indirectes. À titre d’exemple de l'absence de supériorité
d'une association on peut citer l’association de VP16 et d’ifosfamide (45).
La toxicité de ces protocoles est souvent importante (48 à 58% de neutro-
pénie de grade III-IV) (54, 55), voire rédhibitoire (ifosfamide + topotecan aux
doses conventionnelles en monothérapie) (62).
Évaluation de l'effet de la chimiothérapie
L’efficacité des produits de chimiothérapie et de leurs associations est jugée sur
le taux de réponses objectives (complètes et partielles) définies par les critères
WHO ou, plus récemment, RECIST. Mais il semble que la stabilisation de la
maladie ait, elle aussi, une valeur pronostique indépendante de la survie, le
bénéfice en terme de survie est comparable à celui des tumeurs en réponse
partielle (63). Habituellement les tumeurs ne progressant pas sous traitement
ni ne régressant ont une cinétique lente. En réalité, le groupe des tumeurs
« stables » comporte aussi des tumeurs dont la régression est inférieure à celle
408 Les cancers ovariens

Traitement médical des rechutes (récidives) précoces 409
Tableau II – Principales associations utilisées en deuxième ligne dans les rechutes précoces.
Association Chimio. Nombre Type résistance Réponse/survie Auteur
Carboplatine hebdo 53%
+ paclitaxel hebdo 18 < 6 m ssp 10 m 46
sg 13 m
Docetaxel 24%
+ vinorelbine 41 Rés ssp 4,5 m 47
sg 9,3 m
Oxaliplatine Pt 20 < 6 m 25% 48
+ FuFol -
Fol FOX-4 Pt Px 38 ? 29 % RO
ssp 4,8 m 49
sg 10 m
Oxaliplatine PtPx 5 Réfr 0%
+ Gemcitabine 9 0-3 m 44% 50
33 0-6 m 42%
Oxaliplatine Pt 17 Rés 26 % 51
+ Gemcitabine 3 Réfr
Oxaliplatine Pt 18 Rés 30 % 52
+ Paclitaxel
Etoposide po 32 4-12 m 91% 53
+ cisplatine hebdo* ssp 8 m sg 16 m
28 Réfr/ 46%
< 4 m ssp 5 m sg 13 m
Gemcitabine + 64%
Cisplatine J1&8/21 22 < 6 m ssp 3,9 m 54
sg 11,4 m
Gemcitabine + 40%
Paclitaxel hebdo PtPx 33 Rés ssp 5,7 m 55
sg 13,1 m
Gemcitabine PtPx 16 Réfr 25 % (R globale) 56
+ etoposide Pt 11 Rés 2 lignes dr 6 m
Topotecan IV PtPx 24 multitraitées 8% 57
+ etoposide PO
Topotecan IP 22 Rés 38% 58
+ etoposide PO
Topotecan Pt 24 Rés 30% 59
+ Ifosfamide
Irinotecan Pt 13 Réfr ? 31% 60
+ Mitomycine ssp 24 sem
sg 36 sem
Pt = platine, Px = paclitaxel Rés = résistant, Réfr = réfractaire, Rechut = rechute
D(m)rep = durée mediane de réponse
ssp = médiane de survie sans progression
sg = médiane de survie globale
m = mois
sem = semaines
* association testée en 1991 (61).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%