L’ Apport de l’angiographie de contraste numérisée quantitative dans le diagnostic

30 | La Lettre du Cardiologue ̐ n° 450 - décembre 2011
DOSSIER THÉMATIQUE
Le diagnostic de la DVDA
Apport de l’angiographie
de contraste numérisée
quantitative dans le diagnostic
de la DVDA
Contribution of quantitative digitized contrast angio-
graphy to the diagnosis of ARVD
J.-L. Hébert¹, G. Duthoit², Z. Bennoui¹, G. Kasser³, O. Gérard¹, V. Claes⁴, Y. Lecarpentier¹, ⁵
¹
Laboratoire d’explorations fonc-
tionnelles cardiovasculaires, hôpital
de Bicêtre, université Paris-Sud, Le
Kremlin-Bicêtre.
²
Unité de rythmologie, institut de
cardiologie, hôpital de la Pitié-Salpê-
trière, AP-HP, Paris.
³ École nationale supérieure des arts
et métiers, Paris.
⁴
Faculteit farmaceutische, biome-
dische en diergeneeskundige weten-
schappen, Anvers, Belgique.
⁵ Centre de recherche clinique, CHR
de Meaux.
L’
imagerie tient une place importante dans le
difficile diagnostic de la dysplasie ventricu-
laire droite arythmogène (DVDA), dont les
critères ont fait l’objet d’une révision récente (1), où
une place grandissante a été réservée aux aspects
quantitatifs, à l'échocardiographie et à la résonance
magnétique nucléaire. Cette attitude, négligée lors
de la première conférence de consensus (2), est justi-
fiée : on ne cerne scientifiquement un phénomène
qu’en le quantifiant. L’angiographie de contraste, la
plus ancienne des techniques d’imagerie, reste dans
sa version numérisée la technique de référence dans
la DVDA (3-5), car elle offre une très bonne défini-
tion des contours endocardiques et de la cinétique
pariétale des 2 ventricules. Toutefois, la morphologie
complexe du ventricule droit (VD) rend difficile (mais
non insurmontable) sa modélisation géométrique.
Nous avons développé un outil informatique dédié
à l’angiographie quantitative, qui exprime en milli-
mètres les excursions pariétales et qui permet de
classifier la DVDA sur des critères fonctionnels et
morphologiques (6). Cette démarche offre une
approche à la fois diagnostique − en particulier
dans les formes localisées, difficiles à cerner par les
techniques non invasives − et pronostique, indis-
pensable dans les formes diffuses biventriculaires,
préoccupantes en raison du risque hémodynamique
encouru. Cette technique offre en effet une vision
complète des contours de la cavité dans une inci-
dence donnée, ce qui permet de juger d’emblée la
morphologie globale de la cavité et la diffusion de
l’atteinte. Le strict respect d’un protocole dédié a
permis un rendu contributif, sans aucune mortalité
et sans morbidité appréciable, sur près d’un millier
de patients explorés pour suspicion de DVDA.
Population
Notre expérience porte sur 300 patients répondant
aux critères révisés de la DVDA (33 ans d’âge moyen,
75 % d’hommes et 60 % de sportifs s'entraînant
au moins 6 heures par semaine). Les pathologies
associées sont absentes et la coronarographie est
normale. Les résultats angiographiques des patients
sont comparés à ceux de 20 témoins soumis au
même protocole pour suspicion de diverses cardio-
pathies non confirmées.
Protocole
Les détails du protocole d’exploration ont été déve-
loppés dans un article antérieur (6). Après recueil des
pressions droites avec une sonde de Swan-Ganz et
gauches à travers une queue de cochon, on mesure
le débit cardiaque par thermodilution et la différence
artérioveineuse en oxygène.
Le facteur de grandissement des images, indispen-
sable à la calibration, est déterminé à l’aide une bille
métallique de 40 mm de diamètre filmée dans le plan
du cœur, dans les 2 incidences orthogonales retenues

La Lettre du Cardiologue ̐ n° 450 - décembre 2011 | 31
Points forts
La cinéangiographie de contraste est la technique d’imagerie de référence dans le diagnostic de la dysplasie
ventriculaire droite arythmogène. Les malades sont classifiés selon leur fraction d’éjection du ventricule
droit (FEVD), conservée ou abaissée.
>> Les malades de type I (65 %) ont une FEVD ≥35 %, des volumes VD normaux et une excursion systolique
de l’anneau tricuspide (TAPSE) respectée (>14 mm). Ils se répartissent en type Ia (45 %) avec altérations
antéroapicales limitées et en type Ib (20 %) ayant les atteintes du type Ia, associées à des déhiscences
de la paroi inférieure.
>> Les malades de type II (35 %) ont une dilatation majeure du VD, une FEVD <35 % avec TAPSE < 12mm.
Ils se répartissent en type IIa avec ventricule gauche (VG) préservé et en type IIb avec FEVG <40 %, en
défaillance cardiaque.
Mots-clés
Dysplasie ventriculaire
droite arythmogène
Diagnostic
Imagerie
Angiographie de
contraste numérisée
quantitative
Highlights
»
Quantitative cineangi-
ography can be considered
as gold standard -when
QFSGPSNFECZFYQFSUTBNPOH
PUIFSJNBHJOHUPPMTVTFEGPS
UIFEJBHOPTJTPG"37%$5IF
patients were classified on the
CBTJTPGQSFTFSWFEPSJNQBJSFE
SJHIUWFOUSJDVMBSFKFDUJPOGSBD-
tion (RVEF).
»
5ZQF*QBUJFOUTIBE
QSFTFSWFE37&'öOPSNBM
RV volumes and preserved
TAPSE (≥14mm). They were
divided into two groups: type
*BXJUIXBMMJNQBJS-
ment limited to anterior wall
BOEBQFYUZQF*CTBNF
alterations as previously, asso-
ciated with diaphragmatic wall
bulgings.
»
5ZQF**QBUJFOUTIBE
JNQBJSFE37&'BOE
5"14&NNXJUIJNQPS-
UBOU37EJMBUJPOBOEEJGGVTF
parietal alterations. They were
divided into two groups: type
**BXJUIPVU37JOGVOEJCVMBS
beating aneurism; type IIb with
37JOGVOEJCVMBSCFBUJOHBOFV-
SJTN*OUIFTFDBTFTUIFMFGU
WFOUSJDVMBS-7TZTUPMJDGVODUJPO
XBTDPMMBQTFE-7&'
with poor hemodynamic condi-
tion implying heart transplant
GPSCJWFOUSJDVMBSIFBSUGBJMVSF
Keywords
Arrhythmogenic right
ventricular dysplasia
Diagnosis
Imaging
Quantitative digitized
contrast cineangiography
pour les injections : l’oblique antérieure droite (OAD)
de 45°, et l’oblique antérieure gauche (OAG) de 45°.
L’exploration peut être complétée par une coronaro-
graphie qui montre, dans les formes dilatées, des
aspects d’étirement typiques sur le réseau marginal
droit en zone dysplasique, avec stagnation distale
en arbre mort.
Le traçage manuel des contours télédiastolique
et télésystolique sur des cycles sinusaux et non
postextrasystoliques, dans chaque incidence, permet
l’analyse segmentaire des excursions pariétales par
la technique “centerline” de FH. Sheehan et al. (7)
quantifiée (6) [figures (1 à 5)B]. L’excursion de
chaque segment est exprimée en millimètres et est
comparée à une valeur de référence, dans chaque
incidence, à l’aide d’un nomogramme établi sur les
témoins (figures [1 à 5]C). L’excursion segmentaire
est normalisée par rapport au périmètre télédiasto-
lique du contour considéré. Les volumes ventriculaires
télédiastolique et télésystolique du VD et la fraction
d’éjection du VD (FEVD) sont calculés par le modèle
géométrique de l’hémiellipsoïde de JG. Boak et al. (8).
L’analyse biplane du VG permet le calcul des volumes
et de la fraction d’éjection du VG (FEVG) par le modèle
géométrique de l’ellipsoïde de H. Dodge et al. (9),
et la comparaison de la cinétique segmentaire à un
nomogramme dans chaque incidence.
Résultats
Anomalies morphologiques
élémentaires, aspects qualitatifs
◆Ventricule droit
Le choix des incidences, non conventionnelles,
est déterminant. L’OAD 45° permet, mieux que
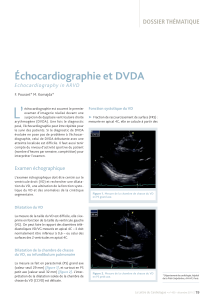
figure 1. Ventricule droit OAD 45°. DVDA type Ia.
d = 1,9 mm
Espaces
intertrabéculaires
Trabéculation
6,8 mm
AZoom
C
B
Télédiastole

32 | La Lettre du Cardiologue ̐ n° 450 - décembre 2011
DOSSIER THÉMATIQUE
Le diagnostic de la DVDA
l’OAD 30°, de visualiser le plan de l’anneau tricuspide,
refoulé à droite en cas de dilatation importante du VD,
afin de mesurer son déplacement systolique (Tricuspid
Annular Plane Systolic Excursion [TAPSE]), déterminant
majeur de la FEVD (6, 10). Cette incidence dégage
aussi parfaitement les lésions élémentaires dans les
zones du “triangle de la dysplasie” : infundibulum
pulmonaire, apex et zone sous-tricuspidienne. Elle
montre l’enchevêtrement des trabéculations de la
paroi antéroapicale et leur hypertrophie, quanti-
fiée par comparaison avec le diamètre apparent de
la sonde d’angio graphie : une épaisseur supérieure
ou égale à 4 mm des trabéculations en télédiastole
est pathologique (figures [1 et 3]A), même chez un
sportif entraîné. La zone de jonction infundibulotra-
béculaire antérieure peut présenter un bombement
akinétique, siège d’une hypertrophie trabéculaire
prenant un aspect confluant en “chou-fleur” en télé-
systole. La bandelette ansiforme est souvent hyper-
trophiée, trop bien visible. L’apex du VD peut être
amputé avec un aspect “en coup de serpe ” (figure
4A, p. 34), rarement anévrismal ; il est le siège de
l’Y renversé du système de haubanage hypertrophié
de la bandelette ansiforme. Le plancher du VD peut
présenter des déhiscences pariétales localisées, en
doigt de gant ("outpouchings"), stagnantes (figure
3A, p. 33). La zone sous-tricuspide peut présenter
un aspect en hamac ("bulging") avec distension
stagnante diastolique, voire systolodiastolique
(figures [4 et 5]A, pp. 34, 35). La zone sous-tricus-
pidienne est alors déplacée en dessous du plan de
l’apex. La cinétique de l’éperon de Wolff est égale-
ment bien vue, diminuée dans les formes diffuses avec
réduction de TAPSE, ainsi que celle de l’infundibulum
sous-pulmonaire, anévrismal à parois amincies seule-
ment dans les formes les plus diffuses (figure 5A,
p. 35). En OAD 45°, les trabéculations hypertrophiées à
projection septale prennent un aspect tabulaire ("stac-
king") avec des espaces intertrabéculaires horizontaux
parallèles médiocavitaires, et elles se superposent
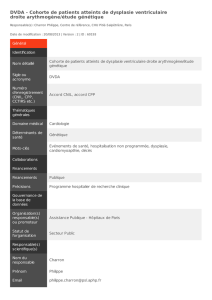
Figure 2. Ventricule droit OAG 45°. DVDA type Ia, même patiente que sur la figure 1.
A
Zoom
B
ZoomTélédiastole
Télésystole
Apport de l’angiographie de contraste numérisée quantitative
dans le diagnostic de la DVDA

La Lettre du Cardiologue ̐ n° 450 - décembre 2011 | 33
DOSSIER THÉMATIQUE
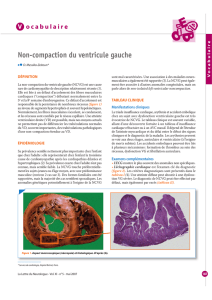
Figure 3. Ventricule droit OAD 45°. DVDA type Ib.
A
B
Télésystole
Télédiastole
C
aux images fissuraires (figure 1A, p.31). Cette inci-
dence permet enfin d’identifier et de quantifier une
éventuelle régurgitation tricuspidienne. L’OAG 45°
offre une excellente visualisation de la morphologie
et de la cinétique du septum interventriculaire (SIV),
meilleure que l’OAG 60° ou l’incidence transverse
gauche, et renseigne de façon très démonstrative sur
les interactions interventriculaires dans les formes
avec dilatation du VD. Elle permet de confirmer l’hy-
pertrophie des trabéculations à projection septale
avec des aspects d’indentations profondes en “dents
de requin”, qui se projettent sur l’ensemble du mur
septal (figure 2A, p. 32). Elle permet d’apprécier la
dilatation transversale du VD et de visualiser une éven-
tuelle déformation anévrismale de sa paroi libre. Dans
les formes diffuses, l’aspect fissuraire disparaît en
raison de la dilatation de la cavité, mais l’hypertrophie
demeure et les trabéculations apparaissent épaissies,
étirées, parallèles et fixes (figure 5A, p.35), ce qui est
confirmé en OAG, avec un aspect en “mie de pain”
dans la zone septale, verticalisée et immobile. Les
autres causes d’hyper trophie trabéculaire (commu-
nication interauriculaire [CIA], retour veineux pulmo-
naire anormal partiel [RVPAP], sténose pulmonaire à
SIV intact, hypertension artérielle pulmonaire [HTAP],
etc.) devront être éliminées.
◆Ventricule gauche
En OAD 45°, les interactions interventriculaires se
traduisent, dans les formes dilatées, par un recou-
vrement partiel de la paroi antérieure du VG par la
zone trabéculaire du VD, d’où un aspect de pseudo-
hypertrophie de la paroi antérieure avec réduction
importante de son déplacement (normale = 10 mm)
et aspect laminé en systole. L’OAG 45° permet
une bonne analyse des interactions interventri-
culaires lorsque le VD est dilaté, alors que le volume
du VG reste normal ou peu augmenté (inférieur
ou égal à 130 % de la normale), même dans les
formes diffuses. Chez le sédentaire ayant un VD

34 | La Lettre du Cardiologue ̐ n° 450 - décembre 2011
DOSSIER THÉMATIQUE
Le diagnostic de la DVDA
figure 4. Ventricule droit OAD 45°. DVDA type IIa.
ABTélésystole
Mésosystole
Zoom
Télédiastole
C
dilaté, le SIV devient paradoxal et sa face gauche
est incurvée vers le VG de taille normale, qui est
refoulé en haut et à gauche avec verticalisation
du plan de l’anneau aortique. En revanche, chez le
sportif entraîné, le VG est plus volumineux que chez
le sédentaire et les interactions interventriculaires
sont moins nettes : le SIV reste en position médiane,
mais il demeure vertical et immobile tout au long
du cycle cardiaque.
L’atteinte d’origine intrinsèque du VG est globale-
ment plus discrète que celle du VD et n’aboutit à des
répercussions sensibles que dans les formes diffuses.
Elle s’ajoute aux interactions interventri culaires
d’origine volumétrique. En OAG 45°, la cinétique
de la paroi libre du VG, qui n’est soumise qu’à la
contrainte péricardique, est le meilleur marqueur
de l’intégrité de la fonction systolique du VG : l’ef-
fondrement de son excursion (normale = 10 mm)
accompagne les formes biventriculaires sévères
et traduit une atteinte intrinsèque du VG. De
même, une paroi inférieure hypo- ou akinétique
en OAD 45° (normale = 10 mm) témoigne d’une
atteinte intrinsèque du VG, en particulier dans
la zone sous-mitrale. Toutefois, certains signes
morphologiques d’atteinte intrinsèque loco-
régionale du VG peuvent être décelés, y compris
dans des formes peu importantes à droite. Ils sont
limités, mieux vus en OAD 45°, et concernent : la
zone médioventriculaire, hypokinétique, engainée
d’un manchon fibreux sur un large segment moyen ;
la zone apicale, comblée, en “coup de serpe” ; et la
zone sous-mitrale en arrière du pilier postérieur,
donnant au VG un aspect en “ballerine”.
Anomalies cinétiques et volumétriques,
aspects quantitatifs et résultats
hémodynamiques
La démarche suivie pour établir la classification
angiographique des DVDA a consisté à focaliser
l’analyse sur le VD en raison de la constance de
Apport de l’angiographie de contraste numérisée quantitative
dans le diagnostic de la DVDA
 6
6
 7
7
1
/
7
100%