Lire l`article complet

4 | La Lettre du Cardiologue ̐ n° 450 - décembre 2011
ÉDITORIAL
DVDA, bientôt 40 ans ! L’évolution des connaissances
Right ventricular dysplasia… nearly 40 years of evolving knowledge
O
n retrouve dans la littérature médicale des descrip-
tions anatomocliniques parfois très anciennes
de cette cardiomyopathie avec transformation
adipeuse du ventricule droit (VD), mais c'est à Guy Fontaine
que revient le mérite d’avoir fait adopter la dénomination
de dysplasie ventriculaire droite arythmogène (DVDA), et
d’avoir stimulé la recherche dans la plupart des aspects de
cette maladie.
Tout a commencé avec l’apparition de la chirurgie des troubles
du rythme cardiaque, à laquelle il s’était intéressé au début des
années 70 en développant avec Gérard Guiraudon, puis avec
moi-même, la méthode de cartographie cardiaque épicardique
d’abord appliquée au syndrome de Wolf-Parkinson-White,
puis aux tachycardies ventriculaires (TV). Combinée aux
progrès des explorations électrophysiologiques endocavi-
taires, cette étude des troubles du rythme à thorax ouvert chez
des patients aux arythmies rebelles et récidivantes a permis,
tout en résolvant des cas cliniques impossibles à traiter autre-
ment par les moyens de l’époque, de mieux comprendre le
mécanisme des tachycardies. Avec les TV, notre équipe a en
particulier découvert et étudié les potentiels tardifs ventri-
culaires chez l’homme, enregistrés après la fin du QRS de
surface, en rythme sinusal et en tachycardie. Cette expérience
chirurgicale a permis de reconnaître la DVDA en tant que
nouvelle entité clinique et par ailleurs a jeté les bases des
futures méthodes d’ablation des tachycardies par cathéter.
Dans les années 60, le traitement chirurgical des TV rebelles
consistait à réséquer une cicatrice d’infarctus et grâce aux
cartographies, au début des années 70, il a été possible de
localiser la zone d’émergence épicardique, puis endocardique
de TV déclenchées en salle d’opération. Cependant, certains
patients n’avaient pas d’infarctus, et, sur le premier d’entre
eux, le chirurgien, pour rechercher une éventuelle cicatrice
endocardique − qui n’existait pas −, a pratiqué une ventricu-
lotomie sur le site d'émergence des TV sur l’épicarde gauche.
La disparition des tachycardies après l’intervention nous a
fait comprendre que nous avions probablement interrompu
un circuit de réentrée. Certaines de ces tachycardies “idio-
pathiques” venaient du VD, négligé dans les investigations
cardiologiques essentiellement centrées sur le ventricule
gauche (VG). C’est en 1973, lors de l’intervention sur le
premier patient dont les TV naissaient du plancher du VD, que
Gérard Guiraudon a remarqué que le VD était anormal, dilaté.
On enregistrait à ce niveau des potentiels très tardifs au-delà
du QRS de surface. Après la ventriculotomie, on pouvait voir
une paroi anormale et l’histologie montrait une transforma-
tion adipeuse de la paroi avec persistance d’une fine couche
endocardique. La première publication des 4 premiers cas a
soulevé la question de la dénomination appropriée de cette
affection, et c’est alors que Guy Fontaine a proposé la termi-
nologie de “dysplasie ventriculaire droite arythmogène”. Les
2 derniers termes sont évidents, et celui de "dysplasie" avait
été choisi, car le remplacement du myocarde par du tissu
adipeux évoquait une anomalie plus congénitale qu’acquise,
due à un trouble de l’organogenèse, ce qui n’était pas mal
trouvé, au vu de l’élucidation ultérieure du mécanisme géné-
tique de la DVDA.
En 1980, le Pr Frank Marcus, de Tucson, est venu passer une
année sabbatique dans notre service. Il a rédigé avec Guy
Fontaine l’article princeps paru en 1982 dans Circulation, à
partir de 24 cas colligés par notre équipe chez les patients
hospitalisés pour des TV ou pour des VD anormaux sans étio-
logie précise, décrivant les aspects anatomopathologiques,
cliniques, électrocardiographiques − dont les potentiels tardifs
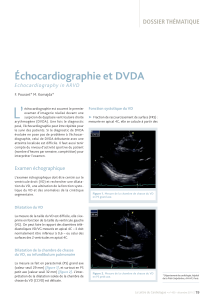
avec les ondes epsilon −, morphologiques, échographiques
et angiographiques de la DVDA.
La décennie 80 a permis de reconnaître les formes fami-
liales et la fréquence de cette étiologie dans la mort subite
des sujets jeunes, grâce notamment aux contributions de
l’équipe de Gaetano Thiene, de Padoue. Le caractère fami-
lial de cette maladie avait déjà été remarqué dans un des
cas de la publication de Marcus et dans quelques cas de
la littérature, mais il s’est précisé en 1986 avec la forme
particulière de DVDA familiale de l’île de Naxos (anomalies
des phanères, cheveux laineux et kératose palmoplantaire).
En 1988, la série de Padoue concernait 9 familles de la région

La Lettre du Cardiologue ̐ n° 450 - décembre 2011 | 5
ÉDITORIAL
vénitienne où ces formes familiales étaient particulièrement
fréquentes, de l’ordre de 70 % des cas, bien plus que les 30
à 50 % d’autres séries éditées ultérieurement. Cette même
équipe a publié la même année une proportion de 20 % de
DVDA à l’autopsie systématique de morts subites de sujets
âgés de moins de 35 ans en 6 ans, bien plus dans leur région
que les 5 et 10 % des séries lyonnaises de 1996 et 2003.
Enfin, ces études, ainsi que les séries cliniques, montraient
le rôle fréquent de l’effort dans le déclenchement des aryth-
mies, et en particulier chez les sportifs.
L’affection a ainsi été reconnue, puis classée en 1995 par
la World Health Organization dans les cardiomyopathies,
mais son diagnostic restait difficile, surtout pour les formes
localisées. Un groupe de travail coordonné par William
McKenna a proposé en 1994 une liste de critères répartis
en critères mineurs et en critères majeurs, réévalués et un
peu modifiés en 2010. C’est au cours de cette décennie que
2 autres méthodes non invasives de diagnostic ont été mises
au point, l’angioscintigraphie isotopique pour détecter les
anomalies localisées de contraction ventriculaire, et surtout
l’IRM qui pouvait aussi identifier la graisse et la fibrose dans
le myocarde, malheureusement avec des limites importantes
pour le VD.
Au début des années 2000, plusieurs cohortes de patients sont
publiées, montrant l’évolution à long terme de la maladie,
recherchant les facteurs prédictifs de mort subite, vérifiant
l’apport du défibrillateur implantable et montrant que, en
l’absence de mort subite, on voyait progressivement appa-
raître une insuffisance cardiaque à prédominance droite, et
une atteinte plus tardive du VG.
En une dizaine d'années, la biologie moléculaire va alors
complètement transformer la conception de la nature de
cette maladie. Avec la maladie de Naxos, on va identifier
entre 1998 et 2000 une mutation du gène de la plakoglo-
bine, l’un des composants du desmosome. Depuis, plusieurs
autres mutations ont été individualisées, qui concernent
en général les gènes des différentes protéines composant
le desmosome. La DVDA devient alors une cardiomyopa-
thie des jonctions intercellulaires. On peut expliquer par un
facteur mécanique l’incidence particulière de la maladie chez
les sportifs, chez qui le VD est soumis à des contraintes inha-
bituelles. Ensuite, la transformation adipeuse est attribuée
à une déviation du métabolisme de la cellule par l’accumu-
lation des précurseurs du desmosome dans son cytoplasme.
Enfin les arythmies ventriculaires étaient jusque-là expli-
quées par les anomalies histologiques de dissociation des
myocytes par la dégénérescence graisseuse favorisant
les phénomènes de réentrée. Ce phénomène est encore
accentué par un ralentissement des conductions intercel-
lulaires, lié à un déficit d’expression de la connexine 43, due
au déficit en plakophiline.
La DVDA est donc née d’une observation fortuite sur un terrain
préparé, et il est extraordinaire d’avoir pu assister en près de
40 ans à une explication des phénomènes observés de son
mécanisme grâce à la biologie moléculaire. En revanche, le
diagnostic des formes limitées est encore difficile à établir,
et l’évaluation du risque de ces formes, incertaine. Enfin
le traitement reste palliatif, essentiellement antiarythmique,
entre médicaments, ablations et défibrillateur implantable,
sans effet sur la progression de la maladie et sur l’apparition
d’insuffisance cardiaque, probablement accentuée par des
épisodes myocarditiques, comme le remarquait déjà Guy
Fontaine en 1990, ce qui nécessite, lorsqu’elle est réfractaire,
une transplantation cardiaque.
Robert Frank
Institut de cardiologie,
hôpital de la Pitié-Salpétrière, AP-HP, Paris.
1
/
2
100%