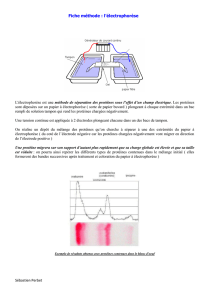
Les différentes structures des protéines

1
C. Lacombe 1
Les différentes structures des protéines
-Ala-Glu-Val-Thr-Asp-Pro-Gly-
-AEVTDPG-
Domaine
Structure primaire Structure secondaire
Structure tertiaire Structure quaternaire
Hélice
Feuillet
C. Lacombe 2
Les différentes structures des protéines
structure primaire : suite ordonnée de résidus d’acides aminés
liés par des liaisons peptidiques (= séquence)
structure secondaire : conformation spatiale répétitive régulière
de segments de la chaîne protéique (hélice , feuillet )
structure tertiaire : conformation biologiquement active (dite
native) d’une chaîne polypeptidique repliée en une structure
tridimensionnelle.
structure quaternaire : structure dans l’espace adoptée par
l’association d’au moins deux chaînes polypeptidiques distinctes
en un multimère protéique.

2
C. Lacombe 3
I - Structure primaire
Liaison peptidique
COO -
R1
CH
+3HN COO -
CH
+CH
CO - NH
CH
Liaison peptidique
+3HN +3HN
COO -
R2R1R2
CH
CO
NH
CH
CO
NH
CH
CO
NH COO -
H3N+
CH3
CH OH
2
CH SH
2
CH 2
Ala Ser Cys Gly
Alanyl Séryl Cystéinyl Glycine
Résidu
amino-
terminal
Résidu
carboxy-
terminal
ASCG
C. Lacombe 4
II -Méthode d’étude des protéines
Techniques de purification d’une protéine
* Précipitation fractionnée
* Centrifugation
* Chromatographies
* Dialyse
* Électrophorèse sur gel de polyacrylamide
* Isoélectrofocalisation
* Électrophorèse bidimensionnelle

3
C. Lacombe 5
II -Méthode d’étude des protéines
Techniques de purification d’une protéine
* Électrophorèse sur gel de polyacrylamide en
présence de SDS (SDS-PAGE)
Le SDS (Sodium Docécyl Sulfate) dénature les protéines et les charge
négativement.
Séparation des molécules en fonction de leur masse, les plus
petites migrent plus loin dans le gel (plus près de l’anode)
(Cf chapitre : Techniques)
C. Lacombe 6
L’électrophorèse
•L’électrophorèse sur gel
Le gel va ralentir la migration des grosses molécules.
Plaques de
verre entre
lesquelles le gel
a été coulé
Anode
Dépôt de
l'échantillon
Cathode

4
C. Lacombe 7
L’électrophorèse
•L’électrophorèse sur gel de polyacrylamide en
présence de SDS (SDS-PAGE)
PM
kDa
94
67
43
30
20
14
Séparation des molécules en
fonction de leur masse, les plus
petites migrent plus loin dans le gel
(plus près de l’anode)
+
-
C. Lacombe 8
II -Méthode d’étude des protéines
Techniques de purification d’une protéine
* Électrophorèse bidimensionnelle: un gel de polyacrylamide
sur lequel a été réalisé une isoélectrofocalisation (IEF) est déposé au-dessus d’un
gel de polyacrylamide-SDS (SDS-PAGE). Les protéines sont ainsi séparées dans
la première dimension en fonction de leur pHi et dans la deuxième dimension en
fonction de leur PM.
pHi
II : SDS-PAGE
pHi
Extrémité basique Extrémité acide
PM
I : IEF

5
C. Lacombe 9
II -Méthode d’étude des protéines
Détermination de la séquence d’une protéine
*Rupture des ponts disulfures
-oxydation par l’acide performique
CH -CH2-S - S -CH2- CH + H - C -O -OH
Pont disulfure acide performique
Acide cystéique
2 CH - CH2-SO3-
O
=
Inconvénients : les résidus Met sont oxydés (en méthionine sulfone) et
le Trp est détruit
C. Lacombe 10
II -Méthode d’étude des protéines
Détermination de la séquence d’une protéine
*Rupture des ponts disulfures
-réduction par le -mercaptoéthanol
CH -CH2-S - S -CH2- CH + 2 HS - CH2-CH2-OH
Pont disulfure -mercaptoéthanol
Cystéine
2 CH - CH2-SH +S -CH2-OH
S -CH2-OH
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%