La thoracoscopie médicale - Medical thoracoscopy

L
a thoracoscopie médicale est l’exploration endoscopique
de la cavité pleurale réalisée par un médecin. Elle per-
met en outre la réalisation de prélèvements biopsiques
au niveau pleural et pulmonaire, selon l’expérience de l’opérateur,
ce qui apporte infiniment plus d’informations qu’une simple biop-
sie pleurale percutanée.
Chaque fois qu’un drain thoracique est requis, il ne prend que
quelques minutes à un pneumologue pour introduire un endo-
scope par la même incision cutanée afin d’inspecter la cavité pleu-
rale, de localiser les adhérences et les brides, de prélever des frag-
ments pleuraux et de vérifier que le drain est en situation correcte.
Chez les patients présentant un cancer pleural primitif (mésothé-
liome pleural malin), c’est le seul examen qui permette un diagnostic
à un stade précoce de la maladie, et, pour les autres épanchements
pleuraux, la réalisation de biopsies sous le contrôle de la vue avec
un rendement diagnostique de plus de 95 %.
La thoracoscopie médicale, tout en permettant une exploration
complète de la cavité pleurale, est moins invasive que la thora-
cotomie (1). Les complications sont rares si elle est pratiquée en
tenant compte des recommandations appropriées. Elle est réalisée
en utilisant une ou deux portes d’entrée selon son indication. Un
drain pleural est mis en place à la fin de l’examen afin d’assurer
une réexpansion pulmonaire satisfaisante. Si des biopsies pulmo-
naires ou une symphyse pleurale sont réalisées, le drain sera laissé
en place quelques jours. Dans le cas d’une simple thoracoscopie
diagnostique avec prélèvements biopsiques au niveau de la plèvre
pariétale, le drain peut être enlevé dès l’arrêt du bullage au bocal
et contrôle clinique du retour du poumon contre la paroi. Pour pra-
tiquer une thoracoscopie, un médecin doit bénéficier d’un entraî-
nement spécifique (comme pour tout geste endoscopique), afin
d’intégrer des connaissances sur l’anatomie thoracique, sur l’uti-
lisation des instruments (pince pour biopsies, système de coagu-
lation, équipement vidéo-endoscopique, etc.) et sur la surveillance
du drainage thoracique.
ÉQUIPEMENT ET TECHNIQUE
Équipement
L’équipement requis pour une thoracoscopie rigide comprend des
trocarts (7 mm et 5 mm), des optiques et une pince porte-optique
(avec, au minimum, un angle de vision de 180°) reliées à une source
de lumière froide, et des pinces coagulantes dans le cas d’un examen
La thoracoscopie médicale
Medical thoracoscopy
L. Greillier*, A. Fraticelli*, P. Astoul*
* Département des maladies respiratoires, service d’oncologie thoracique, hôpi-
tal Sainte-Marguerite, Marseille. UPRES 3287, faculté de médecine, Marseille.
Résumé :La thoracoscopie médicale est un examen endoscopique de la cavité pleurale qui peut être réalisé par le pneumologue
sous anesthésie locale ou générale, le malade étant idéalement maintenu en respiration spontanée, après la réalisation d’un
pneumothorax artificiel. À la fin de l’intervention, un drain thoracique est mis en place afin d’assurer le retour du poumon à la
paroi. Les complications sont exceptionnelles et la mortalité est inférieure à 0,017 %. La thoracoscopie trouve son indication
principale dans le diagnostic des épanchements pleuraux, avec une sensibilité et une spécificité bien supérieures à celles de la
biopsie pleurale à l’aiguille et/ou de la cytologie du liquide. Certains gestes thérapeutiques sont réalisables par cette voie, et
principalement la pleurodèse par talc dans les cas de pleurésie ou de pneumothorax récidivants. La thoracoscopie médicale doit
faire partie des techniques endoscopiques thoraciques médicales courantes.
Mots-clés :Thoracoscopie - Pleurésie - Pneumothorax.
Summary: Medical thoracoscopy allows an endoscopic examination of the pleural cavity using local or general anesthesia, with
the patient ideally in spontaneous breathing, after induction of an artificial pneumothorax. At the end of the procedure, a chest
tube is inserted to expand the lung. Complications are rare and mortality is below 0.017%. The main indication for medical thora-
coscopy is the diagnosis of pleural effusion, and the sensitivity and specificity are clearly superior to that of needle pleural biopsy
and fluid cytology. Some therapeutic measures are mainly feasible by this route, in particular pleurodesis for recurrent pleurisy
and pneumothorax as well. Medical thoracoscopy must be included in the armamentarium of thoracic endoscopy techniques.
Keywords: Thoracoscopy - Pleurisy - Pneumothorax.
I
M A G E R I E
162
La Lettre du Pneumologue - Volume VII - n
o
4 - juillet-août 2004

nécessitant deux portes d’entrée ( f i g u r e 1 ). La vidéo est conseillée,
non seulement pour son intérêt didactique, mais aussi pour la commo-
dité des gestes, leur sécurité et la meilleure asepsie qu’elle pro-
cure, l’œil et la tête de l’opérateur étant loin du champ opératoire.
La thoracoscopie médicale doit être réalisée dans des conditions
d’asepsie draconiennes. La salle d’examen doit être stérilisée de
la même manière qu’un bloc opératoire. Les trocarts, les endo-
scopes, les pinces, les câbles de raccordement et tous les acces-
soires doivent être stérilisés après un nettoyage soigneux.
Technique
La thoracoscopie médicale est une technique invasive qui doit être
utilisée lorsque l’analyse cytologique du liquide pleural n’a pas été
contributive. En effet, le rendement des biopsies percutanées n’est
pas plus élevé, et ce geste technique est de plus en plus réservé aux
cas de forte suspicion de tuberculose pleurale. La thoracoscopie médi-
cale est très voisine de la technique de mise en place d’un drain tho-
racique au moyen d’un trocart, la différence étant que l’exploration
de la cavité pleurale est possible, ainsi que la réalisation de biopsies.
Anesthésie
Plusieurs modalités d’anesthésie sont possibles, basées sur l’expé-
rience des équipes, le plateau technique local, l’indication de
l’examen, et le choix du patient après information éclairée sur la
qualité de l’examen. Une prémédication est indispensable quelle
que soit la méthode d’anesthésie réalisée. L’anesthésie locale
(uniquement au niveau de l’incision) est recommandée pour un
examen rapide chez un patient qui présente une cavité pleurale
libre d’adhérences, chez les patients à haut risque en mauvais état
général, ou en cas d’insuffisance cardiorespiratoire contre-indi-
quant une anesthésie générale.
L’anesthésie générale est nécessaire dans certaines situations.
L’idéal est un patient sous anesthésie générale conservant une
respiration spontanée (sous intubation trachéale ou masque
l a r y n g é ) ; cela évite le retour du poumon à la paroi, qui gêne l’exa-
men, ainsi que la lourdeur d’une intubation sélective pour un geste
diagnostique le plus souvent anodin (2).
Déroulement de l’examen
L’examen est réalisé sur un patient en décubitus latéral sur son
côté sain. La porte d’entrée se situe au niveau de la ligne axillaire
moyenne entre les troisième et septième espaces intercostaux. Le
prérequis indispensable est la présence d’une cavité pleurale acces-
sible d’au moins 6 à 10 cm de diamètre.
Un pneumothorax artificiel est réalisé la veille de l’examen ou sur
la table de thoracoscopie, immédiatement avant l’examen, à l’aide
d’une aiguille de plèvre (2 à 3 mm de diamètre et 100 mm de
long) à double mandrin, l’un pointu pour traverser la peau et les
muscles intercostaux, l’autre mousse pour traverser le fascia endo-
thoracique et la plèvre pariétale sans léser le poumon. L’aiguille
est mise en place dans la cavité pleurale comme pour une simple
ponction pleurale, et le robinet assurant l’étanchéité est ouvert afin
de laisser l’air entrer de manière active (pas d’insufflation d’air
sans contrôle de la vue). Le bruit caractéristique de l’air entrant
dans la cavité pleurale est audible jusqu’à l’équilibre des pressions,
période pendant laquelle l’air entre et sort en fonction des mou-
vements expiratoires et inspiratoires du patient.
Le choix de la porte d’entrée dépend de l’indication de l’examen
et de la présence de brides éventuelles. Dans le cas d’un pneumo-
thorax, le troisième ou quatrième espace sera choisi (lésions pul-
monaires et pleurales le plus souvent apicales), alors que le cin-
quième, sixième ou septième espace sera préféré en cas de suspicion
de pleurésie néoplasique (lésions débutantes au niveau de la
plèvre pariétale inférieure et postérieure).
Le reste de l’examen comprend les étapes suivantes :
–aspiration soigneuse du liquide en cas de pleurésie, avec réali-
sation des prélèvements adéquats, à visée diagnostique ;
– section éventuelle de brides gênant l’exploration ;
–inspection de la cavité pleurale avec endoscope à vue directe
ou latérale. Des biopsies peuvent être réalisées à l’aide de la pince
porte-optique, en utilisant une seule porte d’entrée. Cette pince ne
permet pas la réalisation d’une coagulation. Dans l’idéal, quand
la plèvre pariétale est fine et présente un aspect inflammatoire
non spécifique, les prélèvements doivent être réalisés contre une
côte, afin d’éviter le paquet vasculo-nerveux intercostal.
Figure 1. À gauche (de haut en bas) : endoscope Panoview
®
(Richard Wolf, Knittlingen, Allemagne) de 7 mm à vision directe, endoscope court de 4 mm, pince
porte-optique, pince coagulante. À droite : trocart de 7 mm, trocart de 5 mm.
163
La Lettre du Pneumologue - Volume VII - n
o
4 - juillet-août 2004

À la fin de l’examen, une symphyse pleurale par talc dépourvu de
fibres d’amiante (Stéritalc
®
Novatech, France) et calibré peut être
réalisée en cas de pneumothorax ou de pleurésie récidivante. Un
drain thoracique est inséré en fin d’examen afin d’assurer sur la
table, en décubitus latéral, la réexpansion pulmonaire (3).
COMPLICATIONS ET CONTRE-INDICATIONS
Complications
L’ensemble des résultats concernant les complications de la thora-
coscopie, obtenus à partir des principales séries de la littérature, rap-
porte une mortalité inférieure à 0 , 0 1 %. Plusieurs litres de liquide
peuvent être complètement aspirés pendant cet examen, avec un
risque limité d’œdème du fait de l’équilibre des pressions permis
par l’entrée de l’air à travers le trocart dans l’espace pleural. Si la
réexpansion pulmonaire paraît difficile, une aspiration à faible pres-
sion négative doit être appliquée. La prise de pression intrapleurale
avant l’examen permet de prévoir cet inconvénient. La complica-
tion la plus sérieuse est l’embolie gazeuse après insufflation active
d’air dans la cavité pleurale, qui est cependant rare (< 0 , 1 %) et peut
être évitée en utilisant un insufflateur à double ballonnet.
Les complications d’une thoracoscopie médicale peuvent être
prévenues en observant les règles suivantes :
– suspendre l’examen si le patient a une toux difficilement
réductible,
–pendant l’examen, surveiller l’oxymétrie et l’ECG, oxygéner,
– éviter les biopsies près des scissures ou du médiastin,
– insérer un drain thoracique dans tous les cas.
Contre-indications
Elles sont rarement absolues. Le principal écueil est la taille de la
poche pleurale à explorer. Certains facteurs peuvent retarder la
réalisation de l’examen. Il s’agit de la toux, de l’hypoxémie, des
troubles de la crase sanguine (taux de prothrombine < 6 0 %e t / o u
plaquettes < 6 0 0 0 0 / m m
3
) et des anomalies cardiologiques. Le
pneumologue doit évaluer le rapport bénéfice-risque pour chaque
cas (4, 5).
Les contre-indications pour les biopsies pulmonaires sont l’hyper-
tension artérielle pulmonaire, un aspect du poumon en “rayons
de miel”, une suspicion d’anévrisme artério-veineux, le kyste hyda-
tique, les tumeurs très vascularisées.
APPLICATIONS CLINIQUES
La thoracoscopie médicale est avant tout un examen diagnos-
tique, mais elle peut également être utilisée dans le cadre de gestes
thérapeutiques.
Indications de base
Les pleurésies cancéreuses
Il s’agit de l’indication principale de la thoracoscopie médicale,
compte tenu du mauvais rendement diagnostique de l’analyse du
liquide pleural et des biopsies pleurales percutanées. En outre,
elle offre la possibilité d’évaluer le caractère disséminé ou loca-
lisé des lésions ainsi que l’atteinte de la plèvre viscérale et du
diaphragme, ce qui présente un intérêt pronostique dans certaines
situations et peut modifier la stratégie thérapeutique. Le rendement
se situe entre 90 et 100 %, comparé à une sensibilité d’environ
4 0 % pour la biopsie percutanée et de 60 % pour la cytologie
pleurale. Si le patient a un cancer connu et une cytologie pleurale
négative à la ponction, une thoracoscopie doit être préférée à une
biopsie pleurale percutanée.
Dans le cas de pleurésies néoplasiques récidivantes, une sym-
physe pleurale peut être réalisée dans le même temps. Après une
évacuation complète du liquide, l’insufflation douce de talc cali-
bré, stérile, sans fibres minérales, sous contrôle de la vue de toute
la surface pleurale, permet d’obtenir une symphyse dans plus de
9 0 % des cas lorsque la réexpansion complète du poumon est
obtenue. On note dans les suites une ascension thermique chez
30 % des patients et une durée moyenne d’hospitalisation de 4 à
5 jours. Cette méthode est actuellement considérée comme la
meilleure option dans le cadre du traitement palliatif des pleurésies
néoplasiques récidivantes (6). Les nouvelles stratégies de prise
en charge des pleurésies récidivantes, notamment ambulatoires
ou au lit du patient, doivent être comparées à cette technique (7).
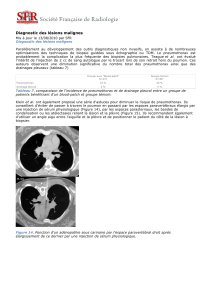
Pleurésies métastatiques
Les biopsies percutanées ne permettent pas le diagnostic des
nodules localisés au niveau du diaphragme, de la plèvre viscérale
et sur le médiastin. Le rendement diagnostique est en outre dépen-
dant de la dissémination de la tumeur dans la cavité pleurale
(figure 2). Le principal avantage de la thoracoscopie est de per-
mettre un diagnostic précoce et une évaluation complète de la
cavité pleurale. Dans 85 %des cas de cancer pleural, la thoraco-
scopie met en évidence un aspect macroscopique évocateur de
malignité. Cet aspect doit cependant être confirmé par l’analyse
histologique, qui est le seul critère diagnostique. Le seul écueil à
l’examen est la présence d’adhérences gênant la réalisation de la
pneumoséreuse.
Mésothéliome pleural malin
La thoracoscopie permet le choix des sites biopsiques, des pré-
lèvements multiples, et donc un rendement élevé. Les biopsies
sont positives dans plus de 98 % des cas, alors que la combinaison
de la cytologie du liquide pleural et de la biopsie percutanée donne
un diagnostic dans moins de 40 % des cas.
La thoracoscopie permet aussi d’apprécier le stade de la maladie,
qui est un paramètre pronostique important. Elle permet en outre
des prélèvements pulmonaires, afin de documenter une éventuelle
exposition à l’amiante (8).
Les pleurésies tuberculeuses
Dans 70 à 90 % des cas, le diagnostic peut être obtenu par biopsie
percutanée (dont c’est actuellement la seule indication) pour ana-
lyse histologique et culture. Un deuxième prélèvement permet un
rendement de 95 %. De fait, la thoracoscopie ne joue pas un rôle
important dans le diagnostic de cette maladie, et sa découverte est
le plus souvent fortuite. L’aspect en est le plus souvent celui de
granulations blanchâtres recouvrant la plèvre pariétale et dia-
phragmatique. Les lésions initiales perdent souvent leur spécifi-
cité macroscopique, mais également histologique lorsque l’exa-
men est réalisé tardivement. Les cultures de fragments sont
positives dans seulement 50 % des cas.
I
M A G E R I E
164
La Lettre du Pneumologue - Volume VII - n
o
4 - juillet-août 2004

Autres pleurésies
Les pleurésies associées à un cancer bronchopulmonaire peuvent
résulter d’un mécanisme direct, par envahissement de la plèvre, ou
être en rapport avec une cause indirecte ( 9 ) . Dans cette situation, la
thoracoscopie est préférable à la thoracotomie pour identifier les
patients susceptibles de bénéficier d’une résection chirurgicale.
Les pleurésies récidivantes d’étiologie bénigne sont le plus fré-
quemment retrouvées chez les patients insuffisants cardiaques,
dans les suites d’une chirurgie cardiaque, et dans les cas de syn-
drome néphrotique, de connectivites et d’autres maladies inflam-
matoires ( 1 0 ). La thoracoscopie est alors requise quand les symp-
tômes sont invalidants et qu’ils ne sont pas contrôlés par des
ponctions itératives. Habituellement, des prélèvements biopsiques
sont réalisés pour éliminer un problème infectieux ou néoplasique,
et pour réaliser une symphyse pleurale.
Le pneumothorax spontané
Des études récentes ont défini la place du drainage thoracique dans
les cas de pneumothorax spontané primaire (11, 12). Si un drain
doit être mis en place dans la cavité pleurale, il est simple, dans un
premier temps, d’introduire une optique pour examiner la cavité
pleurale et la surface du poumon. La thoracoscopie est une
alternative diagnostique, voire thérapeutique, excellente en cas de
drainages répétés, pour les patients présentant des pneumotho-
rax récidivants ou prolongés malgré le drainage (13). L’examen
peut mettre en évidence des brides pleurales plus ou moins sous
tension, des blebs, des bulles, ou, à l’inverse, montrer une surface
pulmonaire macroscopiquement normale. Aucune étude n’a actuel-
lement mis en évidence l’intérêt de réséquer des bulles ou des blebs
macroscopiquement sains, et seules les brèches visibles nécessitent
un geste curatif. Malgré la controverse concernant l’utilisation
du talc à faible dose (< 2 g) pour symphyse pleurale en situation de
récidive, plusieurs études cliniques sur de grandes cohortes et de
récents résultats expérimentaux vont dans le sens de l’innocuité
de cette technique (14, 15). Une étude comparant prise en charge
chirurgicale et talcage pleural par thoracoscopie mettrait fin à
cette controverse.
Pleurésies purulentes
La thoracoscopie est utile dans la prise en charge de l’empyème
à un stade précoce (16). Durant la phase exsudative et d’organi-
sation, l’examen endoscopique permet d’effondrer des adhérences
à ce stade fibreuses, et d’évacuer le liquide et les membranes fibrino-
purulentes par aspiration et à la pince afin de créer une cavité
pleurale unique ( f i g u r e 3 ) . Le drainage et l’irrigation pleurale sont
plus efficaces, ce qui raccourcit la durée d’hospitalisation et évite
une thoracotomie. Le moment de la réalisation de la thoracosco-
pie est crucial et, dans tous les cas, celle-ci doit être envisagée lorsque
la mise en place d’un drain thoracique est indiquée ( 1 7 ). Le rôle de
la thoracoscopie dans cette indication, au même titre que l’utilisa-
tion des fibrinolytiques, et du recours à la chirurgie est très contro-
versé, et des études prospectives comparatives sont nécessaires.
Syndrome vasomoteur des membres supérieurs
La section de la chaîne sympathique dorsale au niveau du plexus
(deuxième, troisième ± quatrième ganglions dorsaux) représ e n t e
le traitement le plus efficace de l’hyperhidrose axillo-palmaire. L a
sympathectomie par thoracoscopie peut être réalisée par
électrocoagulation, dissection ou excision. Entre les mains d’un
opérateur expérimenté, la diathermocoagulation du plexus sympa-
thique dorsal par thoracoscopie médicale est réalisable avec un
excellent résultat ( 1 8 ). Les effets secondaires et les complications
sont rares (hypersudation compensatrice, douleur).
CONCLUSION
Les indications de la thoracoscopie sont loin d’être exhaustives,
mais elle doit être réalisée par un pneumologue formé à cette
technique, c’est-à-dire connaissant l’anatomie endoscopique pleu-
rale, rompu à la mise en place correcte d’un drain thoracique et
ayant pratiqué un certain nombre d’examens sous contrôle d’un
opérateur expérimenté. Son intérêt est évident sur le plan du dia-
gnostic des pleurésies et elle doit rester du domaine médical strict.
Le recours au chirurgien dans cette indication repose uniquement
sur l’impossibilité d’accéder simplement à la cavité pleurale.
Figure 2. À gauche : métastase au niveau de la plèvre pariétale. Quelques nodules se répartissent sur la surface pleurale, qui, par ailleurs, est saine (la positi-
vité des biopsies percutanées à l’aiguille est le fruit du hasard). À droite : adénocarcinome pleural métastatique. Le cancer primitif n’a pas été retrouvé.
165
La Lettre du Pneumologue - Volume VII - n
o
4 - juillet-août 2004

I
M A G E R I E
166
La Lettre du Pneumologue - Volume VII - n
o
4 - juillet-août 2004
Concernant le pneumothorax, la thoracoscopie médicale reste “la
mise en place d’un drain sous le contrôle de la vue” lorsqu’un
drainage est nécessaire. Elle permet dans le même temps d’exa-
miner la surface du poumon, voire de mettre en évidence une brèche
macroscopique. La discussion du talcage pleural ne porte pas sur
la technique endoscopique en soi, mais bien sur la meilleure
option pour obtenir une symphyse pleurale lorsque celle-ci est
indiquée.
Les directions futures de la thoracoscopie vont dans le sens du déve-
loppement d’instruments de taille réduite permettant des actes peu
invasifs dans le cadre de fonctionnements ambulatoires, et de la
généralisation de cet examen en secteur pneumologique, qui doit
faire partie des techniques endoscopiques médicales (19).
R
É F É R E N C E S B I B L I O G R A P H I Q U E S
1 .
Loddenkemper R. Thoracoscopy – State of the art. Eur Respir J 1998;11:213-21.
2.
Plummer S, Hartley M, Vaughan RS. Anaesthesia for telescopic procedures
in the thorax. Br J Anaesth 1998;80:223-34.
3.
Boutin C, Astoul P. Diagnostic thoracoscopy. Clin Chest Med
1998;19(2):295-309.
4.
Colt HG. Thoracoscopy: a prospective study of safety and outcome. Chest
1995;108:324-9.
5.
Hansen M, Faurschou P, Clementsen P. Medical thoracoscopy, results and
complications in 146 patients: a retrospective study. Respir Med 1998;9:228-32.
6.
Astoul P. Pleurodesis for the therapy of malignant pleural effusions: inpa-
tient procedure. J Bronchol 2003;10:215-7.
7.
Sterman D, Kruklitis R, Lund M, Musani A. Pleurodesis for the therapy of
malignant pleural effusions: outpatient procedure. J Bronchol 2003;10:218-22.
8.
Boutin C, Frenay C, Astoul P. Endoscopic diagnosis of mesothelioma. Rev
Mal Respir 1999;16:1257-62.
9.
Sahn SA. Pleural diseases related to metastatic malignancies. Eur Respir J
1997;10:1907-13.
10.
Wilsher ML, Veale AG. Medical thoracoscopy in the diagnosis of unex-
plained pleural effusion. Respirology 1998;3:77-80.
1 1 .
Sahn SA, Heffner JE. Spontaneous pneumothorax. N Engl J Med 2000;342:
868-74.
12.
Baumann MH, Strange C, Heffner JE et al. Management of spontaneous
pneumothorax. An American College of Chest Physicians Delphi Consensus
statement. Chest 2001;119:590-602.
13.
Tschopp JM, Boutin C, Astoul P et al. Talcage by medical thoracoscopy
for primary spontaneous pneumothorax is more cost-effective than drainage: a
randomised study. Eur Respir J 2002;20:1003-9.
14.
Delaunois L, el Khawand C. Medical thoracoscopy in the management of
pneumothorax. Monaldi Arch Chest Dis 1998;53:148-50.
15.
Fraticelli A, Robaglia-Schlupp A, Riera H et al. Distribution of calibrated
talc after intrapleural administration. An experimental study in rats. Chest
2002;122:1737-41.
16.
Karmy-Jones R, Sorenson V, Horst HM et al. Rigid thoracoscopic debri-
dement and continuous pleural irrigation in the management of empyema.
Chest 1997;111:272-4.
17.
Cassina PC, Hauser M, Hillejan L et al. Video-assisted thoracoscopy in
the treatment of pleural empyema: stage-based management and outcome. J
Thorac Cardiovasc Surg 1999;117:234-8.
18.
Noppen M, Herregodts P, D’haese J, D’Haens J, Vincken W. A simplified
T2-T3 thoracoscopic sympatholysis technique for the treatment of essential
hyperhidrosis: short-term results in 100 patients. J Laparoendosc Surg 1996;
6:151-9.
19.
Tassi G, Marchetti G. Minithoracoscopy. A less invasive approach to tho-
racoscopy. Chest 2003;124:1975-7.
Figure 3. Pleurésie purulente cloisonnée. À terme, de telles adhérences rendent la ponction, voire le drainage, difficile. La thoracoscopie permet un
décloisonnement à la pince et l’obtention d’une cavité unique.
1
/
5
100%