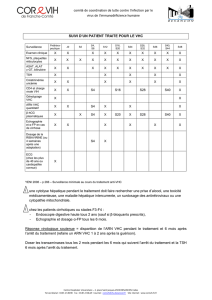
Examen des traitements pour les patients présentant un VHC

Examen des traitements pour les patients présentant un VHC
chronique de génotype 1
Contexte
Environ 250 000 Canadiens seraient infectés par le virus
de l’hépatite C (VHC); cependant, plusieurs autres
ignoreraient qu’ils sont infectés. Bien que 25 % des
personnes infectées se libèrent spontanément du VHC,
les autres personnes atteintes développeront une
infection chronique au VHC. On connait six génotypes
du VHC et la stratégie de traitement peut différer d’un
génotype à l’autre. Au Canada, les infections du
génotype 1 représentent de 55 % à 65 % des infections
au VHC.
Technologie
Pendant plusieurs années, le traitement standard pour
les patients présentant un VHC chronique de génotype 1
consistait en une combinaison d’interféron pégylé et de
ribavirin. Cependant, les médicaments antiviraux à action
directe que sont le télaprévir, le boceprévir, le siméprévir,
et le sofosbuvir ont récemment été conçus pour traiter le
VHC, en association avec la combinaison interféron pégylé
et ribavirine. Tous ces médicaments sont autorisés pour le
traitement des infections de génotype 1, à l’exception du
sofosbuvir, qui est pour sa part autorisé pour le traitement
du VHC chronique de plusieurs génotypes. Le daclatasvir,
un autre médicament antiviral à action directe, n’a pas
encore été mis sur le marché au Canada.
Sujet
Un examen des lignes directrices internationales basées
sur des données probantes dans le traitement de patients
présentant une infection au VHC chronique de génotype 1
éclairera les prises de décisions dans le traitement de ces
patients.
Méthode
On a procédé à une recherche documentaire limitée à
partir des ressources clés et examiné les titres et
résumés des publications repérées. On a ensuite évalué
le texte intégral des publications en vue de procéder au
choix final des articles selon des critères de sélection
déterminés au préalable.
Résultats
La recherche documentaire a permis de relever 155
références, auxquelles s’ajoutent 4 ensembles de lignes
directrices tirées d’autres sources. Après examen des
résumés, 5 ensembles de lignes directrices répondaient
aux critères de sélection de l’examen.
Messages clés
Les lignes directrices internationales sur le
traitement des patients présentant une infection au
VHC chronique de génotype 1 recommandent une
combinaison de :
siméprévir ou de sofosbuvir associé à la
combinaison interféron pégylé et ribavirine;
siméprévir ou de sofosbuvir avec de la
ribavirine (pour les patients ne pouvant utiliser
l’interféron)*
siméprévir et de sofosbuvir*
ou
daclatasvir et d’interféron pégylé associé à la
ribavirine ou au sofosbuvir.
Ces recommandations sont appelées à changer
lorsque de nouveaux agents seront offerts.
*Ces traitements ne sont pas encore autorisés au Canada.
AVERTISSEMENT : L’information contenue dans ce Rapport en bref vise à aider les décideurs des soins de la santé, les patients, les professionnels de la
santé, les dirigeants des systèmes de santé et les décideurs politiques à prendre des décisions éclairées et ainsi améliorer la qualité des services de santé.
L’information contenue dans ce Rapport en bref ne doit pas être utilisée comme substitut à l’application d’un jugement clinique en ce qui concerne les soins
d’un patient ou autre jugement professionnel dans tout processus décisionnel ni n’est-elle destinée à remplacer un avis médical professionnel. Bien que
l’ACMTS ait tout mis en œuvre pour veiller à l’exactitude, à l’exhaustivité et à l’actualité du présent rapport, elle décline toute responsabilité à cet égard,
comme elle ne saurait être tenue responsable des erreurs, omissions, blessures, pertes ou dommages découlant de l’usage (ou du mauvais usage) de
l’information contenue ou implicite dans le présent Rapport en bref.
L’ACMTS assume l’entière responsabilité de la forme finale et du contenu de ce Rapport en bref. Les déclarations, conclusions et opinions qui y sont
exprimées ne reflètent pas nécessairement le point de vue de Santé Canada ou des gouvernements provinciaux et territoriaux. La production de ce Rapport
en bref a été rendue possible grâce à une contribution financière de Santé Canada.
Juillet 2014
RC0562
1
/
1
100%