Réactivité des carbonyles C=O

Chapitre 10 :
Réactivité des carbonyles C=O
Christel ROUTABOUL
Docteur en Chimie
Chimie - Chimie organique
MED@TICE PCEM1 - Année 2006/2007
Faculté de Médecine de Grenoble - Tous droits réservés.

1 – Addition nucléophile
2 – Substitution nucléophile
δ+
δ−
CO
Y
R
R = chaîne carbonée
Si Y = chaîne carbonée
⇒cétone / aldéhyde
Si Y = groupement électroattracteur
⇒acide carboxylique ou dérivé
Nu

1 – Additions
nucléophiles

OOHCN
Na+CN
−
H2O
R1
R2
R1
R2
COCN
R1
R2
H2O
a) Addition d’ion cyanure CN
−
N
ONa+CN−
H2ON
CN
OH agoniste
de 5HT3
Équation – bilan :
Mécanisme :
Exemple :
Réaction acide-base
(Prototropie)
cyanhydrines
hydroxyde
nitrile
ou cyano
acide
base
δ+δ−
CN CO
R1
R2
COHCN
R1
R2
1.1 – Formation des dérivés

CR1
O
R2
BH
H
H
H
χ(B) < χ(H)
⇒bases très fortes (réactions violentes avec les acides)
⇒pas bon nucléophiles
Réaction acide-base
avec le solvant
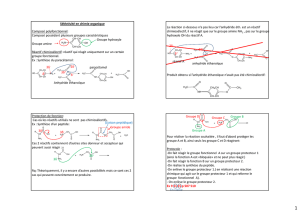
b) Addition d’ions hydrure H
−
NaH (hydrure de sodium)
LiH (hydrure de lithium) ⇒Na+H−
⇒Li+ H−
NaBH4(borohydrure de sodium) ⇒Na+BH4−⇒bon nucléophile
B
H
H
H
CR1
OH
R2H
CR1
O
R2H
acide
de Lewis
base
CH3OH
acide
NaBH4/ méthanol (CH3OH) ?Réaction
de
réduction
(+II) (0)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%