– UE :IV – L'eau 2016-2017

2016-2017 Voie d'accès aux substances médicamenteuses
Chimie inorganique
– UE :IV – L'eau
Pas d'annexe
Semaine : n°8 (du 24/10/16 au
28/10/16)
Date : 26/10/2016
Heure : de 8h00 à
9h00 Professeur : Pr. Deprez
Binôme : n°21 Correcteur : 13
Remarques du professeur
PLAN DU COURS
1/6
IV) L'EAU (SUITE)
E) Effet hydrophobe
1) Conclusion de l'expérience avec les particules de talc
2) Effet hydrophobe et stabilité des protéines
F) Propriétés colligatives
G) Protéines AFP
1) Structure des protéines AFP
2) Effet kelvin
H) Aquaporines
1) Les AA impliqués
2) Le passage contrôlé de l'eau
3) Mécanisme de Grotthus (conductivité molaire)
I) Antagoniste sélectif de V2

2016-2017 Voie d'accès aux substances médicamenteuses
E) Effet hydrophobe
1) Conclusion de l'expérience avec les particules de talc
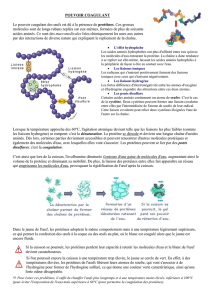
✔ Effet hydrophobe (expérience précédente): on introduit un petit volume de molécules amphiphiles à la surface
de l’eau, elle diffusent à la surface. En diffusant elles repoussent les molécules de talc.
✔La diffusion est liée à l’augmentation de l’entropie lors de la diffusion, qui est liée au fait que la molécule
diffuse et qu’une partie de la surface liquide exposée à l’air a été réduite.
✔Cet effet hydrophobe déstabilise l'interface entre l’eau et une phase incapable de faire des liaisons : c’est un effet
hydrophobe où il y a très peu de molécules échangées.
Exemple: Butane
La réorganisation entraine une diminution de l’entropie néfaste pour la réalisation de la dissolution.
Exemple : structure hydrophobe
Perdre le moins de structures entre elles, l’entropie baisse de manière proportionnelle à cette surface.
L’effet hydrophobe est proportionnel à la surface de la molécule qui ne peut pas établir de liaisons avec
l’eau. Il est facile à modéliser.
Toute molécule flexible va chercher à adopter une conformation dans laquelle la surface hydrophobe sera plus
faible : hydrophobic collapse (effet hydrophobe= stabilité des protéines)
2) Effet hydrophobe et stabilité des protéines
Si on a une molécule à fragments polypeptidiques avec des AA polaires (chaines latérales capables de faire des
liaisons H avec l’eau) et par ailleurs des AA hydrophobes ou apolaires, spontanément, la chaine polypeptidique
lorsqu’elle sera dans l’eau va voir sa conformation évoluer de manière à cacher les AA incapables de faire des
liaisons H avec l’eau (donc les AA apolaires) et exposer ses AA polaires.
Cependant la surface hydrophobe diminue et l’entropie augmente, c’est la force principale qui concoure à
l’établissement d’une structure tertiaire dans les protéines.
La préservation de cette surface hydrophobe minimale est garante de la stabilité thermique des protéines.
2/6

2016-2017 Voie d'accès aux substances médicamenteuses
F) Propriétés colligatives:
Propriétés exclusives des solutions, qui dépendent de la concentration en soluté et non de sa nature.
= propriété d’une collection.
Exemples: Variations de température de changement d’état. En effet on sait que l’eau pure congèle à 0°C et bout
à 100°C dans les conditions de pression habituelles.
Si on prend une solution aqueuse, quelque soit le soluté dissout, les températures seront différentes (fusion
diminue et ébullition augmente).
Modification de l’équilibre vaporisation/condensation:
L’équilibre sera lié aux forces intermoléculaires dans le solvant (liaisons H dans l’eau) mais aussi à la surface
disponible aux molécules pour passer à la phase gaz.
Si dans la solution on a des solutés qui masquent la surface, la température d’ébullition va augmenter.
Si on a une phase solide, les ions en solution vont diminuer l’échange entre le cristal et la solution, la température
de fusion diminuera (eau de mer congèle à -0°C).
→ Variation de la température d’ébullition : constante ébulloscopique
→ Variation de la température de fusion : constante gyroscopique
Constantes pour l’eau : exemple du caramel plus on met de sucre plus la température d’ébullition augmente.
G) Les protéines AFP
AntiFreezeProteins: on les retrouve dans les organismes vivants exposés à des faibles températures pendant leur
cycle de vie.
Exemple:
- Les poissons et microorganismes des zones polaires, présentent des protéines qui vont diminuer le point de
congélation de l’eau.
- Insectes : synthétisent des protéines en hélice ß qui retardent la congélation de l’eau.
Ces protéines sont intéressantes pour conserver des échantillons biologiques.
Exemple (hélice ß) :
•Protéine avec une structure extrêmement bien définie dans l’espace (beaucoup mieux que la moyenne).
3/6

2016-2017 Voie d'accès aux substances médicamenteuses
1) Structure des protéines AFP
•Sur une face de l’hélice on a établissement d’un feuillet ß (flèches vertes) à chaque extrémité on a des AA qui
portent une fonction alcool (capables de réaliser des liaisons hydrogène) qui sont des thréonines.
•Présentes à intervalle régulier (1.4 Angström exactement) entre chaque fonction alcool.
Les molécules d’eau se répartissent de manière extrêmement régulière.
On comprend comment la protéine AFP se colle à la surface du cristal d’eau.
•Géométrie sur le cristal de glace : on voit que l'angle formé par 3 atomes d'oxygènes de 3 molécules d'eau
fait exactement 109°, la distance entre 2 atomes d'oxygène dans l'eau est de 2,76 angstrom, et la distance
entre 2 atomes d'oxygène en surface du cristal va être de 2,76 x 2sin (alpha/2) = 4,5 angström. Ces 4,5
angstrom nous rappellent la distance entre 2 fonctions thréonines (à peut près 4,6 angstrom). Donc à 0,1
angstrom près les atomes d'oxygène des fonctions OH de la protéine antigène sont exactement en face des
atomes d'oxygène qui sont à la surface du cristal et donc capables de faire des liaisons hydrogènes.
Donc la molécule antigène va venir faire un nombre de liaison hydrogène très important, donc une fois qu'elle est
fixée, il est très difficile de la décoller du cristal. C'est un établissement de liaisons hydrogènes qui sont
coopératives.
Donc la protéine antigène se colle au cristal et ne peut plus se décoller.
Une partie de la surface du cristal sera masquée à l'eau du solvant, donc ces protéines antigènes ne vont pas
empêcher le démarrage du processus de cristallisation mais elles vont empêcher la croissance des cristaux.
2) Effet Kelvin: énergie libre = f(1/r)
Les protéines AFP empêchent la croissance des cristaux, à une température inférieure à la température de fusion,
des microcristaux se créent mais ils seront empêchés de croitre grâce à la présence de ces molécules AFP à la
surface.
Physiquement, on ne sera pas obligés de couvrir la surface du cristal en croissance avec ces protéines pour en
empêcher la croissance : car quand on regarde l'énergie libre d'un cristal en croissance, si on a bloqué le processus
de cristalisation à l'endroit où on a mis les protéines AFP, on va voir que le cristal va croitre entre 2 protéines AFP
et il va se créer une courbure de la surface du cristal. Et Kelvin a montré que l'énergie libre du système est fonction
de l'inverse du rayon de courbure.
Donc le rayon de courbure est inversement proportionnel à l’énergie libre.
Quand c'est plat, le rayon de courbure est infini : énergie libre à son minima
Dès que le cristal commence à croitre en faisant des bosses entre 2 protéines AFP : le rayon de courbure va
diminuer : l'énergie libre va augmenter : ce qui est thermodynamiquement défavorable.
H) Aquaporine AQP1
Elles sont capables de faire passer l’eau à travers les membranes des cellules : ce sont des pores à eau, elles font
passer l’eau de manière passive à travers les membranes des cellules.
•10 gènes dans notre génome qui codent pour ces AQP.
•Elles régulent les flux d’eau au niveau de l’intestin, du rein et de la peau (glandes sudoripares).
•Lorsqu’il y a un changement d’environnement par rapport à l’intérieur de l’organisme, quand on veut passer une
membrane, il faut que l’eau puisse passer par les protéines des pores, elles ont évolué pour ne laisser passer que
les molécules d’eau (pas les ions).
Même si on garde un gradient de pH de part et d’autre de la membrane (pH différent mais les molécules
passent quand même la membrane).
1) Les AA impliqués
La plupart des AA de l’intérieur de la membrane sont hydrophobes donc incapables de réaliser des liaisons H
4/6

2016-2017 Voie d'accès aux substances médicamenteuses
avec néanmoins 2 AA qui sont hydrophiles, les asparagines, au milieu du pore.
On trouve 2 asparagine au milieu du pore de l’aquaporine hydrophobe. L’asparagine peut donc faire des liaisons
hydrogènes primaires.
2) Le passage controlé de l’eau
•Au niveau de l’aquaporine: on a des molécules d’eau qui passent en file indienne dans le pore une par une
en gardant 2 liaisons hydrogènes (une avec la molécule qui précède et une aves celle de derrière).
•Atome d’O de l’asparagine et le NH2: formation d’une liaison H
•L’aquaporine fait passer les molécules en file indienne et interrompt la chaine de liaisons hydrogène au
milieu du pore. Le sens de circulation est uniquement dépendant de la concentration de la différence de
pression osmotique des deux cotés de la membrane (phénomène symétrique et réversible).
La molécule d’eau se positionne impeccablement au milieu de la chaine hydrogène.
•Dans les hélices alpha, les dipôles carbonyles s’additionnent les uns entre les autres de manière anti-
parallèle pour former un autre gros dipôle qui forme un champ électrique intense à l’endroit où les têtes
des hélices alpha se rejoignent.
•2 asparagine font des liaisons H avec les molécules d’eau et les hélices alpha les orientent pour qu’elles se
fassent sans barrière d’énergie.
Pourquoi la chaine est-elle rompue au milieu du pore ?
Parce que les aquaporines doivent faciliter le passage de l’eau sans aucune barrière mais ça doit se faire en gardant
potentiellement un gradient de pH entre les 2 faces de la membrane. (exemple: mitochondries, pH différents,
gradient de 6 unités de pH)
3) Mécanisme de Grotthus (conductivité molaire)
Le Na+ a une conductivité 7 fois plus faible que H30+ alors que la force exercée est la même.
Pourquoi H30+ circule 7 fois plus vite que les charges Na+?
Cela s’explique par le mécanisme suivant de déplacement des charges positives dans une eau qui contient des ions
H30+
Chaine hypothétique de molécules d’eau avec des chaines liées. Si on a un champ électrique, la charge va bouger
mais l’ion ne va pas physiquement bouger, les liaisons H vont faire comme un fil électrique et ce sont les électrons
qui vont bouger. Les centres de masse ne vont pas bouger mais grâce aux LH les ions vont bouger (leurs
électrons).
Au final, on aura le déplacement de la charge électrique très rapide sans changement des centres de masse des
molécules d’eau.
A l’inverse d’un ion Na+ qui doit bouger physiquement, les protons seront plus intéressants car il n’y a pas de
mouvement.
Pour que le proton se déplace il faut une chaine de LH ininterrompue. Si dans l’aquaporine grâce à l’asparagine on
peut empêcher les LH, on empêche le passage des protons. On peut garder un gradient de pH entre les aquaporines
et les molécules d’eau.
5/6
 6
6
1
/
6
100%