CAS CLINIQUE Mots-clés :

CAS CLINIQUE
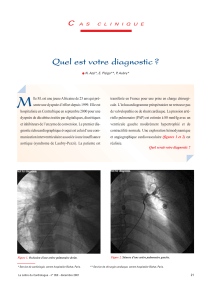
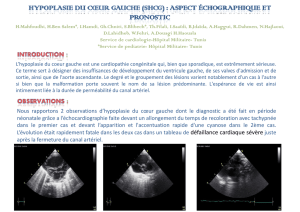
Figure 1. Scanner de l’aorte thoracique et abdominale.
A : calcifications de l’aorte ascendante et sténose supravalvulaire aortique.
B : incrustation calcaire avec sténose serrée de l’ostium coronaire gauche.
C : reconstruction tridimensionnelle surfacique.
Noter les calcifications étendues de l’aorte ascendante, l’occlusion des troncs
supra-aortiques, l’oblitération de l’aorte abdominale sous-rénale et de l’axe
iliaque droit avec perméabilité des artères fémorales profondes.
36 | La Lettre du Cardiologue • n° 458 - octobre 2012
Mots-clés :
Maladie de Takayasu – Sténose aortique supravalvulaire – Insuffisance aortique – Sténose coronaire ostiale – Syndrome de Leriche.
Keywords:
Takayasu’s disease – Supravalvular aortic stenosis – Aortic regurgitation – Coronary ostia stenosis – Leriche’s syndrome.
Aortite de Takayasu avec sténose
supravalvulaire engainant les ostia
coronaires, insuffisance valvulaire
et syndrome de Leriche
Takayasu’s aortitis with supravalular stenosis, coronary ostia embedding,
valve insufficiency and Leriche’s syndrome
C. Bouthors¹, I. El Hajjaji², R. Boutekadjirt³, P. Fouret⁴, F. Koskas², C. Acar¹
¹ Service de chirurgie cardiaque, hôpital de la Pitié-Salpêtrière, AP-HP, Paris.
² Service de chirurgie vasculaire, hôpital de la Pitié-Salpêtrière, AP-HP, Paris.
³ Service de radiologie, hôpital de la Pitié-Salpêtrière, AP-HP, Paris.
⁴ Service d'anatomopathologie, hôpital de la Pitié-Salpêtrière, AP-HP, Paris.
U
n homme, âgé de 45 ans et d’origine antillaise, est
atteint de la maladie de Takayasu. Il a été hospitalisé
pour la prise en charge chirurgicale d’une occlusion des
3 troncs supra-aortiques. Le patient était asymptomatique,
hormis une comitialité occasionnelle, mais il présentait au
scanner une séquelle d’un accident vasculaire cérébral dans
le territoire frontal.
Observation
Du fait de la présence de calcifications pariétales massives, la
revascularisation de l’hémicorps supérieur initialement prévue
à partir de l’aorte ascendante a été réalisée à partir de l’aorte
abdominale dans sa portion cœliaque qui était indemne. Malgré
plusieurs tentatives de reprise chirurgicale, le pontage sur les
troncs supra-aortiques a été le siège de thromboses itératives.
La vascularisation de l’encéphale reposait exclusivement sur
une artère vertébrale alimentée par une riche collatéralité
issue de l’artère sous-clavière gauche en aval de l’occlusion.
Le patient était asymptomatique sur le plan neurologique, et
un nouveau geste chirurgical n’a pas été tenté. Un traitement
médicamenteux comportant des corticoïdes à long terme et
du méthotrexate a été instauré.
Huit années plus tard, le patient a été réhospitalisé pour une claudi-
cation intermittente unilatérale qui a nécessité un pontage fémoro-
fémoral. En raison d’une élévation anormale du taux de troponine

CAS CLINIQUE
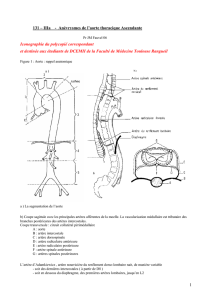
Figure 2.
Pièce opératoire.
A : résection monobloc
comprenant les valvules
aortiques, l’origine des
ostia coronaires (non
visibles) et l’ensemble
de l’aorte ascendante.
B : sténose supraval-
vulaire : à gauche, les
valvules épaissies et
rétractées (insuffisance
valvulaire) sont en place ;
à droite, même vue après
l’ablation des valvules.
Noter le rétrécissement
supravalvulaire induit par
la protrusion exubérante
des calcifications parié-
tales.
C : aortite de Takayasu
avec calcifications parié-
tales massives alternant
avec des plages d’ulcéra-
tions. L’origine des ostia
coronaires n’est plus
identifiable.
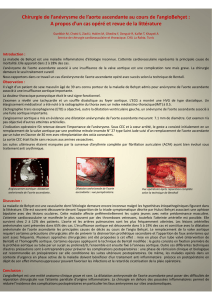
Figure 3. Scanner postopératoire de contrôle.
A : reconstruction tridimensionnelle surfacique. Aspect satisfaisant de
l’intervention de Bentall et perméabilité du pontage aortobifémoral depuis
l’aorte ascendante.
B : intervention de Bentall avec prothèse de Saint-Jude (en gris) incluse dans
un tube en Dacron® (en jaune). Noter le tube prothétique intermédiaire (en
bleu) sur le tronc commun et la translocation avec anastomose directe de
l’artère coronaire droite. Un deuxième tube en Dacron® (en jaune) destiné à
la revascularisation des membres inférieurs est anastomosé au tube rempla-
çant l’aorte ascendante.
C : projection d’intensité maximale. Noter l’émergence des artères coronaires
: à l’opposé de l’ostium gauche, qui est en position anatomique, l’artère coro-
naire droite a été repositionnée sur le flanc droit du tube prothétique aortique.
D : reconstruction tridimensionnelle surfacique. Reconstruction du tronc
coronaire gauche à l’aide d’un court tube prothétique (T) de Gore-Tex® anas-
tomosé au tube aortique.
La Lettre du Cardiologue • n° 458 - octobre 2012 | 37
dans la période postopératoire, une coronarographie a été réalisée.
Celle-ci a retrouvé une sténose serrée du tronc coronaire gauche
proximal qui a été traitée par la mise en place d’une endo prothèse
active.
Trois années ont passé et le patient a de nouveau été admis
pour un œdème aigu du poumon. On notait par ailleurs une
récidive de la claudication intermittente, affectant cette fois les
2 membres inférieurs dans le cadre d’un syndrome de Leriche. Le
patient se plaignait également de l’apparition d’une impuissance
sexuelle. L’échographie cardiaque a révélé l’existence d’une insuf-
fisance valvulaire aortique volumineuse dont le mécanisme était
une rétraction et un épaississement des valvules. Le ventricule
gauche était notablement hypertrophié et la fraction d’éjec-
tion était abaissée à 35 %. En l’absence d’accès vasculaire, une
nouvelle coronarographie n’était plus possible et un angioscanner
de l’ensemble de l’aorte thoracique et abdominale et de ses
branches a été effectué. L’aorte ascendante était entièrement
calcifiée et présentait un rétrécissement prononcé au niveau de la
jonction sinotubulaire (diamètre : 12 mm) [figure 1A]. Les calci-
fications pariétales étaient responsables de sténoses coronaires
serrées aux dépens des ostia droit et gauche en dépit du stent
(figure 1B et 1C). Plus en aval, le réseau coronaire distal était
intact. Le scanner a également révélé l’existence d’une oblité-
ration complète de l’aorte abdominale sous-rénale étendue à
l’axe iliaque d’un côté, associée à une thrombose des 2 artères
fémorales superficielles (figure 1).
Un traitement chirurgical en 1 temps des différentes oblité-
rations artérielles thoraciques et abdominales a été planifié.
L’anesthésie a été monitorée à partir de la pression systémique
radiale gauche. Bien que moins pulsée, celle-ci reflétait assez
fidèlement la pression aortique moyenne mesurée par ponction
directe pendant l’opération. Le débit cardiaque a été mesuré à
l’aide d’une sonde de Swan-Ganz à débit continu. Le traitement
chirurgical a été effectué par reprise de la sternotomie avec abord
des artères fémorales communes au triangle de Scarpa. La circu-
lation extracorporelle a été instituée entre l’oreillette droite et la
crosse aortique qui était indemne de calcification. En raison de
l’importance des calcifications pariétales de l’aorte ascendante, la
protection du myocarde par canulation sélective des ostia coro-
naires nous a semblé hasardeuse. Le cœur a donc été arrêté par
injection de cardioplégie par voie rétrograde après la canulation
du sinus coronaire. L’aorte a été sectionnée au niveau de la voie
d’éjection au-dessous des valvules aortiques et l’ensemble de
l’aorte ascendante, comprenant la valve aortique et la portion
initiale des artères coronaires, a été réséqué en bloc (figure 2).
Un remplacement de la valve aortique et de l’aorte ascendante
a été effectué selon la méthode de Bentall à l’aide une prothèse
valvulaire mécanique Saint-Jude de 25 mm de diamètre incluse
dans un tube prothétique en Dacron® de 28 mm de diamètre
(figure 3A et 3B). Le tronc coronaire gauche a été réimplanté
par l’intermédiaire d’un court segment de tube prothétique en
Gore-Tex® de 6 mm de diamètre selon une modification de la
technique de Cabrol (figure 3). L’artère coronaire droite a été
mobilisée sur plusieurs centimètres avec section de la branche
du cônus, ce qui a permis une réimplantation directe sur le tube
prothétique aortique (figure 3A, 3C et 3D).

CAS CLINIQUE
38 | La Lettre du Cardiologue • n° 458 - octobre 2012
Un pontage aorto-bifémoral a alors été réalisé à partir de l’aorte
ascendante au moyen d’un deuxième tube en Dacron® de 25 mm
de diamètre. Celui-ci a été acheminé au niveau de l’abdomen
selon un trajet rétromusculaire pararectal gauche et prépéritonéal
jusqu’à une troisième prothèse de Dacron® dont les extrémités
ont été anastomosées aux artères fémorales profondes (figure 3).
L’examen anatomopathologique a confirmé la sévérité de l’atteinte
pariétale de l’aorte ascendante avec la présence de calcifications
massives au voisinage de portions ulcérées (figure 2). L’examen
microscopique a retrouvé une hyperplasie intimale avec disparition
de la média, remplacée par un intense remaniement fibrocalcaire
dépourvu de cellules spécifiques.
Les suites opératoires ont été marquées par une durée prolongée
de ventilation assistée en raison d’une pneumopathie. Le contrôle
par angioscanner au premier mois a confirmé l’absence d’anomalie
du montage réalisé sur l’aorte ascendante et la perméabilité du
pontage aorto-bifémoral (figure 3). Le patient a quitté l’hôpital
après le délai habituel, les signes d’ischémie des membres infé-
rieurs ayant disparu. L’échographie cardiaque a confirmé le fonc-
tionnement normal de la prothèse valvulaire alors que la fraction
d’éjection était mesurée à 40 %.
Discussion
Les patients atteints de la maladie de Takayasu font habituellement
l’objet de multiples interventions de revascularisation, le risque de
complication artérielle postopératoire étant notoirement élevé (1).
L’atteinte de la valve aortique au cours de la maladie de Takayasu
a été documentée depuis longtemps (2, 3). Dans le cas décrit
ci-dessus, il existait en outre une aorte ascendante porcelaine et, de
façon plus inhabituelle, la protrusion de calcifications exubérantes
était responsable d’un aspect de sténose supravalvulaire au niveau
de la jonction sinotubulaire (figure 1). La saillie des calcifications
masquait l’émergence des artères coronaires dont les ostia étaient
sévèrement rétrécis (figure 1), une localisation classique de la
maladie coronaire en cas d’aortite de Takayasu (4, 5). Il existait
une altération de la fonction ventriculaire gauche systolique asso-
ciée à une hypertrophie myocardique notable, et on connaît le
pronostic péjoratif de ces anomalies échographiques au cours de la
maladie de Takayasu (6). Les valvules aortiques étaient rétractées
et fibreuses (figure 2) et une intervention conservatrice telle que
certains ont pu la réaliser lorsque le mécanisme de la fuite était lié
à une ectasie de l’aorte ascendante n’était pas envisageable (7). Un
remplacement de l’ensemble de la valve et de l’aorte ascendante
a donc été réalisé (intervention de Bentall). La portion initiale
du tronc coronaire gauche a été excisée et celui-ci a été réim-
planté par l’intermédiaire d’un court segment de tube prothétique
(technique de Cabrol modifiée) [figure 3]. Après l'excision de son
premier centimètre, l’artère coronaire droite a été mobilisée et
réimplantée directement sur la face antérodroite du tube aortique.
Certains ont proposé des méthodes alternatives pour traiter les
sténoses coronaires ostiales liées à une maladie de Takayasu :
endartériectomie avec ou sans patch d’élargissement (8, 9), ou
encore pontages aortocoronaires avec des greffons veineux, car
l’artère mammaire interne est souvent inutilisable (10, 11). Dans
le cas de notre patient, l’ancienneté et la sévérité des calcifica-
tions pariétales aortiques, alors que le réseau coronaire d’aval
était indemne, nous ont conduits à préférer une revascularisation
coronaire directe. Il a enfin été possible de traiter le syndrome
de Leriche par un pontage entre l’aorte ascendante et les artères
fémorales profondes (12) [figure 3]. ■
1. Saadoun D, Lambert M, Mirault T et al. Retrospective
analysis of surgery versus endovascular intervention in
Takayasu arteritis: a multicenter experience. Circulation
2012;125:813-9.
2. Dubourg O, Thomas D, Sirinelli A et al. Insuffisance
aortique dans la maladie de Takayasu : à propos de 3 cas
opérés et revue de la littérature. Arch Mal Cœur Vaiss 1984;
77:998-1005.
3. Matsuura K, Ogino H, Kobayashi J et al. Surgical treat-
ment of aortic regurgitation due to Takayasu arteritis:
long-term morbidity and mortality. Circulation 2005;112:
3707-12.
4. Amano J, Suzuki A. Coronary artery involvement in Takaya-
su’s arteritis. Collective review and guideline for surgical
treatment. J Thorac Cardiovasc Surg 1991;102:554-60.
5. Endo M, Tomizawa Y, Nishida H et al. Angiographic
findings and surgical treatments of coronary artery invol-
vement in Takayasu arteritis. J Thorac Cardiovasc Surg 2003;
125:570-7.
6. Soto ME, Espinola-Zavaleta N, Ramirez-Quito O,
Reyes PA. Echocardiographic follow-up of patients with
Takayasu’s arteritis: five-year survival. Echocardiography
2006;23:353-60.
7. Adachi O, Saiki Y, Akasaka J, Oda K, Iguchi A, Tabayashi K.
Surgical management of aortic regurgitation associated with
Takayasu arteritis and other forms of aortitis. Ann Thorac
Surg 2007;84:1950-3.
8. Matteucci ML, Iascone M, Gamba A et al. Left main stem
patch plasty and aortic root homograft in Takayasu’s disease.
Ann Thorac Surg 2004;77:314-7.
9. Nakano S, Shimazaki Y, Kaneko M et al. Transaortic
patch angioplasty for left coronary ostial stenosis in a
patient with Takayasu’s aortitis. Ann Thorac Surg 1992;53:
694-6.
10. Bottio T, Cardaioli P, Ossi E, Casarotto D, Thiene G,
Basso C. Left main trunk ostial stenosis and aortic incom-
petence in Takayasu’s arteritis. Cardiovasc Pathol 2002;11:
291-5.
11. Kazui T, Mitsunaga Y, Nakajima T, Okabayashi H.
Bentall operation with saphenous vein graft for a Takaya-
su’s aortitis patient. Ann Thorac Cardiovasc Surg 2010;16:
373-5.
12. Ahn H, Hwang HY. Ascending aorta-abdominal aorta
bypass for Takayasu’s arteritis. Asian Cardiovasc Thorac Ann
2003;11:357-8.
Références bibliographiques
1
/
3
100%