Lire l`article complet

La Lettre du Cardiologue - n° 326 - mars 2000
17
OBSERVATION
M.L., 73 ans, hypertendu, hypercholestérolémique, non diabé-
tique, est hospitalisé pour dyspnée paroxystique nocturne.
Ce patient, aux antécédents familiaux de dissection aortique,
avait été opéré en urgence en 1994 d’une dissection de l’aorte
ascendante dont la porte d’entrée était située à la face antéro-
gauche de l’aorte, en regard du tronc artériel brachio-cépha-
lique, et qui se prolongeait jusqu’à l’ostium de la coronaire
droite, sans que celle-ci soit disséquée. L’opération avait alors
consisté en une résection sus-coronaire de la partie disséquée,
transection complète de l’aorte, interposition d’un tube en
Dacron de 24 mm.
M.L. était asymptomatique jusqu’en mai 1999. La pression arté-
rielle était contrôlée sous inhibiteurs calciques. Les contrôles
échographiques bi-annuels étaient satisfaisants. Les électrocar-
diogrammes (ECG) étaient normaux.
En mai 1999, le patient présente plusieurs épisodes de dyspnée
nocturne, sans angor. La pression artérielle est à 110/70 mmHg,
la fréquence cardiaque à 80/mn, un souffle d’insuffisance aor-
tique est apparu, le reste de l’examen cardiovasculaire est nor-
mal.
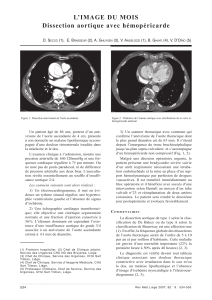
L’ECG inscrit un rythme sinusal régulier avec une onde Q de
nécrose en territoires antéro-septo-apical et inférieur (figure 1).
Les enzymes cardiaques sont normales.
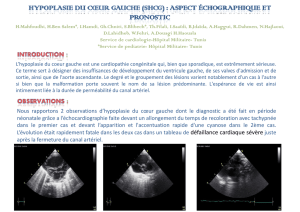
L’échographie cardiaque montre une hypokaliémie latérale et
postérieure, une akinésie apicale, une insuffisance aortique modé-
rée et un faux anévrysme de 3 cm de la paroi postérieure de l’aorte
(figure 2).
CAS CLINIQUE
Ischémie myocardique silencieuse
après chirurgie de l’aorte ascendante
●R. Dumaine*, C. Le Feuvre*, G. Helft*, A. Pavie**, J.P. Metzger*, A. Vacheron*
*Clinique cardiologique, hôpital Necker, Paris.
** Service de chirurgie cardiaque, hôpital Pitié-Salpêtrière, Paris.
Figure 1. Électrocardiogramme de mai 1999 : séquelles d’infarctus antéro-septo-apical et inférieur.

La scintigraphie au thallium 201 après épreuve d’effort met en
évidence une ischémie myocardique silencieuse : hypofixation
antéro-septale avec redistribution apicale et une hypofixation infé-
rieure avec redistribution inverse, sans angor au maximum de l’ef-
fort.
Une indication chirurgicale est retenue. Le bilan préopératoire
comporte une angiographie sus-sigmoïdienne qui confirme le
faux anévrysme de l’aorte ascendante à sa partie postérieure et
l’insuffisance aortique grade III (figure 3).
La coronarographie objective plusieurs sténoses significatives,
de localisations tritronculaires : deux sténoses serrées de l’artère
interventriculaire antérieure proximale avec bon lit d’aval, deux
sténoses serrées marginales avec bon lit d’aval, une sténose ser-
rée circonflexe avec lit d’aval grêle, une sténose coronaire droite
proximale avec bon lit d’aval (figure 4).
La ventriculographie retrouve une hypokinésie antérieure, une
akinésie inférieure et apicale. La fraction d’éjection angiogra-
phique est à 30 %.
Le patient est alors transféré en chirurgie cardiaque où il bénéfi-
cie d’un remplacement total de l’aorte ascendante par tube val-
vulé Saint Jude n° 23 avec réimplantation des coronaires, et de
pontages mammaires internes gauche et droit avec montage en
Y:l’artère mammaire interne gauche est implantée sur l’artère
interventriculaire antérieure, l’artère mammaire interne droite sur
l’artère marginale. Le pontage veineux saphène-aorto-coronaire
droite est implanté sur le tronc artériel brachio-céphalique. L’exa-
men peropératoire objective une brèche postérieure de 1 cm au
niveau de la suture, donnant accès au faux anévrysme postérieur,
et un prolapsus intraventriculaire gauche de la valve aortique.
Les suites opératoires sont simples.
La Lettre du Cardiologue - n° 326 - mars 2000
18
CAS CLINIQUE
Figure 2. Échographie bidimensionnelle, coupe parasternale grand axe :
visualisation d’un faux anévrysme de 3 cm de la paroi postérieure de
l’aorte .
Aorte
Faux anévrysme
Figure 3. Aortographie sus-sigmoïdienne : faux anévrysme de la paroi
postérieure de l’aorte ascendante et insuffisance aortique.
Faux anévrysme
Figure 4. Coronarographie sélective. En haut : coronaire droite ; en
bas : coronaire gauche, athérome tritronculaire.

La Lettre du Cardiologue - n° 326 - mars 2000
19
DISCUSSION
L’ischémie myocardique est silencieuse chez les patients ayant
bénéficié de chirurgie cardiaque avec nécessité de dénervation
myocardique. C’est le cas des transplantés cardiaques (1), mais
cela pourrait également concerner des patients chez lesquels
l’aorte ascendante et la crosse aortique ont été remplacées.
Au cours du suivi des patients opérés par technique de Bentall
après dissection aortique, le mode de présentation de l’ischémie
myocardique n’a pas, à notre connaissance, été décrit : de nom-
breuses études de suivi ont été réalisées afin de déterminer la
morbi-mortalité de ce type d’intervention (2,3,4), mais les symp-
tômes – tels que la douleur thoracique – révélant un infarctus du
myocarde n’ont pas été détaillés.
L’originalité de cette observation réside dans le caractère silen-
cieux de l’ischémie myocardique (deux nécroses myocardiques
avec ischémie silencieuse documentée à la scintigraphie de stress)
chez ce patient, dont la face antérieure de la crosse aortique a été
remplacée .
L’hypothèse que nous émettons est qu’il pourrait exister une simi-
litude entre l’ischémie silencieuse d’un transplanté cardiaque et
celle de M.L., dont la crosse aortique a été sectionnée chirurgi-
calement (la porte d’entrée de la dissection était située à la face
antéro-gauche de l’aorte) : l’absence d’angor pourrait être en rela-
tion avec la dénervation chirurgicale.
En effet, les rameaux afférents (à destinée encéphalique) des
pneumogastriques et du sympathique s’étendent à la face antéro-
gauche de la crosse aortique (alors que les efférences du plexus
cardiaque sont en arrière de la crosse) (5).
Ainsi, il serait utile de rechercher périodiquement, après rem-
placement de l’aorte ascendante, une ischémie myocardique silen-
cieuse chez les patients avec de nombreux facteurs de risque
d’athérosclérose .
Ce suivi ne saurait être semblable à celui du transplanté cardiaque,
chez lequel une coronarographie annuelle est réalisée, à la
recherche de la maladie athéromateuse du greffon dont la pro-
gression peut être très rapide (6). En revanche, la prise en charge
des patients chez lesquels l’aorte proximale a été remplacée,
etchez ceux à risque élevé d’athérosclérose pourrait être similaire
à celle du diabétique (7), chez lequel la recherche d’ischémie
myocardique silencieuse doit être systématique en cas d’antécé-
dent coronarien sans angor résiduel, d’anomalie électrique (isché-
mie/nécrose) sans angor, ou de plusieurs facteurs de risque coro-
naire associés ; dans ce cas, nous proposons une épreuve d’effort
tous les deux ans et une scintigraphie au thallium 201 (effort et/ou
dipyridamole), ou une échographie avec injection de dobutamine
si l’épreuve d’effort est sous-maximale.
CONCLUSION
Le caractère silencieux de l’ischémie myocardique de ce patient
non diabétique suggère une relation avec les antécédents de chi-
rurgie de l’aorte ascendante, où une dénervation chirurgicale a
été effectuée.
Cela impliquerait que l’ischémie myocardique soit systémati-
quement recherchée lors du suivi des patients ayant bénéficié
d’une chirurgie de l’aorte proximale incluant la crosse et pré-
sentant un risque d’athérosclérose coronaire élevé. ■
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Banner N.R., Yacoub M.H. Physiology of the orthotopic cardiac transplant
recipient. Semin Thorac Cardiovasc Surg 1990 ; 2 : 259.
2. Fournial G., Concina P., Glock Y. et coll. Résultats à long terme du traitement
chirurgical d’une dissection aiguë de type A de l’aorte thoracique. Arch Mal
Cœur 1997 ; 90 : 1233-7.
3. Gillinov A.M., Lytle B.W., Kaplon R.J., Casselman F.P., Blackstone E.H.,
Cosgrove D.M. Dissection of the ascending aorta after previous cardiac surgery :
differences in presentation and management. J Thorac Cardiovasc Surg 1999 ;
117 : 252-60.
4. Taniguchi K., Nakano S., Matsuda H. et coll. Long term survival and compli-
cations after composite graft replacement for ascending aortic aneurysm asso-
ciated with aortic regurgitation. Circulation 1991 ; 84 (suppl. 5) : III31-9.
5. Rouvière H. Innervation cardiaque. In : Anatomie humaine descriptive et topo-
graphique. 8eédition. Paris, Masson et Cie. 1959 : 674.
6. Nitkin R.S., Schroeder J.S. Accelerated coronary artery disease risk in heart
transplant patients. J Am Coll Cardiol 1985 ; 5 (suppl. II) 535.
7. Passa Ph., Drouin P., Issa-Sayegh M. et coll. Coronaires et diabète.
Recommandations de l’ALFEDIAM . Diabete Metab 1995; 21 : 446-51.
CAS CLINIQUE
CHIESI SA (Justor), p. 28 ;
FOURNIER (Cholstat), p. ;
GLAXO WELLCOME (Pritor), p. 11 ;
LIPHA SANTÉ (Fozitec), p. ;
SHERING PLOUGH (Integrilin), p. 15-16.
ANNONCEURS
1
/
3
100%