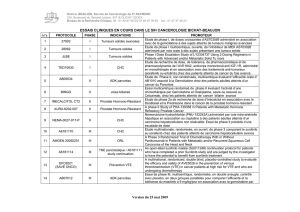
Cancers du rein, de la vessie et du testicule t

Tumeurs urologiques
Tumeurs urologiques
53
La Lettre du Cancérologue - Vol. XVII - n° 1-2 - janvier-février 2008
Cancers du rein, de la vessie et du testicule
Kidney, bladder and testicular cancers
●● P. Beuzeboc*
* Département d’oncologie médicale, Institut Curie, Paris.
I
l faut avant tout insister sur l’important travail de rédac-
tion du Comité cancérologique de l’association française
d’urologie (CCAFU), lequel, sous la férule de son président
Jean-Louis Davin, a permis d’élaborer les recommandations 2007
concernant les tumeurs urologiques. Espérons que, éditées dans
Progrès en urologie (1), elles soient également largement distri-
buées dans la communauté oncologique afin que chacun y trouve,
dans le cadre des décisions multidisciplinaires, la justification
de ses bonnes pratiques. Ce document a aussi reçu l’aval et le
soutien du Groupe d’études des tumeurs uro-génitales (GETUG),
et de la Société française de radiothérapie oncologique (SFRO).
Il devrait servir de base aux référentiels de l’Institut national
du cancer (INCA).
CANCER DU REIN
Épidémiologie
Évolution des présentations
Les données provenant du programme SEER (Surveillance, epide-
miology and end results) concernant 29 053 patients diagnosti-
qués au cours de 3 périodes de 5 ans (1988-1992, 1992-1997,
1997-2002) ont montré que, aux États-Unis, la taille de la tumeur
avait diminué de 66,8 mm à 58,6 mm avec une augmentation de
l’incidence ajustée à l’âge de 8,6 à 11,2 cas pour 100 000 habitants
(2). Le pourcentage de tumeurs de 4 cm et moins a augmenté
dans les 3 périodes (30 %, 34 % et 39 % respectivement) alors
que celui des tumeurs de plus de 7 cm diminuait (34 %, 33 % et
30 %). Pour les tumeurs de 4 à 7 cm, la médiane de survie était
de 105 mois versus 46 mois pour celles de plus de 7 cm.
Traitement local
Tumeurs du rein : traitement par radiofréquence, alter-
native à la chirurgie dans des indications particulières ? (3)
Actuellement, les indications principales des traitements par
radiofréquence dans les cancers du rein sont les tumeurs récidi-
vantes, les lésions survenant chez les patients âgés pour lesquels
la chirurgie serait risquée, les insuffisants rénaux et les patients
à courte espérance de vie. Dans ces indications, la morbidité
est inférieure à celle de la chirurgie.
Les progrès en imagerie permettent de détecter des lésions
cancéreuses rénales de petites tailles (entre 1 et 1,5 cm), décou-
vertes parfois fortuitement, par exemple lors d’échographies
exploratrices devant des douleurs abdominales. Les biopsies
permettent de confirmer leur origine néoplasique. La radio-
fréquence pourrait alors représenter un traitement de choix des
tumeurs inférieures à 2,5 cm, le suivi se faisant par imagerie par
résonance magnétique (IRM). Si la tumeur continue à prendre
le contraste, le patient peut être traité de nouveau par radio-
fréquence, ou opéré.
Marges positives après néphrectomie partielle par lapa-
roscopie
Faut-il de nouveau opérer systématiquement les patients, ou peut-on
parfois simplement les surveiller, comme le laisse entendre
l’expérience rapportée par S. Permpongkosol et al. (4) ?
Études de phase III des formes avancées
en première ligne
Sunitinib versus interféron
Une vaste étude ouverte, multicentrique, internationale et de
phase III (5) a randomisé, entre août 2004 et octobre 2005,
•
•
•
•
RÉSUMÉ
On n’arrête pas le progrès dans les cancers du rein métas-
tatique... Après le sunitinib et le sorafénib, l’association du
bévacizumab et de l’interféron, le temsirolimus, le pazopanib
et l’axitinib ont fait la preuve de leur ecacité.
Dans les cancers de la vessie avancés, l’addition du pacli-
taxel à la combinaison gemcitabine-cisplatine (GC) ne s’est
pas révélée supérieure au doublet GC dans une étude de
phase III de l’EORTC.
Mots-clés : Cancer du rein – Cancer de la vessie – Cancer
du testicule.
▶
SUMMARY
Progress cannot be stopped in metastatic kidney cancer…
Following sunitinib and sorafenib, bevacizumab associated
with interferon, temsirolimus, pazopanib and axitinib have
demonstrated their ecacy.
In advanced bladder cancer, the addition of paclitaxel to
the gemcitabine/cisplatine combination is not superior
to the doublet gemcitabine/cisplatine in a large EORTC
phase III trial.
Keywords: Kidney cancer – Bladder cancer – Testicular
cancer.
▶
LK 1-2008-int.indd 53 28/02/08 14:25:52

Tumeurs urologiques
Tumeurs urologiques
54
La Lettre du Cancérologue - Vol. XVII - n° 1-2 - janvier-février 2008
750 patients, stratifiés en fonction du taux de lactase déshydrogé-
nase (LDH), du PS (ECOG 0-1), d’une néphrectomie antérieure
ou non. Dans le bras A (375 patients), le sunitinib était donné
à la dose de 50 mg/j pendant 4 semaines, suivies de 2 semaines
de repos. Dans le bras B (375 patients), les patients recevaient
des injections s.c. d’interféron α à la dose de 3 000 000 UI x 3/sem
la première semaine, de 6 000 000 UI la deuxième semaine et de
9 000 000 UI ensuite. Les traitements étaient poursuivis jusqu’à
progression.
L’évaluation centralisée indépendante a retrouvé des taux de
réponse respectivement de 31 % (103/335) et de 6 % (20/327)
[p < 0,001]. La médiane de survie sans progression (SSP), qui
était le critère de jugement principal, était très significative-
ment meilleure dans le groupe sunitinib, 11 mois versus 5 mois
(hazard-ratio [HR] = 0,42 ; IC95 : 0,32-0,54), et ce indépendam-
ment des facteurs analysés (néphrectomie antérieure, ECOG 0-1,
taux de LDH, intervalle/diagnostic initial, taux d’hémoglobine,
calcémie corrigée).
Temsirolimus, interféron α, ou les deux ?
Le temsirolimus (TEMSR, CCI-779) est un inhibiteur spécifique
de mTOR, une protéine impliquée dans la croissance et la survie
des cellules tumorales.
Une étude de phase III (6) s’est adressée à des patients métas-
tatiques de mauvais pronostic selon les critères de Motzer.
Ceux-ci devaient présenter au moins 3 des 6 critères suivants :
intervalle < 1 an, IK 60-70, taux d’hémoglobine anormal,
calcémie corrigée > 10 mg/dl, LDH > 1,5 N, plus d’un site
métastatique. Six cent vingt-six patients ont été inclus. Le
traitement a fait appel soit à de l’interféron α seul en s.c. à doses
croissantes jusqu’à 18 000 000 UI x 3/sem, soit à du TEMSR
25 mg i.v. hebdomadaire, soit à la combinaison d’interféron à
la dose de 6 000 000 UI x 3/sem et de TEMSR 15 mg/sem. Le
critère de jugement principal était l’amélioration de la survie
globale (SG), selon l’hypothèse d’une amélioration de 40 %, la
médiane de survie devant passer de 4,9 mois avec l’interféron
à 6,9 mois.
Il est apparu que le TEMSR seul améliorait significativement la
médiane de SG par rapport à l’interféron (HR = 0,73, IC95 : 0,58-
0,92), ainsi que la SSP (p < 0,001). En revanche, l’association de
TEMSR et d’interféron ne fait pas mieux que l’interféron seul
(HR = 0,96, IC95 : 0,76-1,2, p = 0,70).
Étude AVOREN comparant bévacizumab + interféron à
interféron + placebo
Cette étude de phase III (7), réalisée dans 101 centres de 18 pays,
a inclus 649 patients néphrectomisés qui ont été randomisés
entre interféron α2a (9 MUI x 3/sem)/bévacizumab (10 mg/
kg/2 sem) versus interféron/placebo. L’objectif principal était
d’évaluer l’efficacité de la combinaison fondée sur la SG. Les
objectifs secondaires étaient la SSP, le temps jusqu’à progression
(TTP), le temps jusqu’à échec du traitement, le taux de réponse
objective (RO) et la tolérance.
Le taux de RO a été de 31 % dans le bras bévacizumab versus
13 % (p < 0,0001).
•
•
Dans le bras bévacizumab, la SSP a doublé, passant de 5,4 mois
à 10,2 mois. Cet effet était retrouvé dans les groupes à bon
pronostic et à pronostic intermédiaire, mais pas dans le groupe
à mauvais pronostic. Ces résultats paraissent assez comparables
à ceux obtenus avec le sunitinib, aujourd’hui considéré comme
le traitement de référence de première ligne.
L’amélioration en termes de SG devra être confirmée par un
suivi plus long.
En ce qui concerne la tolérance, celle-ci paraît tout à fait accep-
table, marquée essentiellement par de la fatigue (12 % versus
8 % dans le bras interféron seul), la perte de force musculaire
(10 % versus 7 %) et la protéinurie (7 % versus 0 %).
Le bévacizumab se positionne pour de futures associations
avec, notamment, les inhibiteurs de mTOR ou des inhibiteurs
de tyrosine kinase (TKI) de récepteurs du VEGF.
Étude TARGET de phase III comparant sorafénib
versus placebo en deuxième ligne
B. Escudier (8) a publié les résultats de l’étude TARGET compa-
rant le sorafénib (BAY 43-9006), un inhibiteur multikinase oral,
à un placebo. L’objectif principal était la SG.
Identifié au départ par ses propriétés d’inhibition de Raf-1, une
sérine thréonine kinase, il agit aussi contre d’autres récepteurs
à tyrosine kinase comme le VEGFR-2, PDGFR, FLT-3 et c-kit.
Neuf cent trois patients présentant un carcinome à cellules
claires métastatiques résistant à un traitement standard ont été
randomisés et stratifiés en fonction des groupes de Motzer et
des pays pour recevoir soit du sorafénib à la dose de 400 mg x 2/j,
soit un placebo.
Les résultats rapportés en 2005 avaient montré une amélioration
significative de la SSP avec 5,5 mois dans le groupe sorafénib
et 2,8 mois dans le groupe placebo (HR = 0,44, IC95 : 0,35-0,55,
p < 0,01) et un crossover avait été autorisé à partir de mai 2005
pour le groupe placebo. Le taux de réponse était de 10 % dans
le groupe sorafénib.
Les résultats finaux rapportés à l’ASCO 2007 (9) ont montré que,
16 mois après le crossover du bras placebo (48 % des patients),
la SG en intention de traitement (ITT) du bras sorafénib n’était
pas significativement différente (17,8 mois versus 15,2 mois
[HR = 0,88, IC
95
= 0,74-1,04, p = 0,146]). Elle ne l’est que si les
patients avec croisement sont censurés.
Études de phase II avec interféron
Études de phase II associant le sorafénib et l’interféron
J.A. Gollob et al. (10) ont rapporté un taux de réponse de 33 %
(IC95 : 19-49) dans une étude de phase II d’association de sora-
fénib (400 mg/j) et d’interféron α2b (10 000 000 UI x 3/sem)
chez 40 patients métastatiques naïfs ou préalablement traités
par interleukine 2. Les médianes de durée de réponse et de
SSP ont été respectivement de 12 mois et de 10 mois (IC
95
:
8-18). Des réductions de doses ont été nécessaires chez 65 %
des patients.
Une autre étude (11) de phase II du SWOG (Southwest Onco-
logy Group) évaluant cette même association de sorafénib
(400 mg x 2/j) et d’interféron α2b (10 000 000 UI x 3/sem)
•
LK 1-2008-int.indd 54 28/02/08 14:25:56

Tumeurs urologiques
Tumeurs urologiques
55
La Lettre du Cancérologue - Vol. XVII - n° 1-2 - janvier-février 2008
a retrouvé un taux de réponse de 19 % (12/62 patients) avec en
plus 50 % de réponse mineure ou une stabilisation. La médiane
de SSP était de 7 mois (IC95 : 4-11).
Les taux de réponse dans ces 2 études paraissent supérieurs à
ceux attendus pour le sorafénib et l’interféron seul. Les toxi-
cités sont dominées par les effets indésirables imputables à
l’interféron (fièvre, frissons, fatigue, amaigrissement, anémie,
élévation des transaminases) qui limitent le développement de
cette association.
Étude de phase I/II associant le temsirolimus
et l’interféron
Une étude multicentrique rapportée par R.J. Motzer (12) a permis
de fixer la dose recommandée de temsirolimus hebdomadaire à
15 mg i.v., et celle d’interféron à 6 000 000 UI x 3/sem, les toxicités
limitantes étant les stomatites, la fatigue, les nausées/vomis-
sements.
Le taux de réponse chez les 39 patients traités à ces doses
a été de 8 %, avec 36 % de stabilisations pendant au moins
24 semaines. La médiane de SSP pour l’ensemble des patients
a été de 9,1 mois.
Combinaison d’un antiangiogénique
et d’un anti-EGFR
Étude de phase II combinant erlotinib + bévacizumab
versus bévacizumab seul : absence de bénéfice de l’associa-
tion (13)
Cent quatre patients ont été randomisés entre bévacizumab
(10 mg/kg/2 sem) combiné à l’erlotinib (150 mg/j) ou un placebo.
La médiane de SSP a été de 9,9 mois pour le bras erlotinib
versus 8,5 mois (p = 0,58), les taux de RO respectivement de
14 % et 13 %.
Selon J. Baselga : “Nous n’y sommes pas encore” (14).
Nouvelles perspectives
Émergence de nouveaux antiangiogéniques dans les
cancers du rein
Deux nouveaux antiangiogéniques émergent, avec des données
préliminaires très encourageantes.
Le premier, le pazopanib, est un TKI de VEGFR-1, VEGFR-2,
VEGFR-3, PDGFR-a/b et c-kit. Après inclusion de 60 patients,
les résultats d’une analyse intermédiaire d’une étude de phase II
(15) devant randomiser les patients après 12 semaines de
pazopanib (800 mg/j p.o.) [traitement revu par un comité
indépendant] en cas de stabilisation entre la poursuite du trai-
tement et un placebo ont montré un taux de réponse de 38 %
(23/60), avec 42 % de stabilisation (25/60). Pour être éligibles
dans l’étude, ces patients devaient présenter un cancer du
rein métastatique non traité préalablement par cytokine, ou
réfractaire après une ligne d’immunothérapie ou de traitement
par bévacizumab.
Au vu de ces résultats, le comité indépendant du monitoring
a recommandé de suspendre la randomisation versus placebo.
Les principaux effets indésirables analysés chez 161 patients ont
été les élévations des transaminases, les diarrhées, la fatigue, les
•
•
•
nausées, la dépigmentation des cheveux et l’hypertension. Les
données définitives en termes d’efficacité et de toxicité concer-
neront 225 patients.
Le second, l’axitinib (AG-013736), est un puissant inhibiteur
de VEGFR-1, VEGFR-2, VEFR-3. Cinquante-deux patients
présentant un cancer du rein métastatique réfractaire au sora-
fénib ont été inclus dans une étude de phase II rapportée par
B.I. Rini à l’ASCO (16) et publiée par O. Rixe dans le Lancet
Oncology (17). En ITT, il a été observé 2 réponses complètes
(RC) et 21 réponses partielles (RP) [44,2 %, IC95 : 30,5-58,7], ainsi
qu’une stabilisation chez 22 patients avec médiane de durée de
réponse de 23 mois. La médiane de SSP était de 15,7 mois (8,4-
23,4 mois) et la médiane de SG était de 29,9 mois (20,3 – non
estimable). Les principaux effets indésirables ont été l’hyper-
tension, la fatigue, les diarrhées et l’enrouement, 28 patients
ont présenté une toxicité de grade 3-4.
Nouvelles pistes en cours de développement
Il faut insister sur :
le RAD 001,
un nouvel inhibiteur de mTOR (18) pour lequel
les premiers résultats d’étude de phase II sont très encoura-
geants ;
l’infliximab,
un anticorps monoclonal anti-TNFα, uti-
lisé par voie i.v. Les premières données préliminaires de
2 études séquentielles avec 2 schémas de doses rapportées par
M.L. Harrison (19) suggèrent une activité thérapeutique poten-
tiellement intéressante avec 32 % de réponse ou une stabilisation
et une médiane de durée de réponse d’environ 6 mois.
Toxicités
Hypothyroïdie et antiangiogéniques
En réponse aux données de D.R. Feldman (21), P. Wolter et al.
(20) ont rapporté, avec le sunitinib, une incidence élevée de
dysfonction thyroïdienne (60 à 70 % des cas) dans une série
de 65 patients. Cependant, seuls 15 % des patients ont nécessité
le traitement d’une hypothyroïdie.
Avec le sorafénib, l’étude de l’équipe de Cleveland (22) a montré
que des perturbations discrètes des tests thyroïdiens étaient
fréquentes (16/39, 41 %) [IC
95
: 26-58] ; les anomalies sévères
et/ou les hypothyroïdies cliniques justifiant un traitement étant
peu fréquentes, un suivi biologique ne se justifiait pas.
Parmi les cas publiés de complications rares, signalons une
micro-angiopathie thrombotique rénale causée par un anticorps
anti-VEGF (23) et une leuco-encéphalopathie (24).
Métastases cérébrales
Entre la possibilité, avec les TKI antiangiogéniques, de réponse
thérapeutique majeure, parfois complète (25), et le risque
hémorragique (26), le choix est difficile. Néanmoins l’expérience
(portant sur 23 patients) rapportée par J.S. Unnithan à l’ASCO
suggère que le sunitinib et le sorafénib peuvent être utilisés sans
risque majeur en cas de métastases cérébrales traitées. Elles ne
devraient plus constituer de contre-indications absolues à leur
utilisation (27).
•
▶
▶
•
•
LK 1-2008-int.indd 55 28/02/08 14:25:59

Tumeurs urologiques
Tumeurs urologiques
56
▶▶▶
La Lettre du Cancérologue - Vol. XVII - n° 1-2 - janvier-février 2008
Tumeurs rares
Gemcitabine-cisplatine dans les carcinomes des tubes
collecteurs (carcinomes de Bellini)
L’étude du GETUG (28), première étude prospective évaluant l’asso-
ciation de cisplatine et de gemcitabine, et portant sur 23 cas de
carcinomes de Bellini métastatiques, a montré un taux de réponse
de 26 % (IC95 : 8-44) avec une médiane de SSP de 7,1 mois (IC95 :
3-11,3) et une médiane de survie de 10,5 mois (IC95 : 3,8-17,1).
Efficacité du topotécan dans les tumeurs de Wilms
Une étude de phase II (29) portant sur 25 patients évaluables en
récidive après au moins une ligne de chimiothérapie a rapporté
un taux de réponse de 48 % (IC95 : 27,8-68,7).
Tumeurs carcinoïdes du rein
Une revue de 56 cas (30) a permis de définir les principales carac-
téristiques de ces tumeurs exceptionnelles. Il est essentiel, même
si les métastases rénales d’une tumeur carcinoïde sont rares,
de s’assurer par une scintigraphie à l’octréotide qu’il s’agit bien
d’une tumeur primitive. L’âge médian était de 49 ans. Un rein en
fer à cheval était présent dans 17,8 % des cas. Le diagnostic a été
fortuit dans 28,6 % des cas. Seuls 12,7 % des patients présentaient
un syndrome neuro-endocrine. La tumeur était supérieure
à 4 cm pour 73,6 % d’entre les patients, des métastases étaient
présentes chez 45,6 % des patients au diagnostic.
CANCER DE LA VESSIE
Biologie
Mutations de p53 dans les tumeurs superficielles à haut
risque
Dans les tumeurs superficielles à haut risque, la valeur pronos-
tique de la présence d’une p53 mutée dans la cytologie du lavage
urinaire n’est pas suffisante pour modifier les décisions indivi-
duelles (31).
Biologie de la progression tumorale
Il paraît absolument nécessaire de mieux comprendre les voies
moléculaires impliquées dans la progression tumorale pour envi-
sager l’utilisation de traitements ciblés. A.P. Mitra et al. (32), dans
une revue générale publiée dans le Journal of Clinical Oncology,
font le point sur les altérations de la p53, de RB, de ras, sur l’an-
giogenèse, les événements épigénétiques et génétiques impliqués
dans les interactions moléculaires de ces différentes voies.
Famille HER
Les profils d’expression des récepteurs de la famille ErbB peuvent
avoir une signification pronostique, comme le montrent les
travaux canadiens de l’équipe de l’université McGill (33), portant
sur une cohorte de 248 patients. Une expression élevée de l’EGFR
ou une expression basse d’ErbB-4 (au contraire du niveau de
celle d’erbB-2 et erbB-3) était associée de façon statistiquement
significative à un grade élevé et à des tumeurs invasives, ainsi
qu’à des survies sans récidive (SSR) et à des SG plus courtes.
•
•
•
•
•
M.A. Jacobs et al. (34) ont étudié la fréquence des mutations
dans le domaine kinase (exons 18-21) du récepteur de l’EGF, et
ont retrouvé, sur une série de 112 tumeurs invasives, un total
de 6 mutations chez 4 patients (3,6 %) au niveau de l’exon 21. Ils
ont également testé l’action de l’erlotinib sur un panel de lignées
cellulaires, et ont montré que, malgré la rareté des mutations
de l’EGFR, il existait une sensibilité variable à l’erlotinib, et que
le maintien d’un état de phosphorylation d’AKT en présence
d’erlotinib était corrélé à une résistance à ce traitement.
Survivine
La survivine appartient à une famille de protéines inhibitrices de
l’apoptose. Elle est surexprimée dans de nombreuses tumeurs,
mais rarement détectée dans des tissus normaux.
Elle pourrait être un biomarqueur prometteur dans le diagnostic,
le pronostic, la prédiction de réponse à un traitement intravésical
ou systémique (35). Une étude (36) a retrouvé, dans une série de
222 cystectomies avec lymphadénectomie, son expression dans
64 % des tumeurs vésicales et 94 % des atteintes ganglionnaires.
L’expression était corrélée à la récidive (p = 0,04), la mortalité
spécifique (p = 0,037) et la mortalité globale (p = 0,044). Cela ouvre
potentiellement la voie à des traitements ciblant la survivine.
Chirurgie
Résultats de la cystectomie dans les séries contemporaines
S.F. Shariat et al. (37) ont présenté les caractéristiques et les
résultats de 3 grandes séries consécutives de 888 patients (81 %
d’hommes, âge moyen de 66,2 ans) traités par cystectomie radi-
cale et curage ganglionnaire dans 3 centres académiques améri-
cains entre 1984 et 2003. Sept pour cent des patients étaient pT0,
43 % d’entre eux avaient une extension extravésicale, 25 % une
extension extravésicale sans atteinte ganglionnaire et 23 % présen-
taient des métastases ganglionnaires. Les SSR et spécifiques à
5 ans étaient respectivement de 58 % ± 2 % et 66 % ± 2 %.
Elles étaient à 10 ans de 71,9 % ± 3 % et de 77,8 % ± 4 % pour
les tumeurs ≤ pT2N0 l, de 47,3 % ± 4 % et de 50 % ± 5 % pour
les tumeurs > pT2N0, et de 16,2 % ± 5 % et 25,5 % ± 4 % pour
les tumeurs pT1-4 N+.
Formes avec uropathie obstructive
Une équipe indienne (38) a analysé une série de 58 patients présen-
tant une tumeur invasive avec uropathie obstructive. La cystec-
tomie ne semble pas associée à une morbidité supérieure.
Survie par chirurgie seule en cas d’atteinte ganglion-
naire au-delà de la bifurcation des vaisseaux iliaques. Des
données danoises en faveur du curage extensif
K. Steven et A.L. Poulsen (39) ont rapporté les données portant
sur une cohorte de 336 patients successifs traités entre 1993
et 2005 par cystectomie et curage ganglionnaire iliaque extensif
(le nombre médian de ganglions retirés était de 27, allant
de 11 à 49). La SSR et la SG de l’ensemble de la série étaient,
respectivement, de 68 % et 69 %. Soixante-quatre patients (19 %)
présentaient une atteinte ganglionnaire, dont 22 (34,4 %) au-
dessus de la bifurcation iliaque. La probabilité de survie à 5 ans
•
•
•
•
LK 1-2008-int.indd 56 28/02/08 14:26:03

Tumeurs urologiques
Tumeurs urologiques
58
▶▶▶
La Lettre du Cancérologue - Vol. XVII - n° 1-2 - janvier-février 2008
était de 39 % en cas d’atteinte ganglionnaire (versus 76 %). La
survie était significativement plus élevée en cas de N+ ≤ 5 (50 %
versus 13 %, p < 0,002). La survie, en revanche, était identique
chez les patients avec une atteinte au-delà de la bifurcation.
Sujets âgés, importance du PS (performance status)
L’analyse rétrospective d’une cohorte consécutive de 152 patients
âgés de plus de 70 ans (76 ans en moyenne) traités au Ann Arbor
entre 1995 et 2005 (40) a montré qu’un indice de Karnofsky (IK)
supérieur ou égal à 90 était un important facteur prédictif de la
survie (p = 0,05). Soixante-quinze pour cent des patients avaient
opté pour la cystectomie. Seuls 15 % d’entre eux ont été traités
dans une intention palliative.
Chimiothérapie
Chimiothérapie périopératoire
La chimiothérapie périopératoire (dans les 4 mois précédant ou
suivant la chirurgie) est sous-utilisée aux États-Unis pour les
tumeurs de stade III entre 1998 et 2003 : en fait état un rapport
accablant de la National Cancer Data Base (41).
La National Cancer Data Base a collecté les données se rappor-
tant à approximativement 60 % des nouveaux cas de cancers de la
vessie aux États-Unis entre 1998 et 2003. Sur 7 161 des 11 339 cas
de cancer urothélial de stade III, une analyse a été possible. Une
chimiothérapie a été administrée dans seuls 11,6 % des cas (10,4 %
de chimiothérapies néo-adjuvantes et 1,2 % de chimiothérapies
adjuvantes). Ces données font insister sur la difficulté, parfois,
d’intégrer dans la pratique les données des essais randomisés.
Sans commentaire.
C. Sternberg a de nouveau fait, dans un très bon article de
synthèse (42), le point sur la chimiothérapie néo-adjuvante ou
adjuvante dans le contexte de stratégies ayant pour but une
amélioration de la survie, mais aussi, dans certains cas, une
préservation vésicale.
Chimiothérapies des formes avancées
Trois revues générales ont fait le point sur les chimiothérapies
de première et deuxième lignes
(43-45).
En Europe, l’utilisation de l’association gemcitabine-cisplatine
s’est de plus en plus imposée. La substitution du cisplatine au
carboplatine, la combinaison d’un sel de platine et d’un taxane
(docétaxel-cisplatine et paclitaxel-carboplatine) et l’étude de
triplets avec paclitaxel ont constitué les principaux axes de
recherche de ces dernières années. Pour les patients unfit, ne
pouvant recevoir de traitements à base de cisplatine, le choix d’un
traitement par M-CAVI (méthotrexate, carboplatine, vinblastine),
par carboplatine-gemcitabine, carboplatine-paclitaxel, gemcita-
bine-taxane, ou d’une monothérapie par soit de la gemcitabine,
soit du carboplatine, soit un taxane (paclitaxel hebdomadaire)
peut se discuter. Parmi les nouvelles molécules, l’intérêt s’est
porté sur le pémétrexed (28 % de RO dans une étude de phase II),
sur l’oxaliplatine et la vinflunine. Les tumeurs de la vessie restent
l’un des parents pauvres des thérapies ciblées, même si se déve-
loppent des études de traitements dirigés contre les récepteurs
de la famille HER et, plus récemment, d’antiangiogéniques.
•
•
•
L’étude EORTC/Intergroup 30987 comparant, dans les cancers
urothéliaux avancés ou métastatiques, une chimiothérapie
par paclitaxel-cisplatine/gemcitabine à l’association cispla-
tine-gemcitabine n’a pas montré d’avantage significatif de
l’apport du paclitaxel.
Cette étude a inclus, dans 107 centres, 627 patients T4bN0M0,
TxN2-3 ou M1 jamais traités par chimiothérapie et randomisés
entre l’association de référence cisplatine (70 mg/m2 J1 ou J2) et
gemcitabine (1 000 mg/m
2
J1, J8 et J15) tous les 28 jours (tous les
21 jours en l’absence de J15), et la triple association de cisplatine
(70 mg/m
2
J1), de gemcitabine (1 000 mg/m
2
J1, J8), et de pacli-
taxel (80 mg/m2 J1, J8) tous les 21 jours. L’objectif principal était
l’amélioration de la SG, les objectifs secondaires la SSP, le taux
de réponse, la durée de réponse et la toxicité. Pour témoigner
d’une amélioration de la médiane de survie de 14 mois à 18 mois
(HR = 0,78) fondée sur un test de log-rank bilatéral avec α = 0,05
et β = 0,20, il était prévu l’inclusion de 610 patients en 3 ans. La
répartition entre les groupes à risque de Barjorin était équili-
brée pour les 2 bras. Les arrêts de traitements pour toxicité
ont été comparables, respectivement 14,9 % (doublet) versus
13,8 % (triplet). Les taux de RO se sont révélés significativement
supérieurs dans le bras paclitaxel (57 % versus 46 %, p = 0,02). En
revanche, il n’a été retrouvé aucune différence significative en
termes de SSP (8,8 mois versus 7,7 mois, réduction du risque
de 13 %, NS) et de SG (12,8 mois versus 15,7 mois, réduction
du risque de 14 %, NS) [46].
Vinflunine, un nouvel agent antitubuline
S. Culine et al. (47) ont rapporté les résultats d’une étude multi-
centrique de phase II ayant inclus 51 patients en deuxième ligne
d’un cancer urothélial avancé, traités à la dose de 320 mg/m
2
tous
les 21 jours. Le taux de réponse a été de 18 % (IC
95
: 8,4-30,9), avec
69 % des patients en stabilisation ou en réponse mineure (IC95 :
52,1-79,3) et une médiane de durée de réponse de 9,1 mois (IC
95
:
4,2-15). Les médianes de SSP et de SG étaient respectivement
de 3 mois (IC95 : 2,4-3,8) et de 6,6 mois (IC95 : 4,8-7,6). Les prin-
cipales toxicités ont été des toxicités hématologiques (67 % de
neutropénies de grades 3 et 4, avec 10 % de neutropénies fébriles
dont 2 fatales) et une constipation (8 % de grades 3 et 4).
Une deuxième étude multicentique internationale de phase II
(CA 183001) [48] en deuxième ligne de tumeurs urothéliales
réfractaires au platine a inclus 114 patients en progression dans
les 12 mois suivant une chimiothérapie à base de platine. La dose
initiale pouvait être soit 320 mg/m2 tous les 21 jours (n = 34),
soit 280 mg/m2/21 j (n = 80) en cas de radiothérapie pelvienne
antérieure, d’un IK 80 ou 90, d’un âge de 75 ans ou d’une clai-
rance de créatinine < 60 ml/mn. Les résultats viennent d’être
présentés à l’ECCO 2007 (47) : le taux de réponse est de 15 %, la
durée médiane de réponse de 6,8 mois (IC95 : 5,6-9,5), la durée
médiane de stabilisation de 4 mois (IC
95
: 3,2-4,5) ; le taux de
contrôle de la maladie (RC + RP + stabilisation) est de 57 %, la
médiane de SSP de 2,8 mois (IC95 : 2,6-3,8) et la médiane de SG
de 8,3 mois (IC95 : 7,2-9,8).
Une étude de phase III est en cours (étude VINCENT) et porte
sur des patients en première ligne de traitement, et inéligibles au
•
LK 1-2008-int.indd 58 28/02/08 14:26:08
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%