C Recherche avancée et appliquée chez le sujet âgé COMPTE-RENDU

84 | La Lettre du Cancérologue • Supplément 2 au vol. XXI - n° 6 - juin 2012
COMPTE-RENDU
ETANALYSE
Chicago 2012
Recherche avancée
et appliquée chez le sujet âgé
Oncogeriatry 2012: progress in clinical and biological research
E. Carola*
* Unité pilote de coordination en
oncogériatrie, chef du pôle d’onco-
logie médicale, groupe hospitalier
public du sud de l’Oise ; Société
franco phone d’oncogériatrie.
C
ette année, l’oncogériatrie était très repré-
sentée, en particulier dans des sessions
spécifi ques, qui se sont déclinées en 4 temps
principaux :
➤la recherche clinique ;
➤le ciblage physique et génomique ;
➤les traitements adjuvants ;
➤
la prise en charge de la maladie à un stade
avancé.
Par ailleurs, des études oncogériatriques ont trouvé
leur place dans les sessions d’organes, confi rmant le
rôle transversal indispensable de cette spécifi cité.
Recherche clinique
en oncogériatrie :
constat statistique, concept
méthodologique, exemple
pratique
La représentation des patients âgés de plus de
75 ans reste très faible dans les études de recherche
clinique de phases II et III, comme l’a constaté le
Dr Mooney à partir des données démographiques
des populations incluses dans les essais cliniques du
NCI (Clinical Trials Cooperative Group). De 2001 à
2010, force est de constater que le taux d’inclusion
de ces patients est resté modeste (9 % de la totalité
des inclusions). Il varie bien évidemment selon la
localisation tumorale et le traitement proposé. Les
tumeurs du sein, qui concernent 40 % des sujets
inclus dans ces essais, n’apportent une contribution
que de 4 % en termes de sélection de malades âgées
(l’hormonothérapie étant très souvent privilégiée
avec l’âge). À l’opposé, les tumeurs génito-urinaires,
qui ne constituent que 11 % de la population
recrutée dans la totalité des essais, impliquent près
de 20 % des patients âgés, traités, en particulier,
pour la maladie prostatique (tableau I). Ainsi, une
réfl exion au NCI sur les modalités de conduite de
la recherche clinique chez le patient âgé constate
qu’actuellement les informations sont obtenues à
partir d’analyses poolées rétrospectives, d’études
de sous-groupes âgés dans des essais prospectifs
et, enfi n, de protocoles plus récents spécifi ques aux
sujets âgés. Une certaine ambiguïté persiste sur la
reconnaissance de l’âge limite qui défi nit la popu-
lation âgée, quoique l’on semble enfi n tendre vers
un consensus : 75 ans.
L’Europe n’est pas en reste. Les objectifs des études
dans cette population doivent prendre en considé-
ration les toxicités plus fréquentes et plus lourdes
chez les patients âgés, ainsi que les risques de décès
d’autre cause que la maladie. La qualité de vie doit
intégrer ces objectifs.
Enfi n, le Dr Mohile a rappelé l’intérêt de cohortes
observationnelles chez les patients âgés du fait de
la grande hétérogénéité de profi l de ces patients, et
de la nécessité de connaître l’effet des traitements
dans la vie courante et non dans une population
sélectionnée non représentative.
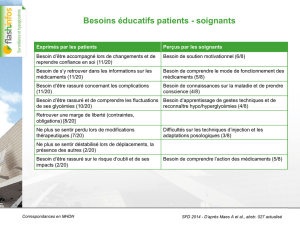
Tableau I. Pourcentage de patients en fonction de l’âge inclus dans les essais de phases II et III
du NCI. Essais de 2001 à 2010.
Localisation Pourcentage
desessais
Pourcentage
despatients
<65ans
Pourcentage
despatients ≥65ans
ou<75ans
Pourcentage
despatients
≥75ans
Sein 40 80 16 4
Gastro-intestinal 14 63 26 10
Génito-urinaire 11 45 37 18
Gynécologique 10 68 24 8
Hématologique 965 21 11
Poumon 850 35 15

Témoins
Exercice
6
4
2
0
Fatigue (changement moyen)
– 2
– 4
BFI
BFI : Body Fatigue Index ; POMS-F : Profile of Mood State-Fatigue ;
MFSI : Multidimensional Fatigue Symptom Inventory.
POMS-F1
Mesure de la fatigue
MFSI
p ≤ 0,05
p ≤ 0,05
p ≤ 0,10
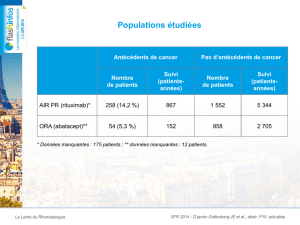
Figure 1. Résultats de l’étude EXCAP : fatigue.
0
60
80
20
40
100
Court
OR = 2,17 ; p = 0,06 GVS = ∑ des facteurs de vulnérabilité
Majeurs : – score ADL < 6
– score IADL < 25
– albuminémie < 35 g/l
Mineurs : – lymphopénie < 1 g/l
– score HADS > 14
➙ Vulnérable si GVS ≥ 3
Long
Longueur du télomère
Patients vulnérables
(GVS ≥ 3 ; ≥ 2 major C, %)
◆ Pas de corrélation significative avec les composants GVS
◆ Mais une corrélation entre la longueur du télomètre des patients (court versus long)
et la vulnérabilité (GVS ≥ 3 ; GVS ≥ 2 critères majeurs)
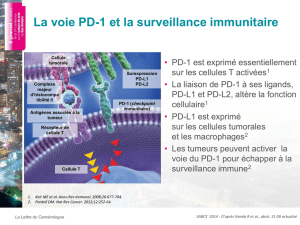
GVS : Geriatric Vulnerability Scale.
Figure 2. Télomères courts corrélés à la vulnérabilité : étude Gynéco-FAG.
La Lettre du Cancérologue • Supplément 2 au vol. XXI - n° 6 - juin 2012 | 85
Résumé
Paramètres gériatriques
physiques et génomiques
Les personnes âgées aux antécédents de cancer
présentent un risque supérieur de limitation des
performances physiques à celui des personnes sans
antécédents de cancer (Sprod L et al., abstr. 9009 ;
Mustian KM et al., abstr. 9010). La mise en place d’un
programme d’exercices peut améliorer la fonction
cardiopulmonaire ainsi que la force musculaire des
patients âgés atteints de cancer de la prostate traités
par radiothérapie et/ou hormonothérapie (protocole
EXCAP) [tableau II et fi gure 1]. C’est l’occasion de
rappeler que, dans ce domaine, l’étude CAPADOGE
est en cours en France.
L’intervention fondamentale du Dr C. Falandry
(abstr. 9011) a ouvert une nouvelle piste de recherche
avec l’étude de la prédictivité du raccourcissement
des télomères sur la vulnérabilité, la toxicité et la
survenue de décès précoces chez les patientes âgées
traitées par carboplatine pour un cancer de l’ovaire
avancé. Cette étude a été menée de 2007 à 2010
sur 111 malades. Les résultats de l’objectif principal
ont été publiés ; les facteurs prédictifs négatifs de
toxicité et de décès précoces en analyse multiva-
riée rapportés étaient l’âge, le stade avancé de la
maladie (IV versus III), l’association avec du pacli-
taxel, la dépression et la lymphopénie. L’infl uence de
la longueur des télomères a également été étudiée.
Il apparaît qu’un raccourcissement des télomères
(< 6 000 paires de bases) est associé à une réduction
du traitement initialement programmé, mais aussi
à un risque augmenté d’effets indésirables sévères
(OR = 2,69 ; IC95 : 1,17-6,19 ; p = 0,019), d’hospitalisa-
tions non programmées (OR = 2,14 ; IC
95
: 0,92-4,95 ;
p = 0,070) et de toxicités non hématologiques de
grade ≥ 3 (OR = 2,04 ; IC95 : 0,88-4,71 ; p = 0,095).
Selon le score de vulnérabilité défi ni par cette équipe,
une corrélation a été à nouveau retrouvée entre une
vulnérabilité défi nie ≥ 3 et des télomères courts
(OR = 2,17 ; p = 0,06). La survie globale est également
corrélée à la longueur des télomères (< 6 000 paires
de bases), tant pour les stades III que IV (HR = 1,57 ;
IC95 : 0,98-2,51 ; p = 0,06) [fi gure 2].
Le Pr P. Soubeyran (abstr. 9012) revient cette année
avec des compléments d’information permettant
Tableau II. Résultats de l’étude EXCAP.
Bras contrôle Bras exercice
Inclusion,
moyenne depas
journaliers
5 861 6 548
Après intervention,
moyenne
de pas journaliers
2 471 7 180
Effets indésirables 1 AE/8 SAE 2 AE/7 SAE
AE:
adverse event
; SAE:
severe adverse event
.
Le 48
e
congrès américain en cancérologie de 2012 a été l’occasion de faire de nombreuses mises au point
dans le domaine de l’oncogériatrie, mais aussi de découvrir de nouveaux paramètres prédictifs biologiques.
Le raccourcissement des télomères est associé à une réduction du traitement initialement programmé,
mais aussi à un risque augmenté d’effets indésirables sévères, d’hospitalisations non programmées et de
toxicités non hématologiques de grade ≥ 3.
Un nouveau paramètre d’évaluation : le déclin fonctionnel précoce est prédictif de la survie.
Les nouvelles études adjuvantes intègrent des paramètres génomiques (ASTER).
Les objectifs principaux habituels deviennent des critères composites.
La recherche clinique et biologique s’adapte à l’hétérogénéité de la population âgée.
Mots-clés
Oncogériatrie
Télomère
Déclin fonctionnel
Critères composites

0
40
60
20
80
0
Aucun déclin fonctionnel précoce
Déclin fonctionnel précoce
21 4 5
Suivi médian : 5,16 années (4,87-5,47)
RR = 1,310
p = 0,16
6783Années
Survie (%)
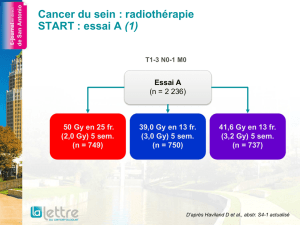
Figure 3. Corrélation entre déclin fonctionnel précoce et survie.
86 | La Lettre du Cancérologue • Supplément 2 au vol. XXI - n° 6 - juin 2012
Recherche avancée etappliquée chez le sujet âgé
COMPTE-RENDU
ETANALYSE
Chicago 2012
d’affi ner l’évaluation prédictive d’événements lors du
traitement oncologique des patients âgés. Il propose
un nouveau paramètre : le déclin fonctionnel précoce
à partir du score ADL (Activities of Daily Living), d’une
évaluation gériatrique sommaire à l’inclusion ainsi
qu’après le second cycle et retient une diminution
du score d’au moins 0,5 point.
Cette étude a concerné 299 patients de plus de
70 ans atteints de différentes localisations tumorales
et ayant bénéfi cié d’une première ligne de chimio-
thérapie. L’âge moyen était de 77,3 ans ; 78 % des
patients avaient un ECOG PS de 0-1. Un patient sur 2
était porteur de métastases, et les localisations les
plus fréquentes étaient hématologiques et digestives.
En analyse multivariée, la diminution du score ADL
et la dépression apparaissent prédictifs du risque
de déclin fonctionnel précoce, associé à une dimi-
nution de la survie (HR = 1,518 ; IC95 : 1,879-2,134 ;
p = 0,016) [fi gure 3].
Traitement adjuvant
chez le patient âgé :
de nombreuses questions,
quelques réponses…
Cancer du sein
(Adjuvant Therapy for Older Women with Early-Stage
Breast Cancer: Treatment Selection in a Complex
Population ; Educational book, Owusu C et al.)
Une fois encore, la sous-représentation des patientes
âgées atteintes de cancer du sein ne permet pas de
disposer de recommandations spécifi ques défi nitives,
mais certaines références détaillent les risques des
différents traitements et les complications à éviter.
L’hormonothérapie en situation adjuvante garde
une place de choix. Les antiaromatases confi rment
leur supériorité sur le tamoxifène pour la survie sans
maladie, mais pas pour la survie globale. La méta-
analyse de E. Amir et al. publiée dans le Journal of the
National Cancer Institute en 2011 (1) a comparé, sur
plus de 30 000 patientes, la toxicité relative des anti-
aromatases et du tamoxifène. Les maladies cardio-
vasculaires (OR = 1,26 ; IC95 : 1,10-1,43 ; p < 0,001)
et les fractures osseuses (OR = 1,47 ; IC95 : 1,34-1,61 ;
p < 0,001) ont augmenté avec les antiaromatases ; en
revanche, les thromboses veineuses (OR = 0,55 ; IC95 :
0,46-0,64 ; p < 0,001) et les cancers de l’endomètre
(OR = 0,34 ; IC95 : 0,22-0,53 ; p < 0,001) ont diminué
dans ce même bras. Ainsi, le traitement hormonal
prescrit doit rester conventionnel en dehors de
contre-indications ou de comorbidités spécifi ques.
Il a été rappelé qu’une radiothérapie adjuvante
ne se justifi ait pas chez les patientes présentant
des récepteurs hormonaux et porteuses de petites
tumeurs de moins de 2 cm. Le seul intérêt éventuel
réside dans une diminution signifi cative du risque
de rechute locale (2).
Des centres français se sont attachés à étudier
les prescriptions et le suivi des traitements chez
les patientes âgées présentant un cancer du sein
surexprimant HER2 en adjuvant ou néo-adjuvant :
102 malades, âgées en moyenne de 75,4 ans, ont été
incluses ; 62 % ont été traitées en néo-adjuvant ou en
adjuvant par du trastuzumab. Cependant, moins de
50 % des patientes traitées ont pu recevoir le proto-
cole dans son intégralité. Vingt-neuf pour cent des
patientes ont présenté une diminution d’au moins
10 % de la fraction d’éjection ventriculaire gauche.
Après un suivi de 33 mois, la médiane de survie
sans rechute n’était pas atteinte (Barthelemy P et al.,
abstr. 636).
Enfi n, ce congrès a été l’occasion de rappeler l’étude
ASTER du groupe GERICO, combinant un traitement
par hormonothérapie avec ou sans chimiothérapie
en adjuvant en fonction d’une évaluation génomique
chez les patientes RH+ de 70 ans et plus (Brain E
et al., abstr. TPS667).
Cancer colorectal
Dans la prise en charge du cancer colorectal en
situation adjuvante, le Dr N.A. Jackson McCleary a
insisté sur les raisons évidentes de la disparité des
prises en charge chez les patients âgés, survenant dès
le diagnostic, selon sa précocité et l’évaluation, se
poursuivant au moment de la décision thérapeutique

La Lettre du Cancérologue • Supplément 2 au vol. XXI - n° 6 - juin 2012 | 87
COMPTE-RENDU
ETANALYSE
Chicago 2012
qui prendra bien sûr en compte l’éloignement
géographique du patient, sa condition physique, le
jugement du thérapeute ainsi que la préférence du
patient et de sa famille. Enfi n, les risques de toxicité
du traitement, qui dépendent du statut fonctionnel
du patient, sont indéniables.
Le 5-FU (méta-analyse Sargent 2001), dont la tolé-
rance est tout à fait acceptable, en particulier dans
les études observationnelles, permet une réduction
de la mortalité de 24 % chez les patients âgés et de
l’ordre de 20 % chez les plus de 80 ans.
Depuis 2009 et la publication des résultats de
l’étude ACCENT (3), l’utilisation de l’oxaliplatine
en adjuvant chez les patients de plus de 70 ans est
fortement discutée. Ainsi, que ce soit dans l’étude
MOSAIC, la NSABP C-07 ou la N016968, la survie
globale à 5 ans n’est pas signifi cativement modifi ée
par l’association de l’oxaliplatine au 5-FU ou à la
capécitabine (4-6).
Une récente étude rétrospective du Dr N.A. Jackson
McCleary comparant 84 patients de plus de 75 ans
et 168 de moins de 75 ans, qui ont reçu du FOLFOX
en adjuvant et/ou métastatique, a montré que les
comorbidités et les polymédications étaient signifi -
cativement plus fréquentes dans le groupe personnes
âgées de plus de 75 ans, et qu’il y avait une dimi-
nution signifi cative de 20 % de l’administration du
traitement dans cette population. Enfi n, Sanoff,
dans une publication à venir, a analysé à partir des
données du SEER (Surveillance Epidemiology and
End Results), le cas de 4 226 malades de plus de
75 ans présentant un cancer colorectal de stade III
et traités par chimiothérapie (42 % des cas). Il a
constaté un bénéfi ce du traitement sur la survie,
similaire à celui obtenu dans les études cliniques ; en
revanche, le bénéfi ce est plus limité avec l’adjonction
d’oxaliplatine (7).
Ainsi, les recommandations en adjuvant sont, suite
à ce congrès :
➤
chimiothérapie pour les stades II par fluoro-
pyrimidines, qui améliorent la survie ;
➤
pas de bénéfi ce de survie avéré avec l’utilisation
de l’oxaliplatine.
Cancer du poumon
(Adjuvant Treatment of Older Patients with Lung
Cancer ; Educational book, Crawford J et al.)
Le cancer bronchique non à petites cellules est
fréquent puisqu’il concerne 2 patients âgés de 65 ans
et plus sur 3. L’âge médian au diagnostic est de
71 ans. En dehors des comorbidités qui s’accumulent
avec l’âge, la diminution de la fonction pulmonaire
est physiologique avec le vieillissement et bien sûr
majorée chez les fumeurs. La FEV1 perd 25 % entre
50 et 75 ans en moyenne chez les non-fumeurs et
plus au-delà de cet âge. Chez les fumeurs, ce déclin
peut atteindre 75 %, voire plus.
Grâce aux progrès des techniques chirurgicales moins
invasives, à une meilleure évaluation préopératoire
et à l’amélioration de l’accompagnement périopé-
ratoire, les stades précoces − quel que soit l’âge du
patient − bénéfi cient plus largement des indications
opératoires.
Une étude cas-contrôle, menée en France entre
2004 et 2008 auprès de 4 000 patientes âgées
dont la moitié avait 70 ans ou plus, a comparé les
indications chirurgicales (lobectomie et pneumo-
nectomie) et analysé la mortalité 30 et 90 jours
après l’opération (8). De cette analyse, il résulte
que le nombre d’actes chirurgicaux est sensiblement
le même chez les patients âgés et chez les plus
jeunes. La mortalité, qui reste inférieure, est signi-
fi cativement plus importante chez les personnes
âgées à 90 jours.
L’analyse poolée LACE (Lung Adjuvant Cisplatine
Evaluation) a rapporté une amélioration de la
survie de plus de 10 % grâce à la chimiothérapie
adjuvante (9). L’analyse du sous-groupe âgé de
l’étude JBR.10 (cisplatine-vinorelbine versus témoins)
permet de conclure que, même si les patients âgés
reçoivent des traitements incomplets, l’amélioration
de la survie est sensiblement équivalente à celle des
patients plus jeunes (10).
Ces études randomisées sélectionnant les popu-
lations âgées sont confortées par les données du
SEER (11). Parmi les 3 324 patients de 65 ans et
plus opérés d’un cancer bronchique non à petites
cellules de stade II ou IIIA, 21 % ont reçu une
chimiothérapie adjuvante à base de platine. Cette
chimiothérapie a amélioré la survie (HR = 0,78).
En revanche, les patients âgés de plus de 80 ans
n’en ont pas tiré le même bénéfice. Les patients
de cet observatoire recevaient du cisplatine ou du
carboplatine, sans différence majeure en termes
de survie. Le carboplatine est mieux toléré dans
cette population (11).
En conclusion, les patients âgés doivent profi ter des
traitements adjuvants lorsqu’ils sont réalisables,
ainsi que l’a indiqué le Dr Hurria. Ceci suppose une
bonne évaluation de la population concernée, du
bénéfi ce attendu du traitement, du risque induit
par les toxicités et, enfin, des soins de support
adaptés en périthérapeutique (avant et après les
traitements).

88 | La Lettre du Cancérologue • Supplément 2 au vol. XXI - n° 6 - juin 2012
Recherche avancée etappliquée chez le sujet âgé
COMPTE-RENDU
ETANALYSE
Chicago 2012
Maladie métastatique :
vers des schémas individualisés
(Considerations and Controversies in the Mana-
gement of Older Patients with Advanced Cancer ;
Educational book, Mohile SG et al.)
L’efficacité du traitement peut être compromise
par la crainte des toxicités, ainsi que l’a rappelé
le Dr Klepin dès l’introduction de sa présenta-
tion. Les recommandations des sociétés savantes
ne conseillent pas l’adaptation de dose chez les
patients âgés “en forme” lors de la première ligne
de chimiothérapie dans la maladie métastatique.
Une étude récente s’est attachée à randomiser
459 patients âgés atteints d’un cancer colorectal
métastatique, considérés comme fragiles par leur
médecin et ne pouvant pas bénéficier d’emblée des
doses standard de chimiothérapie. Ils ont reçu soit
du 5-FU i.v., soit du 5-FU et de l’oxaliplatine, soit
de la capécitabine, soit enfin de la capécitabine
et de l’oxaliplatine (étude FOCUS 2). Le traite-
ment était instauré à 80 % de la dose standard
dans les 6 premières semaines puis était porté à
pleine dose si la tolérance était satisfaisante. L’âge
médian était de 74 ans ; 13 % des patients avaient
plus de 80 ans. Après 12 semaines de traitement,
seuls 14 % ont accédé aux doses standard, 33 %
ont poursuivi à la dose adaptée initiale et 49 %
ont eu une diminution de dose. Les objectifs de
l’étude comprenaient la survie sans progression
(SSP) et la qualité de vie. Un nouvel objectif était
également étudié : un critère composite associant
la progression, les toxicités et leurs effets néga-
tifs. L’oxaliplatine a montré un bénéfice en SSP
non significatif (5,8 versus 4,5 mois ; p = 0,07)
et l’absence de surcroît de toxicité ; en revanche,
Cancer digestif
»
Lorenzen S et al., abstr. 4080 : faisabilité en pério-
pératoire d’une chimiothérapie par FOLFOX avec ou
sans docétaxel chez les patients âgés avec un cancer
œsogastrique localement avancé.
»
Ko JJ et al., abstr. 6014 : chimiothérapie adjuvante
et interruption précoce chez des patients âgés avec un
cancer du côlon de stade III.
»
Chan M et al., abstr. 6018 : chimiothérapie palliative
et thérapies ciblées chez les patients âgés avec un cancer
colorectal métastatique.
Cancer du sein
»
Brain E et al., abstr. TPS667 : présentation de l’étude
ASTER 70s (phase III GERICO).
»
Pritchard KI et al., abstr. 551 : tolérance de l’évéro-
limus chez les patientes de 65 ans et plus atteintes d’un
cancer du sein avancé. Suivi de BOLERO-2.
»
Barthelemy P et al., abstr. 636 : étude rétrospective
multicentrique française portant sur le traitement adju-
vant dans les stades précoces de cancer du sein chez les
patientes âgées.
»
Chavez-Mac Gregor M et al., abstr. 600 : cardiotoxi-
cité du trastuzumab chez les patientes âgées ayant un
cancer du sein.
»
Yao K et al., abstr. 1033 : radiothérapie après curage
axillaire chez les patientes de 70 ans et plus.
»
Pearlstone DB et al., abstr. 1132 : cancer du sein de
la femme âgée.
»
Klepin HD et al., abstr. 6015 : comorbidités, chimio-
toxicité et devenir des femmes âgées traitées par chimio-
thérapie adjuvante pour un cancer du sein.
Tumeur cérébrale
»
Fawole AA et al., abstr. 2093 : glioblastome de bas
grade.
»
Perry JR et al., abstr. TPS2104 : étude de phase III
randomisant un cycle court de radiothérapie avec ou
sans traitement concomitant par témozolomide en
adjuvant chez les patients âgés avec glioblastome
(NCIC CTG CE.6, EORTC 26062-22061, TROG 08.02,
NCT00482677).
»
Tabatabai G et al., abstr. TPS2105 : bévacizumab et
radiothérapie chez les patients âgés avec glioblastome
(ARTE).
Sarcome
»
Garbay Decoopman D et al., abstr. 10057 : sarcome
avancé des tissus mous chez le patient âgé de 75 ans et
plus.
»
Hong Hui Quek R et al., abstr. 10051 : sarcome de
haut grade des tissus mous.
ORL
»
Carballido EM et al., abstr. 5564 ; Moye VA et al.,
abstr. 5577 : impact de l’âge dans la prise en charge des
cancers de la tête et du cou.
Poumon
»Okamoto H et al., abstr. 7017 : phase III comparant
radiothérapie avec ou sans carboplatine chez les patients
atteints de cancer non à petites cellules localement
avancé.
»Gridelli C et al., abstr. 7550 : phase II randomisée en
double aveugle, comparant gemcitabine avec et sans
vandétanib (étude ZELIG).
»
Dy GK et al., abstr. 7555 : N0821 – phase II asso-
ciant pémétrexed, carboplatine et bévacizumab chez
les patients âgés avec PS < 2.
»
Narumi S et al., abstr. 7563 : géfi tinib en première
ligne chez les patients âgés atteints de cancer non à
petites cellules.
»
Sugawara S et al., abstr. 7565 : NJLCG 0801 − phase II
randomisée comparant carboplatine et paclitaxel hebdo-
madaire versus docétaxel seul chez les patients atteints
de cancer non à petites cellules.
»
Socinski MA et al., abstr. 7590 : nab-paclitaxel hebdo-
madaire en association avec carboplatine en première
ligne.
»
Hesketh PJ et al., abstr. 7570 : analyses des études
SWOG de 1993 à 2008.
Marqueurs biologiques et génomiques
»
Falandry C et al., abstr. 9011 : corrélation entre les
télomères courts et la vulnérabilité, les toxicités et les
décès précoces chez les patientes âgées traitées par
carboplatine pour un cancer avancé de l’ovaire.
»Wick W et al., abstr. 2000 : MGMT, promoteur de la
méthylation, biomarqueur de la réponse à la radiothérapie
versus la chimiothérapie dans les astrocytomes malins
du sujet âgé.
Évaluation gériatrique
»
Hamaker M et al., abstr. 1080 : étude OMEGA – EGS
et cancer du sein.
»
Soubeyran PL et al., abstr. 9012 : facteurs pronos-
tiques de perte d’autonomie.
»
Decoster L et al., abstr. 9035 : EGS et décision théra-
peutique.
»
Extermann M et al., abstr. 6100 : EGS et qualité
de vie.
»
De la Motte Rouge T et al., abstr. 6110 : déclin des
fonctions cognitives et décision thérapeutique.
»
Freyer G et al., abstr. 6112 : score gériatrique de
vulnérabilité.
Encart. Les posters par thématiques transversales.
 6
6
1
/
6
100%