L Les cancers du rein, du testicule, de la vessie T

T umeurs urologiques
Tumeurs Urologiques
402
La Lettre du Cancérologue - Vol. XV - n° 7 - décembre 2006
Les cancers du rein, du testicule, de la vessie
et de la verge
Renal, testicular, urothelial and penile carcinomas
$P. Beuzeboc*
L
a confirmation de la révolution apportée par les traite-
ments antiangiogéniques dans les cancers du rein méta-
statiques a été l’élément dominant de cette année 2006,
couronnée par l’autorisation de mise sur le marché (AMM)
accordée au sunitinib et au sorafenib. Elle ouvre enfin des pers-
pectives nouvelles dans cette tumeur jusqu’à présent réfractaire
aux traitements médicaux. Il faut aussi insister sur les deux
essais négatifs d’intensification terminale dans les tumeurs
germinales. La roue tourne, une ère nouvelle s’annonce, alors
qu’une autre s’étiole…
CANCER DU REIN
Biologie
Rôle d’HIF (Hypoxia-Inducible Factor)-1
α
et HIF-2
α
dans
la régulation des gènes cibles d’HIF en réponse à l’hypoxie, de
l’IGF-1 et de la perte de la fonction VHL (Von Hippel-Lindau)
Dans les cancers du rein, les cellules tumorales expriment des
taux de base élevés d’HIF-1α et d’HIF-2α liés à la perte de la
fonction VHL, ce qui conduit à une “up regulation” de gènes
impliqués dans la prolifération et l’angiogenèse. V.A. Carroll
et al. (1) ont montré que, dans des modèles expérimentaux, le
niveau d’expression de base élevé du VEGF (vascular endothelial
growth factor), du glucose transporter 1, de l’UPA-R (urokinase-
type plasminogen activator receptor) et de PAI-1 (plasminogen
activator inhibitor-1) dépendait surtout d’HIF-2α. Ils ont identifié
une petite molécule inhibitrice d’HIF-1α, appelée NSC-134754,
capable également de diminuer significativement l’expression
d’HIF-2α et les niveaux de VEGF régulés par HIF-2α.
Cela pourrait ouvrir la voie à de nouvelles thérapeutiques ciblant
les voies HIF.
Différents profils d’expression d’ARNm de VEGF, de
VEGFR1 et de VEGFR2 dans les carcinomes à cellules
claires et les carcinomes papillaires
À partir d’ARN de 84 carcinomes à cellules claires (cRCC),
de 20 carcinomes papillaires (pRCC), de 6 carcinomes chro-
mophobes et de 27 tissus rénaux normaux, B.J. Ljundberg et
al. (2) ont montré des niveaux d’expression de VEGF, VEGFR1 et
VEGFR2 plus élevés dans les tumeurs que dans le tissu normal.
Dans les cancers du rein, les niveaux de VEGF étaient supérieurs
dans les cRCC par rapport aux pRCC. Dans les cRCC, les niveaux
de VEGFR2 étaient plus élevés dans les stades I-II que dans les
stades plus avancés. En revanche, dans les pRCC, les niveaux
de VEGF et de VEGFR2 étaient supérieurs dans les stades III
comparativement aux stades I-II. Les auteurs ont conclu que les
différents sous-types de carcinomes rénaux avaient différents
profils d’expression de VEGF et de VEGFR et qu’une meilleure
connaissance des différentes voies régulant l’angiogenèse dans
ces tumeurs devrait permettre de mieux adapter les indications
des traitements antiangiogéniques…
Expression d’Ets-1 dans les carcinomes à cellules claires :
implications dans l’angiogenèse
Ets-1 est l’une des molécules cibles du VEGF. S. Mikami et al. (3)
ont étudié l’expression d’Ets-1 et de VEGF en immunohisto-
chimie (IHC) et en RT-PCR ainsi que leurs corrélations avec
la densité des microvaisseaux. Ils ont pu montrer que l’expres-
sion d’Ets-1 en IHC et la densité des microvaisseaux étaient
plus élevées dans les carcinomes à cellules claires que dans les
carcinomes papillaires. L’expression prédominante de l’ARNm
d’Ets-1 dans les carcinomes à cellules claires a été confirmée
par RT-PCR. Elle était corrélée à la densité des microvaisseaux.
Ces résultats suggèrent qu’Ets-1 peut être impliquée dans l’angio-
genèse des cancers du rein à cellules claires.
Taux élevé de survivine facteur de mauvais pronostic
des cancers du rein localisés opérés
L’équipe de la Mayo Clinic (4), dans une étude multiparamétrique
portant sur 312 patients opérés entre 1990 et 1994, a montré
que des niveaux élevés d’expression de la survivine sont un
facteur de mauvais pronostic indépendant. Dans cette cohorte,
97 patients (31,1 %) avaient des niveaux élevés de cette protéine
en IHC. Les taux de survie spécifique à 5 ans étaient de 43 % en
cas d’expression élevée versus 87,2 %. L’expression de la survivine
s’est révélée être un facteur indépendant associé à la progression
tumorale (RR = 3,9 ; IC95 : 2,4-6,2).
Traitements des formes localisées
Chirurgie conservatrice
M. Carini et al. (5) ont rapporté l’expérience d’une simple
énucléation de tumeurs mesurant entre 4 et 7 cm de diamètre.
Dans cette étude rétrospective de 71 tumeurs traitées entre 1986
* Département d’oncologie médicale, institut Curie, Paris.
LK7-1106.indd 402 22/12/06 17:25:07

T umeurs urologiques
Tumeurs Urologiques
403
La Lettre du Cancérologue - Vol. XV - n° 7 - décembre 2006
et 2004, sans suspicion d’atteinte ganglionnaire sur le bilan
préopératoire, avec un suivi moyen de 74 mois, les médianes
de survie spécifique à 5 et 8 ans étaient respectivement de
85,1 % et de 81,6 %. Sur les 10 patients en rechute (14,9%),
3 présentaient une récidive locale (4,5 %). Les auteurs ont
conclu que, dans le contexte d’une chirurgie de préservation
néphronique, la simple énucléation peut représenter une
approche utile et acceptable.
Les néphrectomies partielles peuvent être réalisées par laparoscopie
avec une bonne sécurité et un bon résultat thérapeutique comme
l’ont montré les nombreuses expériences publiées par E. Heinrich
et al. (6), A.H. Wille et al. (7), A. Moinzadeh et al. (8), R.B. Nadler
et al. (9), y compris sur rein unique comme l’ont rapporté I.S. Gill
et al. (10) et A.F. Fergany et al. (11), ou dans certaines tumeurs
centrales comme l’ont démontré I. Frank et al. (12).
Traitement conservateur par cryothérapie et radio-
fréquence
A. Mejean et al. (13) ont fait le point sur leurs indications limi-
tées aux tumeurs exophytiques, de moins de 4 cm, situées à
distance du hile et des structures gastro-intestinales, chez des
patients âgés de plus de 70 ans ou dans un contexte de carci-
nome rénal héréditaire (maladie de von Hippel-Lindau) déjà
opéré. S’il existe des résultats encourageants dans les premières
séries, les données contradictoires concernant la radiofréquence
sont probablement dues à l’hétérogénéité des équipements.
Le taux de complications est faible. Un PHRC est actuellement
en cours en France pour comparer les résultats oncologiques
et fonctionnels de la radiofréquence et ceux de la chirurgie
conservatrice.
B.F. Schwartz et al. (14) ont rapporté une morbidité minimale
de l’analyse rétrospective de 85 patients consécutifs traités entre
2001 et 2005 par cryothérapie pour des tumeurs périphériques
de petite taille (médiane : 2,6 cm ; extrêmes : (1,2-4,7 cm).
La durée moyenne d’hospitalisation a été de 3 jours (2,2 jours en
cas de laparoscopie), 7 conversions de laparoscopie en chirurgie
ouverte ont été nécessaires. La perte sanguine moyenne a été
estimée à 58 ml. Le recul n’est pas suffisant pour conclure en
termes de résultats thérapeutiques.
Cancer du rein avec thrombus de la veine cave inférieu-
re remontant au-dessus des veines sus-hépatiques : CEC
avec “accès minimal” versus sternotomie ?
À partir de l’expérience de la Mayo Clinic sur 50 néphrectomies
avec thrombectomies de la veine cave inférieure (28 par un
accès minimal, 22 cas par sternotomie), Wotkowicz et al. (15)
recommande “l’accès minimal” qui permet une chirurgie plus
rapide, une réduction de la durée d’hospitalisation, moins de
transfusions et de recours à la ventilation assistée.
Pronostic
Réévaluation du stade TNM ?
Les résultats en termes de récidive et de survie sont équiva-
lents pour les tumeurs T1N0M0 et T3aN0M0 dans l’étude
de la Colombia University Surgical Urological Oncology
database (16).
La classification T3a (tumeurs à extension au-delà de la capsule
rénale, envahissant la graisse) n’a pas de limitation de taille.
Dans cette série, les survies sans récidive à 5 ans des tumeurs
T1N0M0 et des tumeurs T3N0M0 étaient comparables, respec-
tivement de 95,2 % et 90,6 % (p = 0,922).
Mauvaise prédiction de récidive du nomogramme post-
opératoire de Kattan dans une population de patients
français
L’équipe de Necker (17) a appliqué ce nomogramme sur une
série de 844 patients traités entre 1985 et 2000 (565 inclus).
L’index de concordance pour la survie sans récidive était seule-
ment de 0,607 (IC95 : 0,576-0,635).
Pronostic des tumeurs rénales des adultes jeunes
Les tumeurs sporadiques sont rares chez les sujets jeunes.
S. Siemer et al. (18) ont revu le devenir de 120 patients âgés
de 20 à 40 ans au diagnostic, sur 2 710 patients (4,4 %) traités
par néphrectomie entre 1975 et 2004. L’âge moyen était de
34,1 ans. Le taux de tumeurs confinées au rein était plus élevé
chez les patients jeunes (73,6 % versus 59,3 %, p < 0,05).
Les caractéristiques histopathologiques, la taille tumorale, les
atteintes ganglionnaires ne différaient pas significativement
entre les sujets jeunes et les sujets plus âgés. Les femmes avaient
significativement plus de lésions bénignes (41 % versus 20 %,
p < 0,05). La survie spécifique à 10 ans était de 78 % chez les
jeunes versus 68 % chez les plus âgés (p = 0,22).
Seconds cancers associés avec les différents sous-types
histologiques
À partir des données d’une série de la Mayo Clinic (19) de
2722 tumeurs (80,4 % de carcinomes à cellules claires, 13,9 % de
carcinomes papillaires, 4,7 % de carcinomes chromophobes), il a
été retrouvé un risque significativement plus élevé de deuxième
cancer (p < 0,001), notamment du côlon (p = 0,041) et de la
prostate (p = 0,003) en cas de cancer papillaire, ce qui pourrait
avoir à l’avenir des implications dans leur surveillance.
Prédire la survie à partir du moment de la récidive
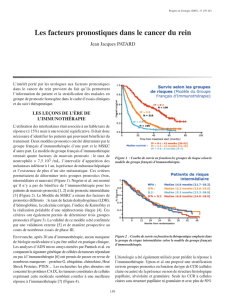
L’équipe du Memorial Sloan Kettering Cancer Center (MSKCC)
de New York (20), en appliquant le score pronostique de
Motzer développé dans les formes métastatiques (de 0 à
5 points, calculé à partir de 5 variables : récidive < 12 mois
après la néphrectomie, calcémie > 10 mg/dl, hémoglobine
inférieure à la normale, LDH > 1,5 N, IK < 80 %) a montré que
la médiane de survie globale dépendait fortement du groupe
pronostique : 76 mois pour les tumeurs de bon pronostic
(score = 0), 25 mois pour celles de pronostic intermédiaire
(score = 1 et 2), et 6 mois pour celles de mauvais pronostic
(score 3 à 5). Les taux de survie à 2 ans étaient respectivement
de 88 % (IC
95
: 77 % à 99 %), de 51 % (IC
95
: 37 % à 65 %) et de
11 % (IC
95
: 0 % à 24 %). Ces données sont importantes pour
stratifier les patients dans les essais thérapeutiques.
LK7-1106.indd 403 22/12/06 17:25:11

T umeurs urologiques
Tumeurs Urologiques
404
La Lettre du Cancérologue - Vol. XV - n° 7 - décembre 2006
TRAITEMENTS ANTIANGIOGÉNIQUES : TROIS NOU-
VELLES DROGUES POUR COMBATTRE LE CANCER
DU REIN (21-23)
Le
sunitinib
(Sutent®) est un inhibiteur de tyrosine
kinase multicible, en particulier de VEGFR et de PDGFR
Études de phase II
R.J. Motzer et al. ont publié (24, 25) les résultats de deux études de
phase II regroupant 106 patients ayant un cancer du rein métasta-
tique en échec d’une immunothérapie avec le sunitinib à la dose de
50 mg/j 4 semaines sur 6. Le taux de réponses a été de 34 % (IC95 :
25 %-44 %) et la médiane de survie sans progression de 8,3 mois
(IC
95
: 7,8-14,5 mois). Les effets indésirables les plus fréquents
ont été l’asthénie (28 %) et les diarrhées (20 %). Les anomalies
biologiques les plus notables ont été les neutropénies (42 %), les
élévations de la lipasémie (28 %) et les anémies (26 %).
Efficacité du sunitinib après progression sous bévacizumab
B. Rini et al. (26) ont rapporté, dans une série de 61 patients en
progression dans les 3 mois d’un traitement par bévacizumab,
un taux de réponses objectives de 16 % avec une survie sans
progression de 24 semaines.
Résultats de l’étude de phase III versus interféron
α
en
première ligne présentés en session orale à l’ASCO 2006
Au vu de ce qu’ont été les résultats des deux études en deuxième ligne
après immunothérapie, il était logique de les comparer en première
ligne à l’interféron α. Cette vaste étude ouverte, multicentrique
et internationale de phase III (27) a randomisé, entre août 2004
et octobre 2005, 750 patients, stratifiés en fonction du taux de
LDH, du statut de performance (ECOG : 0-1), de l’existence d’une
néphrectomie ou non. Dans le bras A, le sunitinib (375 patients)
était adminidtré à la dose de 50 mg/j pendant 4 semaines suivies
de 2 semaines de repos ; dans le bras B (375 patients), les patients
recevaient des injections sous-cutanées d’interféron α à doses crois-
santes : 3000000 UI la première semaine, 6000000 UI la deuxième
et 9000000 UI ensuite. Les traitements étaient continués jusqu’à
progression. Le taux de réponses objectives globales évalué par les
investigateurs a été de 37 % (137/374) pour le sunitinib et de 9 %
(33/373) pour l’interféron (p < 0,000001). L’évaluation centralisée
indépendante retrouvait un taux de réponses respectivement de
31 % (103/335) et de 6 % (20/327). La médiane de survie sans
progression était très significativement meilleure dans le groupe
sunitinib : 11 mois versus 5 mois (HR = 0,415 ; IC
95
: 0,320-0,539)
et ce, indépendamment des facteurs analysés (néphrectomie anté-
rieure, ECOG 0-1, taux de LDH, intervalle/diagnostic initial, taux
d’hémoglobine, calcémie corrigée, etc.). Le suivi est encore trop
court pour disposer des données analysables en termes de survie
globale.
Données à long terme
Quelques réponses de longue durée viennent d’être rapportées
(28), mais il n’y a pas de données à long terme tangibles et l’on
ne sait pas s’il y aura, comme avec les immunothérapies, une
obtention de rémissions durables.
Le sorafenib (Nexavar®) :
également un inhibiteur de VEGFR
Étude après une période de traitement de 12 semaines
randomisant les patients non progressifs entre une pour-
suite du traitement par sorafenib à la dose de 400 mg x 2/j
et un placebo
Cette étude (29) a prouvé l’efficacité du sorafenib en montrant
une différence significative en termes de survie sans progression
24 semaines versus 12 semaines.
Données en survie globale de l’étude de phase III
(TARGET) indisponibles à l’ASCO
Cela ouvre la voie à des protocoles de traitements adjuvants
pour le sunitinib et le sorafenib.
Le bévacizumab (Avastin®)
Résultats prometteurs pour l’association bévacizumab +
erlotinib
L’association de bévacizumab (10 mg/kg/15 j i.v.) et d’erlotinib
150 mg/j p.o. a permis d’obtenir un taux de réponses objec-
tives de 25 % (15 patients sur 59 évaluables dans une étude de
phase II). De plus, 61 % des patients ont présenté une stabilisation
de leur maladie après 8 semaines de traitement. La médiane
de survie était de 11 mois et la survie sans progression à un an
était de 43 % (30).
Un intrus : le temsirolimus, inhibiteur de mTOR
Avantage en survie montré dans une étude de phase III
comparant 3 bras : le temsirolimus seul, l’interféron et l’as-
sociation des deux chez des patients à mauvais pronostic
Le temsirolimus (TEMSR, CCI-779) est un inhibiteur spéci-
fique de mTOR, une protéine impliquée dans la croissance et
la survie des cellules tumorales. Dans une étude de phase II de
111 patients lourdement traités, le TEMSR présentait un taux
de réponses de 7 % (17 % de stabilisation) avec une médiane de
temps jusqu’à progression de 5,8 mois.
Cette étude de phase III (31) concernait des patients métastatiques
de mauvais pronostic selon les critères de Motzer. Les patients
devaient présenter au moins 3 des 6 critères suivants : inter-
valle < 1 an, index de Karnofsky (IK) 60-70, taux d’hémoglobine
anormal, calcémie corrigée > 10 mg/dl, LDH > 1,5 N, plus d’un
site métastatique. Six cent vingt-six patients ont été inclus, avec
une double stratification en fonction de la zone géographique et
de l’existence ou non d’une néphrectomie antérieure.
Le traitement faisait appel soit à de l’interféron α seul en sous-
cutané à doses croissantes jusqu’à 18000000 UI x 3/sem., soit à du
TEMSR 25 mg i.v. hebdomadaire, soit à la combinaison d’interféron
à la dose de 6000000 UI x 3/sem. et de TEMSR 15 mg/sem.
Le critère de jugement principal était l’amélioration de la survie
globale avec l’hypothèse d’une amélioration de 40 %, la médiane
de survie devant augmenter de 4,9 mois avec l’interféron à
6,9 mois.
Il apparaît que le TEMSR seul améliore significativement la
médiane de survie globale par rapport à l’interféron : 10,9 mois
(IC95 : 8,6-12,7) versus 7,3 mois (IC95 : 6,1-8,9), soit une amélio-
LK7-1106.indd 404 22/12/06 17:25:14

T umeurs urologiques
Tumeurs Urologiques
405
La Lettre du Cancérologue - Vol. XV - n° 7 - décembre 2006
ration de 49 % (HR = 0,73, 0,57-0,92 ; p = 0,0069). En revanche,
l’association de TEMSR et d’interféron ne fait pas mieux que
l’interféron seul (HR = 0,95 ; IC95 : 0,76-1,2).
Autres traitements des formes métastatiques
Étude de phase II randomisée de thalidomide
Cette étude comparant, chez 60 patients métastatiques après
une première ligne d’immunothérapie (ou non redevables d’une
immunothérapie), thalidomide et acétate de progestérone n’a
pas montré de différence significative entre les deux traite-
ments (32).
Étude de phase II du lenalidomide (33)
Le lenalidomide est un analogue structurel et fonctionnel
de la thalidomide présentant un meilleur profil de toxicité.
Dans une étude de phase II ouverte de 28 patients métasta-
tiques, traités à la dose de 25 mg/j pendant 21 jours sur 28,
seuls 3 patients (11 %) ont présenté une réponse objective et
étaient non progressifs à plus de 15 mois, et 11 (39 %) sont
restés stables pendant plus de 3 mois. Les principaux effets
indésirables ont été la fatigue (11 %), les toxicités cutanées
(11 %) et les neutropénies (36 %).
Chirurgie des métastases surrénaliennes
A. Antonelli (34) a rapporté l’expérience unicentrique de
45 patients (sur une population de 1179 patients traités entre
1987 et 2003). Sur les 17 patients présentant des métastases
surrénaliennes isolées (14 synchrones, 13 métachrones), 10 ont
eu une survie très prolongée (83 mois en moyenne).
Radiothérapie dans la prise en charge des métastases
cérébrales
Les métastases cérébrales des cancers du rein sont responsa-
bles d’une morbidité et d’une mortalité significative. Une revue
générale (35) a fait le point sur les progrès, dans le domaine de
la radiochirurgie stéréotaxique et de la radiothérapie hypofrac-
tionnée, des drogues radiosensibilantes et sur la nécessité de
nouvelles approches thérapeutiques plus efficaces combinées
à la radiothérapie.
Radiothérapie courte dans les compressions médullaires
Les résultats d’une étude multicentrique rétrospective alle-
mande (36) ont montré qu’une radiothérapie courte (1x8Gy
ou 5 x 4 Gy) semble aussi active qu’une radiothérapie plus étalée
(10 x 3 Gy ou 15 x 2,5 Gy ou 20 x 2 Gy), et suggèrent comme
choix la pratique de 1 x 8 Gy.
Immunothérapie adoptive par transplantation allo-
génique non myéloablative
Les résultats de l’étude de phase II intergroupe du CALGB
(37) d’allogreffe non myéloablative utilisant un conditionne-
ment par fludarabine et cyclophasphamide chez 22 patients de
14 institutions présentant un cancer du rein métastatique ont
été présentés. Plus de 90 % de chimérisme avec les cellules T
du donneur ont été constatés chez 17 des 19 patients évaluables
(89 %) avant 120 jours. Une GVH a été observée chez 11 patients
(50 %). Les résultats sont très décevants avec aucune réponse
objective, une médiane de survie de 5,5 mois et un temps jusqu’à
progression de 3 mois.
Cas cliniques particuliers
Prévalence des cancers du rein chez les patients en insuf-
fisance rénale terminale en attente de greffe
Dans une série de 852 patients consécutifs entre 1994 et 2000
de l’University of Mississipi Medical Center (38), 14 ont présenté
un carcinome rénal, soit une prévalence de 1,64 %. Ce taux élevé
justifie le screening systématique chez ces patients.
Cancer sur rein natif chez des transplantés rénaux
Une étude rétrospective (39) portant sur 373 patients consécutifs
transplantés entre 1993 et 2004 a retrouvé 12 tumeurs sur rein
natif chez 10 patients (5 cancers à cellules claires, 7 papillaires)
lors d’examens de surveillance. La taille moyenne était de 21 mm,
la moitié était de grade 3 de Fuhrman. Un seul patient est décédé
d’une évolution métastatique 6 ans après le diagnostic, un autre
a présenté une rechute locale.
Les auteurs conseillent, compte tenu du risque existant, une
surveillance annuelle du rein natif.
Cet article a fait l’objet de commentaires par AA. Petrolla et
G.T. Maclennan dans le Journal of Urology (40).
Tumeurs rares
Dans un cas d’angiosarcome métastatique du rein, l’associa-
tion d’anthracycline et d’ifosfamide s’est montrée totalement
inefficace (41).
Les tumeurs carcinoïdes primitives du rein sont très rares
(39 cas rapportés). W.T. Lowrence et al. (42) ont publié un cas
traité par néphrectomie partielle réalisée sous laparoscopie.
Cancer médullaire et réponse au bortézomib : E.A. Ronnen
(43) a rapporté une réponse complète durable (se maintenant
après plus de 27 mois) chez un patient.
CANCER DU TESTICULE
Articles généraux
Une revue générale a fait le point, dans e Lancet (44), sur
les récents progrès observés dans la prise en charge des cancers
du testicule au cours des dernières années visant à adapter au
mieux l’agressivité thérapeutique à la sévérité du pronostic.
Signalons aussi la publication des recommandations du
Comité de cancérologie de l’Association française d’urologie
pour le suivi des tumeurs germinales du testicule (45).
Facteurs de risque. Épidémiologie. Pronostic
Facteurs de risque. Tabagisme de la mère et tumeurs
germinales du testicule ?
Des données antérieures avaient souligné de possibles liens entre
les cancers bronchiques chez les mères fumeuses et les tumeurs
germinales chez les fils, ce qui suggérait le possible rôle d’un taba-
•
•
LK7-1106.indd 405 22/12/06 17:25:18

T umeurs urologiques
Tumeurs Urologiques
406
La Lettre du Cancérologue - Vol. XV - n° 7 - décembre 2006
gisme passif. Dans une enquête du National Cancer Institute (NIH)
[46] à partir de l’étude de 754 patients et de 928 sujets contrôles,
mais aussi de 1086 mères de patients et de sujets contrôles, il
n’a pas été retrouvé de relation entre le tabagisme de la mère
(OR = 1,1 ; IC
95
: 0,9-1,3) ou celui du père (OR = 1,0 ; IC
95
= 0,8-
1,3) et le risque de survenue d’une tumeur germinale.
Épidémiologie : absence d’augmentation de l’incidence
des cancers du testicule chez les enfants
On savait que l’incidence du cancer du testicule augmentait dans
la population des adultes de race blanche aux États-Unis, mais
les données concernant les tumeurs prépubertaires manquaient.
Une enquête du SEER (Surveillance, Epidemiology and End
results) (47) menée entre 1973 et 2000 concernant les garçons
âgés de 0 à 14 ans de toutes races a retrouvé 131 cas, soit une
incidence annuelle de 1,6 cas par million de personnes (le plus
souvent des “Yolk Sac Tumors”, suivies par des tératomes). À
l’inverse des adultes, aucune tendance à une augmentation de
l’incidence n’a été identifiée.
Données épidémiologiques européennes d’incidence et de
mortalité (48)
Les données épidémiologiques concernant les incidences de
12 pays ont montré des taux variant de 1-2 % par an (Norvège)
à 6 % par an (Espagne, Slovénie) mais aussi une augmentation
constante de l’incidence dans tous les pays. En revanche, la
mortalité est en diminution de 3 à 6 % par an au cours des
années 1980 et 1990 dans les 22 pays étudiés, sauf en Roumanie
et en Bulgarie, où elle est stable, et en Croatie et au Portugal,
où elle a augmenté.
Mise à jour à partir d’une méta-analyse portant sur la
survie des tumeurs germinales non séminomateuses (TGNS)
selon la classification internationale de l’IGCC (49)
La classification de l’IGCC (International Germ Cell Consensus)
permet de distinguer les patients à bon pronostic de ceux à
pronostic intermédiaire, et de ceux à mauvais pronostic ; ils ont
respectivement des survies globales à 5 ans, fondées sur les résul-
tats de patients traités entre 1975 et 1990, de 92%, 80% et 48%.
D’après les résultats d’une méta-analyse incluant 10 publications
et concernant au total 1775 patients (1087, 232 et 465 respective-
ment de bon pronostic, de pronostic intermédiaire et de mauvais
pronostic) traités après 1989, les survies globales à 5 ans étaient
de 94%, 83 % et 71%, résultats qui témoignent d’une amélioration
des survies des formes à pronostic intermédiaire et surtout de
celles à mauvais pronostic. Cette amélioration est probablement
due à une meilleure expérience concernant la prise en charge de
ces formes et au développement de traitements plus efficaces.
Tumeurs de stade I
Séminome de stade I
À partir des données de l’essai MRC/EORTC, le débat, portant
sur l’intérêt potentiel d’une seule cure de carboplatine AUC 7, s’est
installé, alimentant plusieurs publications (50, 51). Le carboplatine
pourrait permettre, en théorie, de réduire le risque de séquelles
tardives, mais il faut insister surtout sur la réduction à 5 ans de
72 % du risque de cancer controlatéral par rapport à la radiothé-
rapie. Dans l’analyse de 1654 patients, seul un patient a présenté
une récidive survenant plus de 36 mois après le traitement.
Traitement adjuvant des TGNS de stade I
D.C. Gilbert et al. (52) ont reposé le problème de savoir s’il fallait
faire un ou deux cycles adjuvant de BEP (bléomycine, étoposide
et cisplatine) à partir de données anglaises du Royal Marsden sur
22 patients traités par un seul cycle. Aucun n’a rechuté. Il faut
néanmoins relever qu’il s’agissait de patients à risque modéré de
récidive. Les auteurs proposent une large étude multicentrique
randomisée comparativent un et deux cycles de BEP.
Tumeurs métastatiques
Prédiction de la présence de tératome dans la pièce de
curage ganglionnaire rétropéritonéal postchimiothérapie
Une étude du MSKCC de New York (53) portant sur 532 patients
ayant eu, entre 1989 et 2003, un curage rétropéritonéal post-
chimiothérapie pour une TGNS a montré la présence de lésions
tératomateuses chez 235 patients (44 %) et seulement du téra-
tome dans 210 cas (40 %). Des éléments tératomateux étaient
présents chez 42 % des patients sur la pièce d’orchidectomie. En
analyse multivariée, une Yolk Sac Tumor (p = 0,046), la présence
d’un tératome au niveau de l’orchidectomie (p < 0,005) et l’ab-
sence de nécessité d’une chimiothérapie de sauvetage (p = 0,03)
constituaient des facteurs prédictifs indépendants de la présence
de tératome dans le rétropéritoine.
Concernant le PET scan
Signalons la réédition de l’essai SEMPET (54) initialement
publié dans le Journal Clinical of Oncology en 2004.
Le PET scan n’a pas montré d’intérêt prédictif de récidive dans
les TGNS à haut risque dans l’étude T22 du MRC (55). Les tumeurs
de stade I à haut risque de rechutes sont caractérisées par la pré-
sence d’emboles vasculaires ou lymphatiques. Ce groupe présente
un taux de rechutes d’au moins 35 % à 40 % (plus de 50 % en cas
de carcinome embryonnaire majoritaire). La question posée par
l’étude du MRC était de savoir si un PET scan réalisé dans les
8 semaines après l’orchidectomie pouvait représenter une aide
à la détection d’une maladie occulte et à la décision de la mise
en route d’une chimiothérapie immédiate, ou si, au contraire,
on pouvait se contenter d’une surveillance. Sur 111 PET scan,
88 (79 %) se sont avérés négatifs. Avec un suivi médian de 11 mois,
33 rechutes sont survenues sur un total de 87 cas soumis à une
simple surveillance (1 patient traité par chimiothérapie) ce qui
montre clairement que le PET scan n’est pas capable d’identifier
précocement les patients qui vont récidiver.
La sensibilité du PET scan n’est pas suffisante pour évaluer
la viabilité des lésions résiduelles après chimiothérapie de
tumeurs germinales testiculaires et extragonadiques et pour
éviter leur exérèse chirurgicale, comme l’a montré une étude
multicentrique allemande (56) réalisée chez 140 patients
(20 séminomes, 109 TGNS, 11 sans histologie sur la tumeur
LK7-1106.indd 406 22/12/06 17:25:21
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%