Métastases pancréatiques TUMEURS MÉTASTATIQUES : TUMEURS MÉTASTATIQUES : situations particulières situations particulières

dossier
CANCER DU REIN :
les grands débats,
les grandes questions
Correspondances en Onco-Urologie - Vol. V - no 2 - avril-mai-juin 2014
6262
TUMEURS MÉTASTATIQUES : TUMEURS MÉTASTATIQUES : situations particulièressituations particulières
Métastases pancréatiques
D. Fuks*, B. Gayet*, A. Thiery-Vuillemin**, M.J. Paillard***
* Département de pathologies digestives, institut mutualiste Montsouris, Paris.
** Service d’oncologie, Inserm, UMR1098, CHUdeBesançon, et université de Franche-Comté. *** Service d’oncologie, CHU de Besançon.
Quand opérer ?
Les résections pour métastases pancréatiques
(MP) d’un cancer du rein représentent entre
0,25 et 3 % de l’ensemble des pancréatecto-
mies. Les MP sont le plus souvent asympto-
matiques et sont habituellement découvertes
au cours du suivi morphologique. Le délai
moyen entre la néphrectomie et l’appari-
tion de MP est d’environ 7 ans, mais il peut
être beaucoup plus long selon les caracté-
ristiques de la tumeur primitive. La spécifi -
cité diagnostique du scanner hélicoïdal est
élevée, rendant inutile la biopsie dirigée (1, 2).
L’IRM pancréatique pourrait permettre de
compléter le bilan d’extension locale dans
la mesure où la MP est unique dans seule-
ment 60 à 70 % des cas. Historiquement,
seule la chirurgie permettait d’obtenir des
survies prolongées, même si quelques cas
de patients ayant vécu longtemps sans avoir
été opérés ont été rapportés, ce qui laisse
supposer que certaines tumeurs rénales ont
une histoire naturelle favorable. Alors que,
dans la littérature, le taux de résécabilité
est élevé (80 %), les résultats à long terme
de la résection pancréatique ont été peu
étudiés (1, 3, 4). Une étude franco-belge
ayant inclus 62 patients réséqués pour MP
entre mai 1987 et juin 2003, dont les résultats
devraient être publiés prochainement, s’est
intéressée spécifi quement à la survie à long
terme de ces patients. Dans cette série, la
mortalité postopératoire était de 6,4 %. Après
un suivi médian de 91 mois (12-250) à la suite
de la pancréatectomie, 37 patients (60 %) ont
présenté une récidive. Après résection ité-
rative, la survie globale était de 52,6 mois
versus 11,2 mois chez les sujets non réséqués
(p = 0,019), la survie globale à 3, 5 et 10 ans
était de 72, 63 et 32 %, respectivement, et la
survie sans récidive à 3, 5 et 10 ans était de
54, 35 et 27 %, respectivement. En analyse
multivariée, les 2 facteurs pronostiques sont
la présence de métastases ganglionnaires
et de métastases extrapancréatiques avant
l’apparition de MP. Avec un taux de survie
globale de 32 % à 10 ans, les résultats de
cette étude confi rment l’intérêt d’une prise
en charge chirurgicale agressive dès que
les MP sont techniquement résécables (5).
Cependant, il est important de noter que
le traitement médical pour cancer du rein
métastatique a considérablement évolué au
cours des 5 dernières années (ITK, etc.) et que
les résultats de la chirurgie n’ont jamais été
analysés dans ce contexte.
En conclusion, même si la résection chirurgi-
cale reste à ce jour la meilleure option pour
améliorer la survie à long terme des patients
atteints de MP, les candidats à la chirurgie
doivent être soigneusement sélectionnés,
en raison de la mortalité postopératoire non
négligeable (6 %) et de l’absence d’étude
comparative avec le traitement médical.
Quand traiter médicalement ?
Épidémiologie
Les MP sont rares : elles représentent 2 à 11 %
des métastases issues d’un cancer du rein pri-
mitif. Du point de vue des masses pancréa-
tiques, les tumeurs malignes les plus fréquentes
restent les adénocarcinomes classiques du pan-
créas exocrine et les tumeurs neuroendocrines.
Les métastases issues d’autres tumeurs primi-
tives sont beaucoup plus rares. Toutefois, au
sein de celles-ci, les MP issues d’un cancer du
rein représentent 40 % des séries biopsiques
et 58 % des séries chirurgicales.
Iconographie
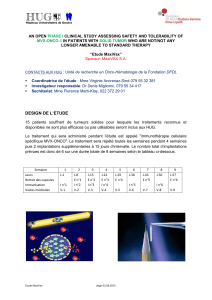
La qualité de l’imagerie avec injection de
produit de contraste est très importante, tout
comme le temps d’injection : un scanner avec
un temps artériel impératif puis portal est
le plus souvent suffi sant (fi gure 1A et B). Les
2 principaux diagnostics diff érentiels radio-
logiques sont les tumeurs neuroendocrines et
les malformations vasculaires. L’intrication des
images dans l’histoire clinique du patient est
donc essentielle. La réalisation d’une biopsie
dépend de sa faisabilité technique (du fait de
la localisation pancréatique) et de sa nécessité
au vu du dossier.
Traitement
La littérature s’intéressant aux thérapeutiques
spécifi ques de ce site métastatique particulier
est assez pauvre, avec de nombreuses petites
séries rétrospectives, le plus souvent mono-
centriques, et des case reports. La chirurgie
est à privilégier chez un patient mono- ou
oligométastatique, en fonction des critères
d’opérabilité (6). D’autres traitements, comme
la radiothérapie ou les ultrasons focalisés
de haute intensité (High Intensity Focused
Ultrasound [HIFU]), ont fait l’objet de quelques
publications ; la radiofréquence semble
délétère. Chez les patients non opérables ou
présentant des métastases nombreuses, les
thérapies ciblées (antiangiogéniques ou inhi-
biteurs de mTOR) peuvent être utilisées, avec
une effi cacité qui ne semble pas diff érer de
ce qui est observé pour les autres sites méta-
statiques, sinon, peut-être, une meilleure
survie sans progression (fi gure 2). En eff et,
diverses séries semblent poser la question
d’un pronostic global qui serait meilleur
pour les patients ayant des métastases pan-
créatiques – en témoignent la cohorte de
Médioni et al. ayant reçu du sunitinib (7), ainsi
que 2 présentations récemment proposées
à l’ASCO® GU 2014 (8, 9).
■
D.Fuks, B.Gayet et M.J.Paillard n’ont pas déclaré leurs
éventuels liens d’intérêts.
A.Thiery-Vuillemin déclare avoir des liens d’intérêts avec
Pfi zer, Novartis et Roche.

>> ILLUSTRATION CLINIQUE
page suivante
Correspondances en Onco-Urologie - Vol. V - no 2 - avril-mai-juin 2014
6363
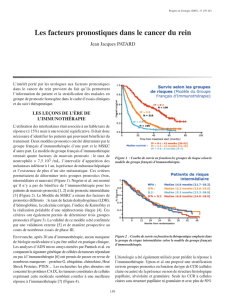
Figure 2
100
50
75
25
5 15 20 250 10 30 35
0
%
Médiane : 19,6 mois ; IC95 : 16,6-30,3
Survie globale
Survie sans progression
Courbes de SG et de SSP chez des patients atteints de MP issues d’un cancer du rein primitif et traités par sunitinib (7).
Figure 1
Patient souff rant d’un cancer du rein dont de nombreuses métastases touchent
le pancréas : scanner injecté au temps artériel.
A
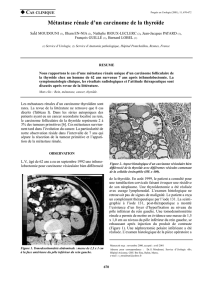
Figure 1
Même patient, scanner au temps portal.
Sous évérolimus, SSP de 22 mois.
B
Métastases pancréatiques
1. Law CH, Wei AC, Hanna SS et al. Pancreatic resection for
metastatic renal cell carcinoma: presentation, treatment, and
outcome. Ann Surg Oncol 2003;10(8):922-6.
2.
Hiotis SP, Klimstra DS, Conlon KC et al. Results after pan-
creatic resection for metastatic lesions. Ann Surg Oncol
2002;9(7):675-9.
3. Faure JP, Tuech JJ, Richer JP et al. Pancreatic metastasis of
renal cell carcinoma: presentation, treatment and survival.
J Urol 2001;165(1):20-2.
4.
Bassi C, Butturini G, Falconi M et al. High recurrence rate after
atypical resection for pancreatic metastases from renal cell car-
cinoma. Br J Surg 2003;90(5):555-9.
5. Schwarz L, Sauvanet A, Regenet N et al. Long-term survival
after pancreatic resection for renal cell carcinoma metastasis.
Ann Surg Oncol 2014 May 31[Epub ahead of print].
6. Ballarin R, Spaggiari M, Cautero N et al. Pancreatic metas-
tases from renal cell carcinoma: the state of the art. World
J Gastroenterol 2011;17(43):4747-56.
7. Medioni J, Choueiri TK, Zinzindohoué F et al. Response
of renal cell carcinoma pancreatic metastasis to sunitinib
treatment: a retrospective analysis. J Urol 2009;181(6):2470-5.
8. Kalra S, Atkinson BJ, Matrana MR et al. Prognosis of patients
with metastatic renal cell carcinoma and pancreatic meta-
stases. J Clin Oncol 2014;32(Suppl. 4): abstr. 527.
9.
Chanez B, Brachet PE, Laguerre B et al. Glandular metastasis
as a surrogate for long survivors in metastatic renal carcinoma.
J Clin Oncol 2014;32(Suppl. 4): abstr. 510.
Références

ILLUSTRATION CLINIQUE
dossier
CANCER DU REIN :
les grands débats,
les grandes questions
•
Patient âgé de 56ans
•
NEL droite en mai2009 : adénocarcinomeT3a, de grade2
•
Résection nodules péritonéaux (août2011) puis RFA sur nodule du poumon (octobre2011)
•
Mai 2012 : lésion pancréatique isolée
Patient consultant à l’IGR en mars 2008 :
TDM
PS0, biologie normale
Bilan d’extension : négatif
Quelle est votre attitude ?
Correspondances en Onco-Urologie - Vol. V - no 2 - avril-mai-juin 2014
6464
A
A B
B C
1
/
3
100%