E La chirurgie dans les MICI DOSSIER THÉMATIQUE

160 | La Lettre de l’Hépato-gastroentérologue • Vol. XVI - n° 4 - juillet-août 2013
DOSSIER THÉMATIQUE
Controverses dans les MICI
La chirurgie dans les MICI
E
n dépit des progrès récents des traitements
médicaux, la chirurgie est nécessaire chez
60 à 70 % des patients atteints de maladie
de Crohn (MC) et chez 20 à 30 % des malades
atteints de rectocolite hémorragique (RCH) [1]. La
prise en charge chirurgicale de ces pathologies est
complexe et a fait l’objet de recommandations pour
la pratique clinique européenne récente, émises
par l’European Crohn’s and Colitis Association
(ECCO) [2, 3].
Rectocolite hémorragique
Chirurgie en urgence : colite aiguë grave
◆Indications du traitement chirurgical
La survenue d’une colite aiguë grave (CAG) expose
les malades à un risque de complication chirur-
gicale de leur poussée : perforation (responsable
d’une péritonite ou d’abcès), hémorragie diges-
tive massive ou colectasie. L’apparition d’une telle
complication nécessite un traitement chirurgical
en urgence, avant tout traitement médical. En
dehors de ces formes chirurgicales d’emblée, la
chirurgie est discutée en cas d’échec du traite-
ment médical. Les recommandations de l’ECCO
proposent le recours à la chirurgie en cas d’échec
du traitement médical de deuxième ligne (ciclo-
sporine ou infliximab) [2].
Dans les CAG compliquées d’emblée, comme dans
les formes résistantes au traitement médical,
le traitement chirurgical de référence reste la
colectomie subtotale (CST) sans rétablissement
de la continuité digestive [2] avec iléostomie et
sigmoïdostomie. Cette intervention doit être,
idéalement, réalisée par laparoscopie, comme
le suggèrent les résultats d’une méta-analyse
récente [4].
Chirurgie élective
◆Indications
Le traitement chirurgical dans la RCH est indiqué
dans 3 situations principales : la RCH réfractaire au
traitement médical, la sténose colique et la RCH
compliquée de dysplasie et/ou de cancer.
RCH réfractaire au traitement médical
Les recommandations américaines
(5) proposent un
traitement chirurgical si les symptômes sont mal
contrôlés malgré un traitement médical optimisé
(notamment en cas de microcolie et de microrectie),
ou si le traitement médical expose le patient à des
complications, en particulier en cas de corticodé-
pendance, ou si les effets indésirables du traitement
médical sont mal tolérés.
Sténose colique sur RCH
Une sténose colique complique la RCH dans 5 à 10 %
des cas. L’apparition d’une sténose doit faire impé-
rativement suspecter une dégénérescence adéno-
carcinomateuse, dont la fréquence, très importante,
varie entre 25 et 30 % des cas [6]. Dans ce contexte,
l’indication du traitement chirurgical doit être large,
compte tenu du caractère souvent symptomatique
et, surtout, souvent complètement sténosant de la
pathologie, empêchant la surveillance endoscopique
du côlon d’amont (3).
RCH et cancer
Le cancer colorectal est une complication à long
terme bien établie des maladies infl ammatoires
chroniques de l’intestin (MICI). Une méta-analyse
a démontré que le risque cumulé de dégénérescence
chez les patients porteurs de RCH était respective-
ment de 2, 8 et 18 % après 10, 20 et 30 ans d’évo-
lution (7). Plusieurs facteurs de risque de dysplasie
et de cancer colorectal ont été démontrés dans la
Les bonnes indications
Good surgical indications in inflammatory bowel disease patients
Léon Maggiori*, Yves Panis*
* Service de chirurgie colorectale,
pôle des maladies de l’appareil digestif
(PMAD), hôpital Beaujon (AP-HP),
Clichy.
pour

La Lettre de l’Hépato-gastroentérologue • Vol. XVI - n° 4 - juillet-août 2013 | 161
Points forts
»
Dans la RCH, l’intervention de référence
est l’anastomose iléoanale.
»
Dans la maladie de Crohn (MC) iléale termi-
nale, la résection iléocolique est indiquée
principalement dans les formes sténosantes symp-
tomatiques et dans les formes perforantes.
»
Le traitement chirurgical de la MC colique est la
colectomie subtotale avec anastomose iléorectale.
»
La laparoscopie a clairement démontré son béné-
fice par rapport à la laparotomie.
»Si, dans un certain nombre d’études, la
chirurgie est considérée comme un événe-
ment indésirable grave ou un échec, son
recours reste très fréquent.
»
Pour un bon résultat, l’indication doit être bien
posée et la procédure réalisée adéquate.
»
En soulignant les mauvaises indications ou procé-
dures, les auteurs concluent sur la nécessité d’inté-
grer le chirurgien aux discussions thérapeutiques
lors des concertations pluridisciplinaires.
Mots-clés
Maladie de Crohn
Rectocolite
hémorragique
Chirurgie
Laparoscopie
Anastomose
iléorectale
Anastomose iléoanale
Highlights
»
In UC, the gold stan-
dard surgical treatment
is the restorative proc-
tocolectomy with ileal
pouch anal anastomosis
»
In small bowell Crohn's
disease, an ileocolic resec-
tion is indicated in symptom-
atic stricturing or perforating
localization.
»
Surgical treatment of colonic
Crohn's disease is subtotal
colectomy with ileorectal anas-
tomosis
»
Laparoscopy has demon-
strated its benefits over the
open approach for IBD surgical
management.
littérature : l’extension de la maladie (risque relatif
de 15 en cas de pancolite), la durée d’évolution de la
maladie (risque relatif de 5,7 à 10 ans), la présence
d’une cholangite sclérosante primitive (risque relatif
de 4,8), l’existence d’une infl ammation histologique
(risque relatif de 3) et les antécédents familiaux de
cancer colorectal (risque relatif de 2,5) [8].
En cas de dysplasie de haut grade sur muqueuse
plane, l’indication chirurgicale est formelle, puisqu’un
cancer sera retrouvé dans près de 1 cas sur 2 sur la
pièce opératoire (9). Une coloproctectomie totale
doit alors être réalisée (3). La prise en charge des
lésions de dysplasie de bas grade sur muqueuse
plane est plus controversée. Les recommandations
de l’ECCO proposent plutôt de réaliser un contrôle
endoscopique 3 à 6 mois après le diagnostic et de
réaliser une coloproctectomie si la lésion est alors
confi rmée (3).
Deux types de dysplasie sur lésion macroscopique
peuvent être distingués : les ALM (Adenoma-Like
Mass), qui présentent les critères morphologiques
des polypes sporadiques, et les DALM (Dysplasia-
Associated Lesion or Mass), qui correspondent à des
lésions au sein d’une muqueuse surélevée et infl am-
matoire. L’existence d’une DALM impose la réalisa-
tion d’une coloproctectomie totale, compte tenu
du risque important de cancer (9). Un traitement
conservateur, par résection endoscopique simple,
est proposé devant une ALM à condition que cette
résection soit complète et en l’absence de dysplasie
ailleurs sur le côlon (9).
◆Choix de l’intervention chirurgicale
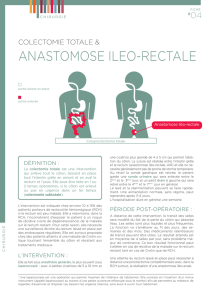
La coloproctectomie totale avec anastomose
iléoanale (AIA) est actuellement le traitement de
référence de la RCH, puisqu’elle permet de guérir
définitivement la maladie en permettant l’abla-
tion de l’ensemble de la muqueuse colorectale
à risque tout en conservant la fonction sphinc-
térienne (figure 1). Elle est réalisée chez plus de
80 % des patients opérés pour une RCH. Idéale-
ment, l’AIA est réalisée par laparoscopie, ce qui
permet une réduction de la morbidité postopé-
ratoire et du risque de stérilité par rapport à la
laparotomie (10, 11).
L’anastomose iléorectale (AIR) dans la RCH n’est
proposée que pour des patients rigoureusement sélec-
tionnés (3). Dans cette indication, l’intervention est
en effet discutable sur le plan théorique, puisque la
maladie touche le rectum dans tous les cas. Elle peut
cependant être envisagée si le rectum est conser-
vable (absence d’atteinte sévère et de microrectum),
sans dysplasie, et a fortiori sans cancer colorectal, sur
l’ensemble du cadre colique et du rectum.
»
If surgery is often
considered, in some
medical series about
Crohn’s disease and
ulcerative colitis, as a severe
adverse event or failure, it is
still very frequently useful.
»
To obtain a good result, the
indication must be good and
the right procedure must be
performed.
»
Emphasizing what is a
bad indication or an inappro-
priate procedure, the authors
conclude that the good
decisions must be taken in
consensus meetings between
surgeons and gastroenterol-
ogists.
pour contre
Keywords
Crohn's disease
Ulcerative colitis
Surgery
Laparoscopy
Ileorectal anastomosis
Ileal-pouch anal anastomosis
Figure 1. Anastomose iléoanale avec iléostomie latérale de protection : montage chirurgical.

162 | La Lettre de l’Hépato-gastroentérologue • Vol. XVI - n° 4 - juillet-août 2013
La chirurgie dans les MICI
DOSSIER THÉMATIQUE
Controverses dans les MICI
La décision de conservation rectale dans la RCH
va cependant nécessiter une surveillance à vie.
Toutefois, en cas d’évolution secondaire vers un
microrectum, ou devant l’apparition d’une dégé-
nérescence néoplasique, la transformation d’une
AIR en AIA reste possible.
Maladie de Crohn
Chirurgie en urgence
Les indications de chirurgie en urgence dans la MC
sont largement dominées par la CAG. Cette dernière
est moins fréquente dans la MC que dans la RCH
mais peut concerner 5 à 10 % des patients au cours
de l’évolution de leur maladie. Les modalités du
diagnostic et de la prise en charge sont exactement
identiques à celles décrites pour la RCH (2). Cette
attitude est d’autant plus logique que, en urgence,
la distinction entre MC et RCH n’est possible que
1 fois sur 2.
La MC de l’intestin grêle peut être à l’origine d’une
perforation intestinale en péritoine libre, respon-
sable d’une péritonite aiguë. Cette complication
est cependant rare, avec une prévalence rapportée
de 1 à 4 %. Son apparition relève d’une prise en
charge chirurgicale en urgence, dictée surtout par
la mauvaise tolérance du patient sur le plan général
(sepsis, choc).
Chirurgie élective
◆Atteintes de l’intestin grêle
Le grêle est l'organe le plus fréquemment atteint
dans la MC : 68 % des malades au moment du diag-
nostic initial (2). Dans près de 70 % des cas, elle ne
touche que la dernière anse iléale (6).
En ce qui concerne les formes sténosantes de la
MC, les recommandations de l’ECCO proposent
un traitement chirurgical dans 2 situations (2) : une
atteinte iléale terminale infl ammatoire, responsable
d’une symptomatologie occlusive (syndrome de
Koenig) ne cédant pas après un traitement médical,
ou une sténose de l’intestin grêle, symptomatique,
sans signe d’activité infl ammatoire (biologique ou
radiologique).
Les formes perforantes de la MC posent un problème
thérapeutique plus complexe. L’apparition d’un abcès
motive la réalisation d’un drainage percutané sous
guidage radiologique suivi d’un traitement par anti-
biothérapie. Le traitement chirurgical en urgence
sera réservé aux cas d’échec ou d’impossibilité de
ce drainage (2), la plupart des équipes proposant un
geste de résection emportant le segment digestif
“coupable” 4 à 6 semaines plus tard.
En cas de fi stule, les recommandations de l’ECCO
proposent un traitement chirurgical dans tous les
cas où la fi stule est symptomatique : diarrhée par
phénomène de “bypass”, fi stule entérocutanée inva-
lidante, fi stule entérovésicale (2). Si un traitement
chirurgical est envisagé, la problématique principale
est d’identifi er l’organe responsable, pour lequel une
résection devra être réalisée, et l’organe “victime”,
sur lequel une simple suture chirurgicale est suffi -
sante dans la majorité des cas (2).
Enfin, quel que soit le phénotype de la maladie
(sténosant ou perforant), la chirurgie est indiquée
dans les formes réfractaires au traitement médical.
L’indication chirurgicale doit être, dans ce contexte,
discutée au cas par cas et ne fait pas l’objet de
recommandations précises (2).
L’intervention consiste, dans la grande majorité des
cas, en une résection iléocolique emportant la valvule
iléocæcale (2). La voie d’abord laparoscopique est ici
aussi devenue la référence, puisqu’elle est associée
à une morbidité postopératoire plus faible que celle
de la laparotomie et à un taux de récidive à long
terme équivalent (10).
◆Atteintes colorectales
Indications chirurgicales
L’atteinte colique concerne près de 30 % des malades
atteints de MC (2). Les indications chirurgicales de la
MC colique concernent essentiellement les formes
réfractaires au traitement médical, les formes sténo-
santes symptomatiques et les formes compliquées
de dysplasie ou de cancer (fi gure 2).
MC colorectale réfractaire au traitement médical
Les recommandations américaines (5) proposent un
traitement chirurgical pour les MC colorectales après
échec du traitement médical. De la même façon
que dans la RCH, 3 situations sont retenues comme
des indications : lorsqu’il existe des symptômes mal
contrôlés après un traitement médical optimisé ;
lorsque le traitement médical à long terme expose
le patient à un risque élevé de complications liées à
ce traitement, en particulier en cas de corticodépen-
dance ; lorsque les effets indésirables du traitement
médical sont mal tolérés.
Formes sténosantes symptomatiques
Les formes sténosantes symptomatiques (respon-
sables d’un syndrome de Koenig) relèvent d’un
traitement chirurgical si l’atteinte résiste au trai-

La Lettre de l’Hépato-gastroentérologue • Vol. XVI - n° 4 - juillet-août 2013 | 163
DOSSIER THÉMATIQUE
tement médical ou si elle apparaît fi breuse et non
infl ammatoire sur les examens d’imagerie et, en
particulier, l’entéro-IRM (2).
Les sténoses coliques de MC doivent faire systéma-
tiquement rechercher une dégénérescence adéno-
carcinomateuse, moins fréquente que dans le cadre
d’une RCH, mais présente dans 7 % des cas (12).
Enfi n, les sténoses complètes empêchant la surveil-
lance endoscopique du côlon d’amont doivent être
opérées.
Choix de l’intervention
En cas d’atteinte colorectale dans le cadre d'une MC,
le traitement chirurgical de référence est la colec-
tomie totale avec AIR, qui doit être proposée dans
tous les cas où le rectum est sain ou peu malade
(rectite ou microrectum modérés) et en l’absence de
manifestations anopérinéales sévères (fi gure 3) [2].
En effet, cette intervention permet d’obtenir des
résultats fonctionnels à moyen et long terme satis-
faisants et va permettre de retarder l’éventuel recours
à une iléostomie terminale défi nitive.
Le consensus de l’ECCO propose de réaliser une colec-
tomie segmentaire, plutôt qu’une AIR, pour les MC
colorectales localisées avec atteinte limitée à moins de
Figure 3. Anastomose iléorectale : montage chirurgical.
Figure 2. Maladie de Crohn colorectale : algorithme décisionnel.
Maladie de Crohn
colorectale
Atteinte segmentaire
Pas d’atteinte
périnéale ou du grêle
Atcd d’atteinte
périnéale
ou du grêle
Pancolite
Rectum normal
ou peu atteint
Isolée Pluri-segmentaire
ou Atcd de pancolite
Microrectum
Colectomie segmentaire AIR AAP AIA
Atcd : antécédent ; AAP : amputation abdominopérinéale ; AIA : anastomose iléoanale ;
AIR : anastomose iléorectale.

164 | La Lettre de l’Hépato-gastroentérologue • Vol. XVI - n° 4 - juillet-août 2013
La chirurgie dans les MICI
DOSSIER THÉMATIQUE
Controverses dans les MICI
Les mauvaises indications
Wrong surgical indications in inflammatory bowel disease patients
Laurent Bresler*, Adeline Germain*
B
ien que la chirurgie soit considérée comme un
échec, voire un événement indésirable grave –
ou, pire, comme un “désastre” –, dans l’analyse
de certaines séries qui s’intéressent aux résultats des
traitements médicaux des maladies infl ammatoires
chroniques de l'intestin (MICI), elle reste fréquem-
ment indiquée et utile pour le patient, notamment
parce qu’elle seule peut guérir les patients porteurs
de rectocolite ulcéro-hémorragique. On estime à
l’heure actuelle que 60 à 70 % des patients atteints
de maladie de Crohn (MC) et 20 à 30 % des patients
atteints de rectocolite hémorragique (RCH) seront
opérés (1).
Malgré tout, sa morbidité propre à court et à long
terme nécessite qu’elle soit utilisée à bon escient,
et si un traitement médical moins délétère a les
mêmes chances de succès, il doit bien sûr être
privilégié. Par ailleurs, si la chirurgie est indiquée,
il faut que le geste chirurgical soit adéquat ; sinon,
on peut effectivement aboutir aux catastrophes
que stigmatisent volontiers nos collègues gastro-
entérologues.
Nous nous proposons dans cet article d’envisager
les indications chirurgicales dans le cadre de la RCH
et de la MC en urgence ainsi qu'en phase chronique,
et de détailler les situations où la chirurgie n’est pas
nécessaire (mauvaises indications) ou discutable
(indications discutables), et où les actes chirurgicaux
ne sont pas adaptés, alors qu’il y a potentiellement
une bonne indication opératoire (mauvaise procé-
dure).
Rectocolite ulcéro-
hémorragique
En urgence : colite aiguë grave
La colite aiguë grave a été défi nie par S.C. Truelove et
al. (15) en 1955 comme l’émission d’au moins 6 selles
sanglantes par jour, associée à une vitesse de sédi-
mentation (VS) > 30, à une température > 37,8 °C,
à un pouls > 90/mn, et à un taux d’hémoglobine
< 10,5 g/dl. Plus récemment, l’European Crohn’s
* Service de chirurgie digestive et
endocrinienne, pôle digestif, CHU
de Nancy.
contre
1/3 du côlon (2) afi n d’améliorer le résultat fonctionnel.
Enfi n, pour les patients porteurs de MC pancolique chez
qui le rectum n’est pas conservable, la réalisation d’une
coloproctectomie totale avec iléostomie défi nitive est
l’intervention classique. Nous-mêmes, puis d’autres
équipes, avons montré que l’AIA pouvait être envi-
sagée chez des patients sélectionnés sans antécédent
d’atteinte de l’intestin grêle ou de lésion anopérinéale,
en alternative à l’iléostomie défi nitive (13, 14).
Conclusion
La prise en charge chirurgicale des MICI est
complexe. Elle doit se concevoir en complément
du traitement médical plutôt qu’à sa place. Elle est
indiquée dans les formes résistantes au traitement
médical et les formes compliquées. La laparoscopie
représente aujourd’hui la voie d’abord préférée pour
toute la chirurgie des MICI, du fait de ses bénéfi ces
démontrés.
En cas de RCH, l’AIA avec réservoir en J est l’inter-
vention de référence, puisqu’elle permet d’atteindre
le double objectif de guérison de la maladie et de
conservation sphinctérienne.
En cas de MC du grêle, il est impératif de traiter
les lésions symptomatiques ou responsables de
complications en pratiquant la résection intestinale
la plus limitée possible. Pour ce faire, des gestes
de stricturoplastie peuvent parfois être proposés
en alternative à la résection de sténoses multiples.
En cas de MC colorectale, l’intervention de réfé-
rence est l’AIR. Le risque principal à long terme est
la perte de l’appareil sphinctérien, qui obligerait à
réaliser une iléostomie défi nitive. Ainsi, en cas de
MC colorectale avec rectum non conservable, l’AIA
peut être proposée chez des patients rigoureuse-
ment sélectionnés et bien informés, en alternative
à l’iléostomie défi nitive. ■
Les auteurs déclarent ne pas avoir de liens d’intérêts.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%