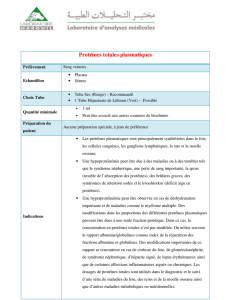
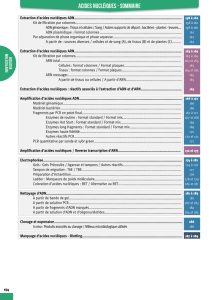
Electrophorèse sur gel de polyacrylamide-SDS Un exemple

Quelques images du TP
électrophorèse, chromatographie


Chromatographie des pigments
chlorophylliens
Fond de l’éprouvette avec solvant mobile
La tache verte ne touche pas le solvant
Cache opaque empêchant la photooxydation
des pigments
Bandelette de papier Whatmann
Sur laquelle on écrase un morceau de feuille

Résultats au bout de 15 minutes de migration
Chlorophylle b
Chlorophylle a
Xanthophylles
Carotènes

Gel de
cellulose sur
feuille
d’aluminium
Chromatographie des acides aminés: phase de dépôt
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%