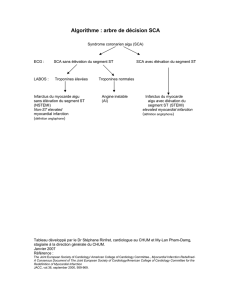
Le coronarien : du domicile à la coronarographie

Mise en page samu-de-france .com - 2002
Le coronarien : du domicile
à la coronarographie
P. Goldstein, N. Assez, V. Marel
Samu régional de Lille, CHRU, 59037 Lille cedex, France
SFAR 2001
POINTS ESSENTIELS
· La maladie coronarienne est la deuxième cause de mortalité en France. L'activité
cardiologique représente 20 à 40 % de l'activité des Smur en France dont plus de 25 % de
syndromes coronariens aigus.
· Le gain de survie est d'autant plus important que la reperfusion du myocarde est précoce
complète et durable. L'idéal est de pouvoir intervenir dans les deux heures suivant le début de
la douleur.
· Les traitements thrombolytiques par voie intraveineuse administrés dès la phase
préhospitalière permettent une réduction de mortalité de 15 % et un gain de temps de 50 min
par rapport à la thrombolyse intrahospitalière.
· Plus de 65 % des patients échappent à toute stratégie de reperfusion. L'alerte tardive est
l'élément pénalisant le plus marqué et concerne avec encore plus d'importance les sous-
populations de patients à risque.
· L'électrocardiogramme peut être normal ou atypique. Il doit impérativement interroger les
dérivations droites et être reproduit s'il est non parlant.
· Les marqueurs biologiques sont utilisables dès la phase préhospitalière. Ils peuvent apporter
une confirmation biologique en cas d'infarctus et ont une valeur pronostique pour les
syndromes coronariens aigus sans élévation du segment ST.
· La thrombolyse préhospitalière est une pratique scientifiquement validée et ne peut être
contestée dans le cadre des infarctus du myocarde. Cependant si le délai exact séparant prise
en charge initiale et réouverture de l'artère occluse par angioplastie est inférieur à une heure,
celle-ci peut être préférée.
· Thrombolyse et angioplastie ne sont pas des stratégies de reperfusion alternative mais des
stratégies complémentaires.
· Les héparines de bas poids moléculaire ont fait la preuve de leur supériorité sur l'héparine
non fractionnée dans le cadre de syndromes coronariens aigus sans augmentation du segment
ST.
· La stratification du risque dès la phase préhospitalière permet d'orienter le patient vers la
meilleure ressource clinique et thérapeutique. Cette orientation ne se conçoit qu'au sein d'une
politique partagée de réseau structuré de l'urgence coronaire.

Mise en page samu-de-france .com - 2002
URGENCE CORONARIENNE
OU PROTOTYPE DE L'URGENCE PRÉHOSPITALIÈRE
Données épidémiologiques
La maladie coronarienne est la deuxième cause de mortalité en France avec 120 000 infarctus
du myocarde par an et plus de 47 000 décès soit 9,4 % incluant les morts subites. Le projet
épidémiologique MONICA a permis d'évaluer la fréquence de ces décès d'origine coronaire à
200-260/100 000 habitants [1]. La mortalité cardiovasculaire est de loin la première cause de
décès chez l'homme de moins de 65 ans. L'amélioration du pronostic porte essentiellement sur
la mortalité hospitalière (5 à 10 %) depuis la généralisation des méthodes de reperfusion
coronaire [2]. La maladie coronaire évolue en France comme en Europe en terme de
prévalence ces dernières années. La fréquence de l'infarctus du myocarde diminue alors
qu'augmentent les syndromes coronariens aigus sans augmentation du segment ST que sont
l'angor instable et l'infarctus sans onde Q [3]. L'activité cardiologique représente en moyenne
20 à 40 % de l'activité des Smur de France dont plus de 25 % de syndromes coronariens
aigus [4]. L'activité des Smur en ce domaine ne peut donc se limiter au seul infarctus du
myocarde en phase aiguë mais bien intégrer des stratégies dynamiques de prise en charge des
syndromes coronariens aigus sans augmentation du segment ST. En fait, c'est la définition
même de l'infarctus qui évolue pour dépasser le seul diagnostic électrique pour s'étendre au
diagnostic biochimique [5].
Temps gagné : myocarde préservé et sauvé
L'infarctus du myocarde aigu est en rapport avec une oblitération artérielle aiguë ; le plus
souvent de nature thrombotique réclamant une reperfusion coronaire la plus précoce
possible [6]. Au cours de l'infarctus du myocarde les six premières heures suivant le début de
la douleur, et donc la phase préhospitalière, sont des paramètres essentiels aux stratégies de
reperfusion et tout particulièrement à la mise en œuvre d'une thrombolyse dans des délais
acceptables [7]. Le gain de survie est d'autant plus important que la reperfusion du myocarde
est précoce, complète et durable [8] [9]. La réduction de mortalité est de 50 % pour un
traitement effectué la première heure et de 30 % la deuxième heure. L'idéal serait d'intervenir
dans un délai inférieur à deux heures pour éviter la mort subite par fibrillation ventriculaire,
mais aussi pour préserver la fonction ventriculaire gauche [10]. Les traitements
thrombolytiques par voie intraveineuse ont donc un rôle essentiel dans cette volonté de
reperfusion précoce [11]. L'administration préhospitalière des agents thrombolytiques permet
une réduction de la mortalité de 15 % et un gain de temps moyen de 50 min par rapport à la
thrombolyse intrahospitalière [12] [13]. Il est donc primordial d'intervenir dès l'appel du
patient, au plus près du début des symptômes [14]. La thrombolyse intrahospitalière est un
échec de la thrombolyse préhospitalière. Si aujourd'hui, cette dernière a largement démontré
sa faisabilité, son innocuité, même chez des personnes âgées, lorsqu'elle est réalisée par des
équipes entraînées ; elle ne peut à elle seule résumer le traitement initial de l'infarctus [15].
Au contraire elle doit s'intégrer dans de réelles stratégies dynamiques de prise en charge
associant l'angioplastie à l'utilisation précoce des inhibiteurs des glycoprotéines IIb-IIIa, à des
doses réduites d'héparine non fractionnée ou d'héparine de bas poids moléculaire. La prise en
charge du syndrome coronarien en phase aiguë est en permanente évolution.

Mise en page samu-de-france .com - 2002
Précocité de l'appel au Samu : facteur clé de succès
En France, l'urgence coronarienne est indissociable de l'activité des Samu-Centres 15. La
douleur thoracique est l'un des motifs d'appel le plus fréquent. Pour le médecin régulateur,
tout appel pour douleur thoracique, suspecte ou évocatrice, engage les moyens d'une unité
mobile de Smur. Cette prise en charge rapide et efficace doit permettre de porter le diagnostic
et d'initier la reperfusion coronaire [16]. Le rôle du Smur est donc essentiel dans le cadre de
l'infarctus, mais aussi dans le cadre plus large des syndromes coronariens aigus où il peut
initier là aussi la thérapeutique et également identifier rapidement la gravité potentielle du
patient pour l'orienter correctement [17] [18]. La concertation entre les urgentistes et les
cardiologues est une étape prépondérante au succès de cette filière de soins, de ce réseau de
l'urgence coronaire. Dès que le temps écoulé entre les premiers symptômes et la prise en
charge initiale est supérieure à 20 min, le bénéfice de la médicalisation préhospitalière est
incontestable [19]. Le principal acteur déterminant de ces premières heures est donc le patient
lui-même ou son entourage immédiat. C'est probablement là que se situe le cœur du
problème ; en effet les registres les plus récents le démontrent [20] : plus de 65 % des patients
échappent à toute stratégie de reperfusion parce qu'ils alertent trop tard ou mal. Il s'agit là d'un
mal international qui concerne particulièrement des sous-populations de patients à risque [21].
Cette alerte tardive apparaît comme encore plus marquée dans l'angor instable [3].
PRISE EN CHARGE INITIALE
Intervenants médicaux
La prise en charge d'un patient suspect d'infarctus ou de syndrome coronarien aigu est
incontestablement un acte de réanimation préhospitalière exigeant une formation préalable
encadrée [22]. Ce médecin, senior de l'urgence, encadre une équipe de Smur disposant d'un
matériel de réanimation complet et immédiatement accessible [23]. L'organisation du travail
en équipe est un gage de réussite [24]. En effet une formation conjointe des médecins et des
paramédicaux à la gestion globale de ces patients permet ici encore de gagner du temps.
Diagnostic avant tout clinique
La douleur peut être typique, d'allure angineuse, à début brutal, intense, rétrosternale
constrictive en barre avec ou sans irradiations. Elle s'accompagne alors d'une sensation de
mort imminente, évolue depuis 30 min et résiste à la prise de dérivés nitrés. Elle est souvent
associée à des signes d'accompagnement tels que des troubles digestifs, un malaise général,
des sueurs, une pâleur, des lipothymies qui parfois résument la symptomatologie. Mais
parfois la douleur peut être absente (5 à 10 % des cas), en particulier chez le sujet âgé et
diabétique [25]. Les formes atypiques sont fréquentes dans leur topographie, leur intensité ou
leur mode de révélation. L'horaire de survenue de la douleur est un élément essentiel à
rechercher car déterminant pour la décision thérapeutique. L'interrogatoire recherche les
antécédents du patient, une éventuelle histoire coronarienne familiale, les traitements en
cours, leur observance ou leur changement récent. Cependant, il convient de remarquer que,
dans le cadre de l'activité des Smur, l'infarctus est inaugural dans plus de 50 % des cas. La
recherche de facteurs de risque majeurs, tels que l'hypercholesterolémie, l'hypertension
artérielle, le tabagisme ou le diabète, est toujours réalisée car ce sont autant d'éléments de
gravité surajoutés qui interviennent, non seulement dans la décision thérapeutique mais
également dans l'orientation du patient. La mesure des constantes vitales, l'auscultation
démasqueront une éventuelle mauvaise tolérance hémodynamique signant le choc

Mise en page samu-de-france .com - 2002
cardiogénique et modifiant la prise en charge initiale. Par ailleurs, l'examen clinique tente
d'éliminer une autre affection lorsqu'un doute diagnostique subsiste en s'attachant à
démasquer tout particulièrement une péricardite ou une dissection aortique. C'est dès cette
phase précoce que l'on recherche d'éventuelles contre-indications à la thrombolyse dans le
cadre d'un infarctus bien sûr mais également devant tout syndrome coronarien aigu dont on
connaît le risque d'évolution à court terme vers l'infarctus [26]. Enfin aujourd'hui chez le sujet
jeune la recherche d'une prise récente de cocaïne est vérifiée [5].
Données électrocardiographiques
L'électrocardiogramme 17 dérivations est idéalement la clé du diagnostic. Les douze
premières dérivations peuvent mettre en évidence un sus-décalage à connexité supérieur du
segment ST supérieur à 1 mm dans les dérivations frontales ou à 2 mm dans les dérivations
précordiales et ceci dans au moins deux dérivations contiguës. La présence d'images en miroir
dans les dérivations opposées conforte le diagnostic. L'enregistrement doit être complété par
l'analyse des dérivations droites (V3R, V4R) à la recherche d'un infarctus du ventricule droit
qui modifie la thérapeutique initiale, engage la prudence et conditionne l'orientation.
L'analyse des dérivations postérieures (V7, V8, V9) vient compléter la rigueur de l'examen
électrique.
En fait 18 % des électrocardiogrammes sont atypiques et 50 % ne permettent pas de faire le
diagnostic [26]. Un authentique infarctus est souvent précédé d'un courant de lésion sous-
épicardique, voire d'un ECG normal. Ceci justifie devant une simple présomption clinique de
réitérer l'examen électrique à 15 min d'intervalle. L'apparition d'un bloc de branche gauche
d'apparition récente associé à une douleur typique doit faire suspecter le diagnostic d'IDM et
faire prendre la décision de revascularisation [27]. Dans tous les cas, la récupération d'un
ECG antérieur vient conforter le diagnostic [28]. Dans les cas les plus litigieux, il peut être
fait recours à la transmission de l'électrocardiogramme par télémétrie [29].
Cependant, devant une symptomatologie et un tracé typique, le diagnostic des médecins
urgentistes est sûr et ce dernier pose le diagnostic d'une revascularisation urgente soit par
thrombolyse, soit par angioplastie primaire [30]. Parfois, malgré une douleur évocatrice, les
signes électriques restent discrets et non spécifiques voire même résolutifs lors de la phase
préhospitalière et les signes patents de syndrome coronarien aigu n'apparaissent que dans les
heures suivantes justifiant l'hospitalisation du patient [31] et des contrôles électriques toutes
les six heures [32].
Les éléments de diagnostic clinico-électriques sont-ils suffisants
en phase préhospitalière ?
La stratification du risque précoce en fonction des seuls événements cliniques ou électriques
n'est peut-être aujourd'hui pas suffisamment exhaustive. En pratique, trois situations s'offrent
à l'urgentiste.
1. L'électrocardiogramme est typique avec un sus-décalage du segment ST franc, la décision
de reperfusion est immédiate.
2. L'électrocardiogramme est anormal sans augmentation du segment ST, il peut s'agir d'un
véritable infarctus sans onde Q ou d'un angor instable.

Mise en page samu-de-france .com - 2002
3. L'électrocardiogramme est normal mais la clinique est évocatrice.
Les marqueurs précoces de l'ischémie myocardique peuvent être dans les deux derniers cas
des éléments essentiels de l'orientation diagnostique et thérapeutique de ces patients et dès la
phase préhospitalière. Ces marqueurs biologiques ont largement fait leur preuve en milieu
hospitalier [33] [34] [35], la myoglobine, les troponines et les CPK-MB sont dosés en
routine [36] et ont une valeur pronostique [37] dans le cadre des syndromes coronariens aigus
sans élévation du segment ST, ils contribuent largement à leur stratification [38] [39] et leur
orientation thérapeutique [40] [41] [42]. La troponine I est le marqueur le plus spécifique de
la nécrose myocardique [43]. Toutefois sa cinétique d'apparition (> 2 h) semble en limiter
l'usage pour la prise en charge précoce des infarctus en phase aiguë mais est probablement
essentielle pour juger de la gravité potentielle d'un syndrome coronarien aigu sans élévation
du segment ST. La myoglobine, marqueur plus sensible, d'apparition plus précoce mais moins
spécifique [44], pourrait être un élément du triage préhospitalier dans les années à venir. La
nécrose myocardique « à minima » peut être détectée par l'élévation isolée de la troponine au
cours d'un angor instable. C'est bien de la synthèse de ces événements cliniques et biologiques
que vient la nouvelle définition des syndromes coronariens aigus [5]. Il est donc possible
d'exprimer la probabilité de survenue d'un événement cardiaque majeur [37]. L'utilisation de
ces marqueurs peut se faire grâce à des kits spécifiques au lit du malade et dès la phase
préhospitalière [45], ils deviendront bientôt incontournables à la prise en charge moderne des
syndromes coronariens aigus, dès la phase préhospitalière. Le dosage des marqueurs avant
toute thrombolyse peut guider l'évolution thérapeutique car une ascension de cette troponine
traduirait un échec de la thrombolyse et imposerait un geste urgent de revascularisation [46].
De plus amples contrôles de qualité et des essais comparatifs de ces mini-laboratoires
embarqués sont encore nécessaires [47]. D'autres marqueurs de l'inflammation comme la CRP
pourraient également très rapidement se positionner [48]. À la lumière de ces données, on voit
se dessiner de nouveaux algorithmes décisionnels pour l'évaluation et la gestion des
syndromes coronariens avec des orientations argumentées vers les centres de cardiologie
interventionnelle.
STRATÉGIE THÉRAPEUTIQUE
Mise en condition du patient
Le patient doit être installé confortablement et aucun effort ne doit lui être demandé. Toute
mobilisation doit s'effectuer sous stricte surveillance médicale. L'anxiété légitime du patient
doit être combattue ; les fonctions vitales sont constamment surveillées grâce à un monitorage
permanent associant électrocardiogramme, mesure de la saturation artérielle en oxygène et
pression artérielle non invasive. En particulier la qualité du monitorage du segment ST est
essentielle [36]. Un défibrillateur vérifié est immédiatement accessible ainsi que l'ensemble
des médicaments de la réanimation cardiaque. Le matériel d'intubation et de ventilation
contrôlée est également à proximité immédiate. Les paramètres vitaux sont relevés et
consignés sur une feuille de surveillance prévue à cet effet et transmise à l'équipe hospitalière,
tous les événements y sont notés. La vigilance de l'équipe de l'unité du SMUR est
permanente. La prise de deux voies veineuses périphériques est indispensable, l'une étant
réservée à l'agent thrombolytique. Un bilan sanguin est réalisé avant l'initiation de toute
thérapeutique.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%