Traitement au stade métastatique

879
Chapitre XIV
Traitement au
stade métastatique
15 à 25% des patients présentent d'emblée une diffu-
sion métastatique lors du diagnostic de cancer du rein,
avec des localisations multiples dans la majorité des
cas (Tableau 1).
Le poumon est l'organe le plus volontiers intéressé
dans 50 à 60 % des cas.
Dans 70 % des cas, les sites métastatiques sont regrou-
pés au sein d'un même organe.
Le pronostic spontané de ces patients est sombre avec
10% de survie à 1 an, 2 à 5% à 5 ans. La survie moyen-
ne est de 10 mois [22].
Ces patients décèdent suite à l’évolution métastatique
et non à la progression loco-régionale.
Le cancer du rein au stade métastatique présente un
pronostic péjoratif avec 10% de survie à 1 an et 5% à 5
ans. Plusieurs facteurs pronostiques influencent la sur-
vie avec notamment l'âge, l'état général et la perte de
poids. Plusieurs études ont confirmé l'existence de
paramètres pronostiques et permettent de distinguer
des groupes de patients présentant des évolutions fort
différentes [60, 61, 66, 78, 107].
En 1988, ELSON étudie une série de 610 patients por-
teurs de cancer du rein métastatique et identifie 5 fac-
teurs de risque statistiquement significatifs :
l'état général, le délai entre le diagnostic et la métasta-
se, le nombre de sites métastatiques, la perte de poids,
ainsi que la cytotoxicité à une chimiothérapie antérieu-
re (Tableau 2) [26].
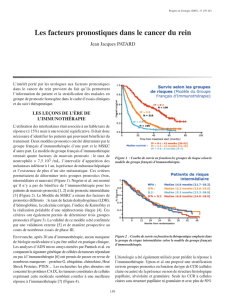
ELSON propose selon le nombre de facteurs de mauvais
pronostic de répartir ces patients selon 5 groupes pro-
nostiques (Figure 1). Le premier groupe présente un
seul facteur de risque, la médiane de survie est de 12,8
mois. Les groupes suivants présentent de 2 à 5 facteurs
associés. La survie moyenne de ces groupes est respec-
tivement de 7, 5, 3, 2 mois [26].
I. LES FACTEURS PRONOSTIQUES
PLAN
I. Les facteurs pronostiques
II. Les différents traitements
• Hormonal
• Chimiothérapie
• Immunothérapie
• Chirurgie
Tableau 1. Les métastases du cancer du rein.
Nombre multiple 97%
unique 3%
L’organe intéressé 1 organe 70%
2 organes ou plus 30%
Fréquence d’atteinte
par organe au diagnostic
(Ritchie-1982) (Franklin 1996) [38]
• Poumon 50-60% 87%
isolé 30%
+ ganglion 25%
+ viscères 31%
• Ganglions 15-30% 49%
• Foie 28%
• Os 30-40% 14%
• Surrénale 10-15% 14%
• Tissu mou 7%
• Cerveau 10-13% 6%
Tableau 2. Eléments pronostiques dans le cancer du rein
métastatique [26].
Etat général
Délai entre diagnostic et métastase
Nombre de sites métastatiques
Perte de poids
Mauvaise tolérance à une chimiothérapie antérieure

880
Figure 1. Facteurs pronostiques dans le cancer du rein métastatique.Survie selon 5 groupes
pronostiques. Etude sur 610 patients [26].
Nombre de Groupes Nombre de Survie (%) Médiane
facteurs de pronostiques patients de survie
risque 3 mois 12 mois (mois)
0 ou 1 1 113 92 52 12,8
2 2 141 87 31 7,7
3 3 151 76 18 5,3
4 4 123 54 93,4
5 582 35 12,1
MOIS

881
Le pouvoir de discrimination de ces groupes doit être
considéré lors du traitement de cancer du rein métasta-
tique. Le groupe qui présente un seul élément de mau-
vais pronostic a la meilleure survie avec 52% à 1 an et
24% à 2 ans.
Plusieurs études ont confirmé ces données. FOSSA,en
1994, étudie une série de 295 patients traités par chi-
miothérapie ou interféron. En analyse mono-factoriel-
le, les facteurs pronostiques sont les suivants : l'âge, la
réalisation ou non d'une néphrectomie élargie, l'état
général, la présence de métastases hépatiques, l'accélé-
ration de la vitesse de sédimentation, la perte de poids
et le traitement. En analyse multi-factorielle, cet auteur
retrouve 3 éléments indépendants de mauvais
pronostic : la VS supérieure à 100 à la première heure,
la perte de poids supérieure à 10% en moins de 6 mois,
l'état général de 2 à 3 [35].
La néphrectomie élargie apparaît dans plusieurs études
en analyse mono-factorielle comme un élément pro-
nostique. Néanmoins, en analyse de régression multi-
variée, la néphrectomie élargie n'apparaît plus comme
un facteur indépendant, mais elle est corrélée à l'état
général du patient [20, 21, 26].
Ces éléments pronostiques permettent d'orienter les
indications thérapeutiques selon le groupe pronostique.
D'autre part, la définition de ces paramètres pronos-
tiques permet lors d'études prospectives randomisées
de répartir les résultats selon ces groupes pronostiques.
Ainsi dans la plupart des études prospectives, quelle
que soit la modalité thérapeutique proposée, la survie
dépend non seulement du bras thérapeutique mais aussi
des différents facteurs pronostiques.
Ceci pourrait dans le futur permettre d'éviter des traite-
ments coûteux et responsables de morbidité importan-
te chez les patients dont le pronostic est trop péjoratif
pour être influencé par le traitement [23, 25, 43].
Le traitement hormonal repose sur des bases expéri-
mentales qui n'ont pas été confirmées par de nom-
breuses études cliniques.
Chez l'animal, une tumeur du rein présente une sensi-
bilité hormonale avec induction tumorale chez le ham-
ster traité de façon prolongé par du Diethylstilbestrol
[63]. Ces tumeurs diminuent de volume après l'arrêt
des oestrogènes ou par utilisation de traitement anti-
oestrogène ou de progestérone. Ces bases expérimen-
tales ont été suivies par de nombreuses études cliniques
utilisant la progestérone dans le traitement du cancer
du rein métastatique. Les résultats sont décevants tant
en ce qui concerne la progestérone, les androgènes ou
les anti-oestrogènes isolés ou en association. Le taux de
réponse est situé entre 5 et 10% dans la plupart des
séries de phase II ou les études randomisées phase III
[45, 119].
Durant les années 80, l'explication de ces mauvais
résultats était difficile à donner dans la mesure où il
existait de nombreux récepteurs d'oestrogène, de pro-
gestérone et d'androgène dans les tumeurs du rein.
Néanmoins, l'expression de ces récepteurs est d'autant
plus grande que la différenciation cellulaire est impor-
tante. Ainsi, le rôle des récepteurs hormonaux a certai-
nement été surévalué. Des études récentes retrouvent
un nombre de tumeurs présentant des récepteurs aux
oestrogènes moins important que sur les études histo-
riques [49].
Des essais cliniques ont étudié l'effet de fortes doses de
Tamoxifen (100 à 150 milligrammes par m2et par jour)
avec 12% de réponses [105] Ces résultats sont déce-
vants et ne sont pas les résultats obtenus par cet anti-
oestrogène dans le cancer du sein [88]. Des études sont
actuellement en cours évaluant le Tamoxifen associé
aux agents cytotoxiques telle la Vinblastine.
Enfin, l'existence de récepteurs à la Somatostatine
pourrait peut-être redonner espoir à la modulation
immunologique des tumeurs du rein par traitement hor-
monal [89].
Lors des 20 dernières années, de nombreuses études
ont utilisé plus de 70 agents cytotoxiques de façon iso-
lée ou associée lors d'études en phase II [45, 118, 119].
Seules la Vinblastine et la Floxuridin (FUDR) ont mon-
tré une activité reproductible. Ces études sont néan-
moins anciennes et les critères d'inclusion ne sont pas
toujours clairement identifiés avec des facteurs pronos-
B. Chimiothérapie
A. Traitement hormonal
A. Traitement hormonal
B. Chimiothérapie
C. Immunothérapie
• Les Interférons
• L’Interleukine 2
• Les associations
• La thérapie cellulaire LAK - TIL
D. Place de la chirurgie
E. En pratique
II. LES DIFFÉRENTS TRAITEMENTS

tiques non rapportés. Ceci explique que les bons résul-
tats rapportés par MURPHY en 1977 avec 25% de
réponses n'ont pas été retrouvés sur les séries plus
récentes. Actuellement, ces études font état de 10 à 15
% de réponses avec une médiane de survie de 8 mois
[13, 20]
Un traitement original a été proposé par HRUSHESKI,
utilisant la Floxuridin [47]. Cet auteur a rapporté 19%
de réponse. La durée de rémission était de 11 mois et la
durée moyenne de survie de 14 mois. Tous les patients
étaient néphrectomisés et avaient pour 1/3 d'entre-eux
des facteurs de bon pronostic. Ces données ont été
confirmées par WILKINSON [115].
RICHARDS utilisant une perfusion sur 5 jours ne rappor-
te aucune réponse dans une étude de 29 patients traités
par Floxuridin [91].
Le cancer du rein est une des rares tumeurs chimio -
résistantes. Cette originalité réside certainement dans
l'existence d'une chimio-résistance spontanée des cel-
lules tumorales du cancer du rein. Cette résistance à la
chimiothérapie est due à l'expression d'un double phé-
notype :
• Résistance multidrogue liée à l'expression de la P
Glycoprotéine. Les agents anticancéreux concernés par
ce phénomène sont les Anthracyclines, les Vinkaloïdes,
le Taxol ainsi que les Epipodophylotoxines et la
Mitoxantrone. LING a isolé une glycoprotéine mem-
branaire, la Glycoprotéine P, qui est l'expression de la
chimio-résistance MDR. Cette Glycoprotéine P est
codée par le gène MDR1 localisé sur le chromosome 7.
Ce mécanisme fait appel a une pompe d'efflux permet-
tant l'explusion de certains agents anticancéreux, dimi-
nuant ainsi leur concentration intracellulaire [82]. Cette
Glycoprotéine peut être détectée par les anticorps spé-
cifiques tel GSB1. La Glycoprotéine P est présente
dans le tissu rénal sain et tumoral au niveau des cellules
du tube contourné proximal du rein. Cette chimiorésis-
tance spontanée du cancer du rein pourrait corres-
pondre à une fonction augmentée de cette protéine pré-
sente dans le tissu normal.
L'expression du gène MDR ou de la Glycoprotéine P
est retrouvée dans la presque totalité des tumeurs, avec
une expression du gène MDR entre 54 et 100 % selon
les études [34, 51, 52, 64]. Ce mécanisme complexe de
la résistance à la chimiothérapie, explique la résistance
notamment à la Vinblastine ou à l'Adriamycine. Sur le
plan thérapeutique, il est possible in-vitro de moduler la
chimio-résistance notamment par introduction d'inhibi-
teurs de canaux calciques tel le R-Verapamil [64]. Des
études cliniques sont actuellement en cours [67].
• Un deuxième mécanisme de chimio-résistance est
illustré par le rôle du système du Glutathion dans le
cancer du rein. Ce deuxième mécanisme a été mis en
évidence par MICKISCH [64]. Le système du
Glutathion induit une résistance à certains médica-
882
ments différents de la résistance MDR (agent alkylant
et platine). Des enzymes conjuguent des substances
toxiques avec le Glutathion (Glutathion S Transférase).
Des études expérimentales démontrent une concentra-
tion de Glutathion plus importante dans les tumeurs
résistantes au Cisplatyl que dans celles exprimant le
gène MDR résistant à la Vinblastine. Un inhibiteur spé-
cifique du système Glutathion est le Buthioninesul-
foximine (BSO) [54].
Au total, le cancer du rein est par essence chimio-
résistant. Cette chimio-résistance est bien étudiée sur le
plan biologique, et pourrait permettre dans un avenir
proche d'être modulée grâce à des molécules bloquant
spécifiquement un ou les deux éléments majeurs de
chimio-résistance connus actuellement [17, 80].
Les défaillances du système immunitaire sont connues
depuis longtemps comme facteur déterminant dans
l'apparition d'un cancer. Ceci est illustré par les régres-
sions spontanées de certaines tumeurs et l'efficacité de
la BCG thérapie dans les tumeurs de vessie.
En ce qui concerne le cancer du rein, l'observation de
diminution spontanée du volume métastatique ainsi
que l'évolution rapide des tumeurs du rein découvertes
dans les suites d'une grossesse confirme l'existence
d'une relation entre système immunitaire et apparition
du cancer [39].
Le système immunologique réalise une surveillance
permanente au sein de notre organisme qui prévient le
développement de cellules tumorales grâce à la partici-
pation de lymphocytes T cytotoxiques, de natural
killers et de macrophages. Ce mécanisme est efficace
car le cancer est reconnu comme un élément étranger à
notre organisme. Cette reconnaissance est due à l'ex-
pression de l'identité des cellules tumorales sous la
forme d'antigènes tumoraux et à l'expression d'anti-
gènes de classe I déterminants dans le mécanisme de
présentation de l'antigène. L'activation des lympho-
cytes T type cytotoxique (CD 8) nécessite la présence
de cellules de classe I et la production de lymphokines
par des lymphocytes T (CD 4).
Les défaillances du système de surveillance immunolo-
gique peuvent être multiples. Un des mécanismes
essentiels est constitué par la mauvaise reconnaissance
des cellules tumorales du fait de la faible expression ou
de l'absence d'expression de molécules de surface de
classe I. Ceci perturbe la reconnaissance de l'antigène
tumoral par les lymphocytes T.
Parmi ces différentes voies thérapeutiques, le traite-
ment adapté actuellement au cancer du rein utilise les
cytokines, les LAK ou les TIL [27, 42, 69, 117].
C. Immunothérapie

1. Les interférons
• Il existe 3 Interférons :. Ils constituent un
ensemble de protéines hétérogènes dont le point com-
mun est de bloquer la réplication virale et il constituent
d'autre part des facteurs de croissance et de puissants
immunorégulateurs.
L'interféron est produit par les lymphocytes en
réponse à des virus ou à des acides nucléiques.
Il a été très largement utilisé dans les quinze dernières
années dans le traitement du cancer du rein métasta-
tique. Les premiers essais ont débuté en 1983. De très
nombreux protocoles ont été proposés.
L'interféron est commercialisé sous 2 présentations :
Roféron pour l'interféron 2 a et Introna pour l'inter-
féron 2 b. Les caractéristiques principales de ces
molécules sont l'inhibition de la réplication de nom-
883
breux virus et une activité anti-proliférative sur les
lignées de cellules cancéreuses à une posologie plus
importante. D’autre part, ils bloquent la traduction des
ARN messagers et accélèrent la cinétique de leur cata-
bolisme ; ils activent les lymphocytes natural killers et
les macrophages assurant ainsi une activité anti-tumo-
rale (Tableau 3) [71].
La cinétique varie en fonction du mode d'administra-
tion : intraveineuse, intramusculaire ou sous-cutanée.
En moyenne, la demi vie d'élimination varie entre 5 et
15 heures. L'élimination est urinaire, il n'est pas néces-
saire de modifier la posologie chez l'insuffisant rénal.
La toxicité est essentiellement marquée par l'existence
d'un syndrome pseudo-grippal, d'une asthénie intense,
d'anorexie ou d'incidents cardiaques ou neurologiques
qui peuvent nécessiter une diminution de la posolo-
gie.
Tableau 3. Principales caractéristiques de l’Interféron et de l’Interleukine 2.
Interféron Interleukine 2
Classe Cytokines Cytokines
Nom déposé INTRONA Interféron 2-b PROLEUKIN 18 MUi
ROFERON Interféron 2-a
Origine Protéine produite par macrophages Glycoprotéine sécrétée par les
et lymphocytes non T -non B lymphocytes T
Synthèse inhibée par la ciclosporine
et les corticoïdes
. Antivirale .• Prolifération des lymphocytes
.Immunomodulatrice activés T4-T8
- cellulaire l'activité NK • Augmente l’effet cytotoxique des
Actions -
macrophage favorise présentation de l’antigène
lymphocytes T
. Antiproliférative : allonge le • Prolifération des lymphocytes T-NK
cycle cellulaire • Activité LAK-TIL
• Production de cytokines INF , TFN
Posologie 18 millions U/j 18 millions UI/m2/j en
Administration selon AMM 3 j/sem. pendant 6 mois perfusion continue sur 5 jours
1 an par voie sous-cutanée Cure à répéter après 1 semaine de repos
Linéaire Biphasique
Pharmacocinétique T maximum : 3 à 6 h T maximum : 3-4 heures
Demi-vie : 1 à 4 heures Demi-vie : 3-5 heures
Elimination urinaire Elimination urinaire
Voie d’administration Intra-musculaire ou sous-cutanée Intraveineuse, intramusculaire ou
sous-cutanée
.Dose-dépendants . Dose-dépendants
.Syndrome pseudo-grippal .Hypotension, rétention hydrique
.Anorexie, nausée, diarrhées . Troubles du rythme, ischémie
. Troubles de la vigilance .Dyspnée, oedème pulmonaire
Effets indésirables .Neutropénie .Hypersensibilité : fièvre,
.Thrombopénie frissons, prurit, rash
.Elévation des transaminases .Nausées, vomissements, mucite
.Erythème, prurit .Thrombopénie, anémie
. Insuffisance rénale
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%