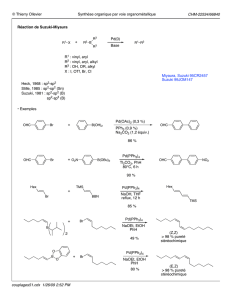
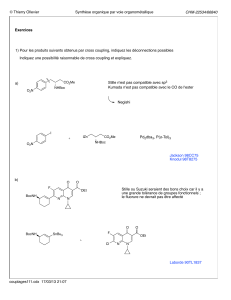
Réaction de Buchwald

Arylation et alcénylation
α-arylation et α-alcénylation des carbonyles ont toujours été considérées comme des réactions difficiles
ligands encombrés
Percée récente grâce à de nouveaux ligands
ligands riches en électrons
CO2HPd(0) Br
CO2R
ibuprofène
Sélection de bases aussi importantes : MHMDS, NaH, ONa
MeONa, EtONa généralement pas utilisables comme bases car elles sont facilement oxydables en aldéhyde
avec les halogénures d'aryle
Ar XPd(0)
Ar PdX
Pd Ar CH3CHO Pd(0) ArH
1) Arylation de composés à méthylène actif
I
PdCl2(PPh3)2
t
BuOK, DME
73 %
CO2Et
CN
OCH3CH2
CO2Et
CN
via
CH3CH2ONa
© Thierry Ollevier Synthèse organique par voie organométallique
CHM-22534/66840
couplages101.cdx 2/21/07 2:20 PM

I
PdCl2(PPh3)2
NaH, THF
72 %
CN
CN
Cl
Pd(dba)2, P(tBu)3
Na3PO4, PhMe
90 %
CO2Et
CN
Br
Pd(OAc)2
K3PO4, THF
Pd(dba)2, PPh3
NaH, Dioxane
77 %
I
NC
NC
MeO MeO
tBu
O
O
O
O
tBu
Me
P(tBu)2
Br PhO2S SO2Ph
Cl
Pd2(dba)3, P(tBu)3
NaH, THF
84 %
CO2tBu
CO2tBu
MeO MeO
Me
CO2Et
CO2Et
Br
MeI MeI
Me CO2Et
CO2Et
Ph
HCO2Et
CO2Et
H
Br
Pd2(dba)3, P(tBu)3
K3PO4, PhMe
91 %
HCO2Et
CO2Et
Ph
CO2Et
CN
CN
CN
SO2Ph
SO2Ph
CO2tBu
CO2tBu
© Thierry Ollevier Synthèse organique par voie organométallique CHM-22534/66840
couplages102.cdx 1/26/09 3:40 PM

2) Arylation de cétones
Toujours considérée comme une réaction difficile
Découverte par Miura, Buchwald et Hartwig presque simultanément (1997)
maintenant les α-aryl cétones sont facilement accessibles
I
PdCl2, LiCl
Cs2CO3
DMF
48 %
Ph Ph
O
Ph Ph
O
Ph Ph
OMe
Pd(dba)2, BINAP
Br
O
Me O
Me
OMe
t-
BuONa, THF
91 %
Pd(dba)3
KN(SiMe3)2, THF
Br
Ph
O
Ph
O
Ph
Fe
P(
o
-Tol)2
P(
o
-Tol)2
Br
Pd(dba)2, Tol BINAP
t-
BuONa
83 %
t-
Bu
O
P(
o
-Tol)2
P(
o
-Tol)2
Tol BINAP =
O
t
Bu
© Thierry Ollevier Synthèse organique par voie organométallique
CHM-22534/66840
couplages103.cdx 2/21/07 2:21 PM

Br
Pd(OAc)2, PPh3
K2CO3, o-xylène
O
O
Pd(PPh3)4
Cs2CO3, o-xylène
61 %
O
Br
Pd(OAc)2, PPh3
Cs2CO3, DMF
85 %
OMe
OMe
OMe
OMe
O
OMe
OMe
OMe
OMe
O
Br
Pd(OAc)2
t-BuONa, PhMe
85 %
O
Me
Me
Me
O
Me
Me
Me
MeMe
Cl
Pd(OAc)2, P(t-Bu)3
t-BuONa, THF
91 %
Ph
O
Me
OMe
Ph
O
Me
OMe
Me Me
© Thierry Ollevier Synthèse organique par voie organométallique CHM-22534/66840
couplages104.cdx 24/03/13 21:47

• Mécanisme
Pd(0)
O
Cs2CO3
OCs OCs
O
PdAr
Ar Br Ar Pd Br OPdAr
Pd(0)
O
Ar
Complexe isolé par Hartwig
P
P
Pd
Ph
Ph
Ph
Ph
O
R
R' R
O
Ar
R'
• Intramoléculaire
PdCl2(PPh3)2
Cs2CO3, THF
83 %
Br
O
O
NPdCl2(PPh3)2
Cs2CO3, PhH
90 %
OTf
O
O
N
O
O
transmétallation
Ar
© Thierry Ollevier Synthèse organique par voie organométallique
CHM-22534/66840
couplages105.cdx 2/21/07 2:22 PM
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%