Insuffisance mitrale organique

Revue
Insuffisance mitrale
organique :
physiopathologie,
histoire naturelle
et stratégies thérapeutiques
Catherine Szymanski
1,2
, Emmanuel Messas
1
, Christophe Tribouilloy
2
1
Hôpital européen Georges Pompidou, Pôle cardiovasculaire, 20 rue Leblanc, 75015 Paris
2
CHU Amiens Sud, Département de cardiologie, Avenue René Laënnec, 80054 Amiens
Cedex 1
L’insuffisance mitrale (IM) se caractérise par un reflux systolique anormal du sang du ventricule
gauche dans l’oreillette gauche, secondaire à la perte d’étanchéité de la valve. Son principal
risque est l’évolution vers une dysfonction ventriculaire gauche avec insuffisance cardiaque
responsable du pronostic péjoratif à long terme de cette valvulopathie. Sa présentation
clinique peut être aiguë ou chronique évoluant sur plusieurs années pendant lesquelles le
patient est longtemps asymptomatique. Si l’indication opératoire doit être rapidement portée
chez les patients symptomatiques, la prise en charge d’une IM asymptomatique reste encore
l’objet de controverse dans la littérature. Deux attitudes peuvent être proposées chez le patient
asymptomatique, en rythme sinusal sans signe de dysfonction ventriculaire gauche : sur-
veillance clinique et échocardiographique régulière avec chirurgie programmée dès l’appari-
tion d’une symptomatologie fonctionnelle ou de signes de mauvaise tolérance clinique
(trouble du rythme supraventriculaire, hypertension artérielle pulmonaire systolique ou signes
de dysfonction ventriculaire gauche) ; ou chirurgie réparatrice d’emblée chez des patients
encore asymptomatiques présentant une IM sévère (surface de l’orifice régurgitant
(SOR)>40mm
2
) associé à un mécanisme simple de la fuite, accessible à un geste de
réparation mitrale. La présence d’une fuite mitrale organique importante aggrave le pronostic
spontané de ces patients. Le moment de l’intervention est encore discuté dans la littérature. En
pratique clinique, ce sont l’étiologie, la sévérité de l’IM, le mécanisme, l’expérience de
l’équipe chirurgicale et l’absence de comorbidité qui pousseront à la réparation mitrale
précoce.
Mots clés :insuffisance mitrale, échocardiographie, plastie mitrale
L’insuffisance mitrale (IM) est,
avec le rétrécissement aortique,
la valvulopathie la plus fréquente dans
les pays occidentaux [1] et sa préva-
lence augmente avec l’âge [2, 3].
On distingue les fuites mitrales
organiques des fuites mitrales fonc-
tionnelles sur valve saine, secondaires
à une cardiomyopathie. Cet article se
consacrera aux fuites mitrales organi-
ques avec atteinte des feuillets valvu-
laires.
Les IM organiques sont définies
par la perte de l’étanchéité de la valve
mitrale, lors de la systole ventriculaire,
entraînant le reflux de sang du ventri-
cule gauche vers l’oreillette gauche.
Cette fuite est secondaire à la pré-
sence de lésions anatomiques de
l’appareil valvulaire et/ou sous valvu-
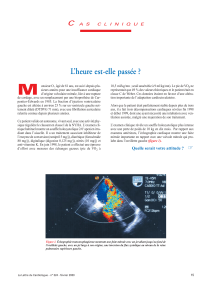
laire mitral (figure 1). Depuis le trai-
tement précoce des angines à strep-
tocoques et la disparition du
rhumatisme articulaire aigu secon-
m
t
Tirés à part : E. Messas
doi: 10.1684/met.2008.0146
mt, vol. 14, n° 1, janvier-février 2008 3
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

daire dans les pays développés, sa cause la plus fréquente
est dégénérative (fibroélastique et myxoïde) ou infectieuse
(endocardite) [4, 5].
Les principes de la prise en charge de l’IM répondent à
ceux de toute valvulopathie organique. L’intervention chi-
rurgicale n’est envisagée qu’en cas de fuite sévère (grade
IV, tableau 1) et elle est formelle en cas de fuite sympto-
matique c’est-à-dire en cas de classe NYHA II à IV. Le
problème actuel est de définir le temps chirurgical pour les
patients a- ou paucisymptomatiques avec fuite mitrale
sévère.
Les recommandations européennes [1] et américaines
[6] définissent les IM sévères selon des critères échocar-
diographiques identiques utilisant la largeur de la vena
contracta (correspondant au diamètre du jet à
l’origine) ≥7 mm, la présence d’un reflux systolique de la
fuite dans les veines pulmonaires, une surface de l’orifice
régurgitant ≥40 mm
2
, une fraction de régurgitation (qui
correspond à la fraction du volume d’éjection systolique
régurgitant dans l’oreillette gauche) ≥50 % et un volume
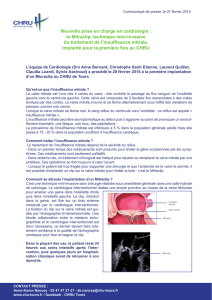
régurgitant ≥60 ml/battement (figure 2).
IM organique d’origine rhumatismale
Pour l’IM organique d’origine rhumatismale qui est
maintenant rare dans les pays occidentaux, la question de
la chirurgie précoce chez les patients asymptomatiques ne
se pose pas. En effet, les résultats de la plastie mitrale ne
donnent pas des résultats assez satisfaisants à long terme
permettant de prendre le risque d’une intervention chez
des patients asymptomatiques ayant un pronostic spon-
tané tout à fait acceptable. Ces résultats variables s’expli-
quent par la rigidité de l’orifice (figé en diastole et en
systole), les lésions valvulaires avec épaississement mar-
AP
V. pulmonaire
OD
V. tricuspide
V. aortique
V. mitrale
OG
VG
Ao
Fuite
mitrale
VD
Figure 1. Topographie des flux sanguins intracardiaques. Gauche : direction des flux sanguins intracardiaques. AP = artère pulmonaire,
V. pulmonaire = valve pulmonaire, OD = oreillette droite, V. tricuspide = valve tricuspide, VD = ventricule droit, Ao = aorte, OG = oreillette
gauche, V. aortique = valve aortique, V. mitrale = valve mitrale, VG = ventricule gauche. Droite : visualisation des flux de régurgitation
mitrale.
Tableau 1.Grades et sévérités
Grade Sévérité
I minime
II modérée
III moyenne
IV sévère
SOR
Flux régurgité
V max de l’IM
Ao
OG
VG
PISA
Figure 2. Evaluation de la fuite mitrale par la métode PISA
(Proximal Isovelocity Surface Area). SOR = surface de l’orifice
régurgitant, Vmax = vélocité maximale de l’IM en doppler continu,
OG = oreillette gauche, VG = ventricule gauche, Ao = aorte.
Revue
mt, vol. 14, n° 1, janvier-février 2008
4
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

qué, les calcifications extensives de l’anneau, rendant la
réparation mitrale plus risquée.
La survie des patients présentant une IM rhumatismale
modérée est excellente [7]. La survenue d’une fuite sévère
a un pronostic semblable à celui des IM dystrophiques,
avec toutefois, une progression annuelle du degré de
régurgitation plus importante dans ces lésions rhumatis-
males [8].
Les IM rhumatismales se prêtent beaucoup moins bien
à la chirurgie conservatrice notamment les formes fibreu-
ses et calcifiées mais des résultats acceptables à long
terme ont été publiés [9]. La plastie mitrale donne des
résultats favorables si les valves sont souples avec peu de
calcifications, et en l’absence d’épaississement trop
important des cordages valvulaires. Dans les formes sclé-
rorétractiles avec valves déformées, calcifiées et rigides,
inaccessibles à une réparation chirurgicale correcte, on
envisage le remplacement valvulaire mitral (RVM) en cas
d’apparition des symptômes et/ou d’une dysfonction VG.
Ce RVM se fera préférentiellement avec préservation de
l’appareil sous valvulaire [6] qui permet la conservation
de la fonction VG en post-opératoire et par prothèse
mécanique chez les patients jeunes (< 70 ans) nécessitant
une anticoagulation au long cours.
IM organique symptomatique
d’origine dystrophique
Les recommandations françaises [10], européennes [1]
et américaines [6] sont unanimes et en faveur d’une inter-
vention chirurgicale rapide.
Chez les patients symptomatiques (stade II-III ou IV de
la NYHA) avec fonction VG conservée ou moyennement
altérée (FEVG ≥30 % et diamètre télésystolique < 55 mm)
l’intervention chirurgicale doit être rapidement envisagée,
si possible par plastie, sinon par remplacement valvulaire
mitral (indication de classe Ib, d’après les recommanda-
tions). En cas de dysfonction VG sévère (FEVG < 30 %
et/ou DTSVG > 55 mm), l’indication opératoire sera por-
tée si l’IM est sévère, symptomatique, avec haute proba-
bilité de plastie mitrale et faible risque opératoire (indica-
tion de classe IIbC).
Les symptômes préopératoires sont un élément déter-
minant de la mortalité opératoire. Ceci est vrai même pour
les patients présentant une FE > 60 %, car il existe une
surmortalité tardive pour les patients opérés en classe
NYHA III ou IV préopératoire comparativement à ceux en
classe I ou II [11] (figure 3, en haut).
La chirurgie conservatrice mitrale a fait d’immenses
progrès ces dernières années. Elle permet de corriger dura-
blement la majorité des fuites avec morbi-mortalité mini-
mes (moins 1 % de mortalité chez les sujets de moins de
75 ans asymptomatiques dans les centres spécialisés) [12]
.
De tels arguments ont incité à proposer une chirurgie
réparatrice chez les patients asymptomatiques.
IM organique asymptomatique
Physiopathologie
Les IM chroniques, peuvent être longtemps bien tolé-
rées et asymptomatiques pendant plusieurs années.
L’adaptation et le remodelage ventriculaire gauche se fait
par une dilatation cavitaire avec augmentation du diamè-
tre télédiastolique (DTD) [13]. Progressivement et en
100
80
60
40
20
0
012345678910
100
80
60
40
20
0
01234 5678910
FE
≥
60
%
79
±
6
75
±
6
49
±
5
P
=
0,0003
NYHA I-II
NYHA III-IV
Survie (%)Survie (%)
Années
Années
FE
<
60
%
P
=
0,0001
41
±
5
Figure 3. Courbes de survie postopératoires chez les patients
avec IM sévère dystrophique insuffisances mitrales en classe
NYHA I-II et en classe NYHA III-IV. En haut : avec FEVG préopé-
ratoire ≥60 %. En bas : avec FEVG préopératoire < 60 %. D’après
Tribouilloy et al.Circulation 1999 ; 99 (3) : 400-5.
mt, vol. 14, n° 1, janvier-février 2008 5
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

l’absence de symptôme, le diamètre télésystolique (DTS)
va lui aussi augmenter avec conservation, dans un premier
temps, d’une FE normale, masquant l’installation d’une
dysfonction ventriculaire gauche silencieuse [14], avant
laquelle il faudrait envisager l’indication de chirurgie
mitrale. La fraction d’éjection ventriculaire gauche est
surestimée à cause de la diminution de la post-charge, et
une valeur de 60 % témoigne en fait déjà d’une altération
de la contractilité.
Histoire naturelle
Ling et al. [15]
,
dans une série incluant 71 % de patients
a- ou paucisymptomatiques, soulignent le pronostic péjora-
tif de ces IM (figure 4) avec une mortalité annuelle de 6,3 %,
une incidence d’insuffisance cardiaque de 63 % et de
fibrillation auriculaire (FA) de 30 %. L’incidence annuelle
de mort subite atteint 1,8 % dans la série de Grigioni et al.
[16]
, dont 0.8 % chez les patients a- ou paucisymptoma-
tiques (stade NYHA I-II) avec IM par rupture de cordage
suivis médicalement. Dans la cohorte de 833 patients
d’Aviérinos et al. [17] un sous-groupe de 153 patients
ayant une IM au moins modérée et/ou une FE inférieure à
50 % a une survie à 10 ans ne dépassant pas 55 %.
La FA associée aggrave le risque évolutif [18]
.
Dix ans
après le diagnostic, 48 % des patients initialement en
rythme sinusal auront développé un premier accès de
fibrillation auriculaire (taux linéaire de 5 % par an). Elle
constitue un facteur de risque de mortalité et d’insuffisance
cardiaque, indépendamment des symptômes. Elle est plus
fréquente chez les sujets de plus de 65 ans et en cas de
dilatation auriculaire gauche (diamètre supérieur à 50 mm).
Stratégies thérapeutiques
Deux travaux portant sur les patients asymptomatiques
avec IM sévère font date actuellement et semblent donner
des résultats contradictoires.
Les travaux menés à la Mayo Clinic ont souligné le
pronostic spontané défavorable de l’IM organique sévère
et l’intérêt d’un traitement chirurgical précoce avant
même tout retentissement sur le VG [15, 16, 18-20]. Alors
que, récemment, l’équipe de Vienne [21] a montré le bien
fondé d’une surveillance armée des patients porteurs
d’une IM dégénérative sévère asymptomatique avec chi-
rurgie qu’en dernier recours.
Ces résultats contradictoires ont conduit à des recom-
mandations américaines et européennes qui diffèrent pour
les patients asymptomatiques [1, 6]. La chirurgie de l’IM
asymptomatique est classée en IIa (opinion des experts en
faveur) par l’American College of Cardiology/American
Heart Association (ACC/AHA) alors qu’elle n’est classée
qu’en IIb (utilité et efficacité moins bien établies) par
l’European Society of Cardiology (ESC).
L’équipe de Vienne de Rosenhek [21] a montré le bien
fondé d’une surveillance armée des patients asymptoma-
tiques en étudiant de manière prospective 132 patients
consécutifs, âgés de 55 ans, asymptomatiques, atteints
d’une IM dégénérative sévère, suivis cliniquement et
échocardiographiquement, pendant 69,2 mois. La chirur-
gie n’était indiquée chez ces patients qu’en cas d’appari-
tion de symptômes, d’une augmentation des diamètres
ventriculaires gauches (DTSVG ≥45 mm ou 26 mm/m
2
),
d’une dysfonction VG (fraction de raccourcisse-
ment < 32 % ou FEVG < 60 %), d’une hypertension arté-
rielle pulmonaire (PAPs > 50 mmHg), ou d’une fibrillation
auriculaire. La survie totale du groupe (incluant la morta-
lité opératoire) a atteint 99 % à 12 ans et 91 % à 8 ans,
survie non statistiquement différente de la survie attendue
(figure 5). La survie libre d’indication chirurgicale a atteint
92 % à 2 ans, 65 % à 6 ans, et 55 % à 8 ans. Les auteurs
plaident ainsi pour cette surveillance armée des IM dégé-
nératives, volumineuses, chroniques, asymptomatiques,
avec indication chirurgicale en cas d’apparition de symp-
tômes, d’une augmentation échographique des diamètres
VG, d’une dysfonction VG, d’une HTAP ou d’une FA.
Cependant, ils insistent sur la nécessité impérative d’une
surveillance rigoureuse, clinique et échocardiographique
régulière entre des mains entraînées. D’après cette étude,
l’IM sévère par prolapsus apparaît comme une maladie
qui ne justifie pas de chirurgie précoce chez les patients
asymptomatiques en rythme sinusal sans dysfonction ven-
triculaire gauche ni HTAP.
Ces conclusions ne vont pas dans le sens du travail
prospectif publié par l’équipe d’Enriquez-Sarano de la
Mayo Clinic [20] incluant 456 patients, âgés de 63 ans,
atteints d’une IM organique asymptomatique sévère. Le
taux de décès à 5 ans, toutes causes confondues, était de
22 %, le taux de décès cardiaques était de 14 % et le taux
d’événements cardiaques de 33 %. Les patients avec une
SOR ≥40 mm
2
avaient un taux de survie à 5 ans inférieur
au taux attendu pour l’âge de la population (58 versus
78 %, p = 0,03). Les patients avec une SOR ≥40 mm
2
Années
Survie (%)
Attendue
Observée
100
80
60
40
20
0
012345678910
P
=
0,016
Figure 4. Courbes de survie sous traitement médical d’une série
d’insuffisances mitrales dystrophiques. La survie des patients por-
teurs d’une insuffisance mitrale est significativement diminuée par
rapport à la survie attendue. D’après Ling et al.N Engl J Med
1996 ; 335 (19) : 1417-23.
Revue
mt, vol. 14, n° 1, janvier-février 2008
6
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

avaient une augmentation du risque de décès de toutes
causes, de décès cardiaques et d’événements cardiaques.
Le moment de la chirurgie dans les IM sévères chroni-
ques asymptomatiques reste donc controversé.
Dans cette série D’Enriquez-Sarano [20], seuls 232
patients ont été opérés et l’intervention chirurgicale est
apparue comme un facteur indépendant d’une améliora-
tion de la survie (rapport de risque ajusté : 0.28 ; intervalle
de confiance à 95 % : 0.14-0.55 ; p<0.01). La chirurgie
précoce était associée à une diminution de l’incidence de
décès cardiovasculaires, d’insuffisance cardiaque et de
survenue de nouvel épisode de FA. Les auteurs plaident
ainsi, pour une intervention chirurgicale précoce chez les
patients ayant une IM organique volumineuse asympto-
matique dont la SOR quantifiée à l’échocardiographie
est ≥40 mm
2
sans dilatation ou dysfonction VG associée.
Ces résultats sont confortés par certains arguments
cliniques :
–Les patients opérés en classe NYHA III-IV [11, 15] ou
avec une FEVG < 60 % [15, 19] (figure 3) ou en FA ont un
moins bon pronostic que ceux opérés en classe I-II, avec
une FE normale et en rythme sinusal. Ces patients (en
classe NYHA I-II et avec une FE > 60 % et en rythme
sinusal) ont, après la chirurgie, une espérance de vie
semblable à celle de la population générale.
–Les patients avec une IM sévère présentent, sous
traitement médical, une surmortalité et une augmentation
du nombre d’événements cardiovasculaires. La chirurgie
réduit la mortalité et les événements cardiovasculaires
[22].
–Les résultats de la plastie mitrale sont excellents en
terme de mortalité opératoire (moins de 1 % de mortalité
chez les sujets de moins de 75 ans asymptomatiques dans
les centres spécialisés) [12] et de correction de la fuite
quand les conditions anatomiques sont favorables. Ils sont
aussi très favorables en termes de conservation de la
fonction VG permettant aux patients opérés précocement
de bénéficier d’une espérance de vie comparable à celle
d’une population de même âge [22].
La prévention de la dysfonction ventriculaire gauche
tardive doit être mise en balance avec l’espérance de vie du
patient et le risque opératoire [23]
. Une chirurgie préven-
tive ne peut se concevoir que si le risque opératoire est très
faible et que si l’intervention n’entraîne pas un surcroît de
risque ultérieur, notamment avec une prothèse valvulaire.
La faisabilité de la chirurgie valvulaire mitrale [12, 24] est
donc un élément essentiel dans la décision d’intervenir
précocement [25]. Le risque opératoire doit être estimé en
fonction des caractéristiques du patient à l’aide de scores
validés, comme l’Euroscore [26]. Les indications opératoi-
res au stade asymptomatique ne sont donc généralement
pas envisagées après 75 ans ou en cas de comorbidités
importantes. Par ailleurs, il est essentiel d’évaluer la faisa-
bilité de la plastie mitrale par échocardiographie lors
d’une confrontation médicochirurgicale prenant en
compte l’analyse échocardiographique détaillée de l’étio-
logie et du mécanisme de la régurgitation.
La chirurgie précoce proposée par Enriquez-Sarano
[20] est raisonnable mais l’attitude basée sur une sur-
veillance médicale clinique et échocardiographique
attentive de Rosenhek [21] est aussi envisageable. De ces
dernières études dérivent les dernières recommandations
sur l’IM sévère asymptomatique.
Recommandations
La place de la chirurgie prophylactique dans l’IM
asymptomatique, par prolapsus, chez un patient en
rythme sinusal, avec fonction ventriculaire gauche préser-
vée (FEVG > 60 %, DTSVG < 40 mm) avec haute proba-
bilité (> 90 %) de réaliser une plastie mitrale sans fuite
résiduelle, est encore discutée.
Cette chirurgie est classée IIa par l’ACC/AHA [6] avec
un niveau de preuve B ; et pour les Européens [1], cette
chirurgie est classée IIb, avec un niveau de preuve B. En
revanche, les auteurs [1, 6] ne recommandent pas la
chirurgie, dans ce contexte, (classe III) s’ilyaundoute
quant à la faisabilité d’une plastie mitrale (niveau de
preuve C).
En conclusion, à partir de ces données, nous avons
proposé un algorithme décisionnel dans la prise en charge
d’un patient avec IM asymptomatique.
Survie (%)
100
90
80
70
50
60
40
30
20
10
0
Globale
Prolapsus
Attendue
012345678
Figure 5. Courbes de survie sous traitement médical dans la série
de Rosenhek et al. La survie totale des patients porteurs d’une
insuffisance mitrale est non statistiquement différente de celle
attendue. D’après Rosenhek et al.Circulation 2006 ; 113 (18) :
2238-44.
mt, vol. 14, n° 1, janvier-février 2008 7
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
1
/
7
100%