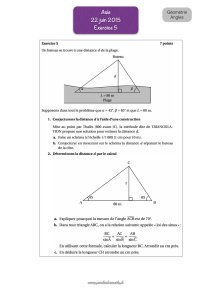
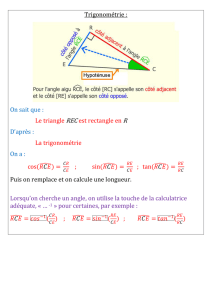
mouvement sans frottement sur un banc incline

- 1/5 -
CORRECTION EVALUATION COMMUNE PREMIERE S
I – MOUVEMENT SANS FROTTEMENT SUR UN BANC INCLINE
1) Bilan des forces : Poids :
P
Réaction du support :
R
=
N
R
+
T
R
Les forces de frottements étant négligeables
0RT
Donc
R
=
N
R
2) Système : le mobile Référentiel : le banc à coussin d’air
Appliquons le théorème de l’énergie cinétique entre A et B
)F(W extAB
=
)A(E)B(E CC
)P(WAB
+
)R(W NAB
=
)A(E)B(E CC
Or,
N
R
est perpendiculaire à AB donc
)R(W NAB
=
N
R
.
AB
= 0
De plus, la vitesse initiale au point A est nulle donc
m
2
1
)A(EC
0v 2
A
L’expression devient
)P(WAB
=
)B(EC
m
2
1
)zz(mg BA
2
B
v
Avec
m0zB
et
sinDzA
m
2
1
sinmgD
2
B
v
singD2vB
A.N. :
0,15sin50,281,92vB
=
1
s.m56,3
3) Appliquons le théorème de l’énergie cinétique entre B et S
)F(W extBS
=
)B(E)S(E CC
)P(WBS
+
)R(W NBS
=
)B(E)S(E CC
Or
N
R
est perpendiculaire à BS donc
)R(W NBS
= 0
De plus, le mobile redescend lorsqu’il a atteint le point le plus haut. C’est pourquoi, en ce point, sa
vitesse s’annule
1
Ss.m0v
Donc
J0)S(EC
L’expression littérale devient :
)P(WBS
=
)B(EC
au point B la vitesse est notée
O
v
m
2
1
zzmg sB
2
0
v
Or
0zB
et
sin.xz SS
mg
sinxS
=
m
2
1
2
0
v
singx2v S0
A.N. :
15sin25,181,92v0
=
1
s.m52,2

- 2/5 -
II – CHUTE DE GRELE
1°) Juste avant l’impact, le glaçon possède de l’énergie cinétique.
L’énergie cinétique est définie par : Ec = ½ . m1 . v2 A.N. : Ec = ½ . 5,0.10-3 . 12 = 2,5 mJ
2°) L’énergie récupérée pour la fusion de la glace représente 90 % de l’énergie cinétique du glaçon avant
l’impact : soit A.N. : = 2,25 mJ
3°) Le glaçon stocke cette énergie sous forme d’énergie d’agitation thermique.
4°) Le transfert énergétique permettant la fusion d’une masse m2 de glaçon est défini par :
Q = m2 . (Lf)eau soit A.N. : = 6,72 µg
5°) Puisque m2 << m1 , alors après l’impact, la masse du glaçon restera quasiment la même m3 = m1
6°) Si Ec = ½ . m1 . v2 , et Q = m1 . (Lf)eau alors = =
Soit A.N. : = 856 m.s-1 soit v = 3,1.103 km.h-1
III – SOLEIL ET PISCINE
1°) Le mode de transfert d’énergie mis en jeu est le transfert par rayonnement Wray.
2°) La puissance reçue par l’eau est définie par : Preçue = P × S soit Preçue = P × (L × ℓ)
A.N. : Preçue = 0,85 × (10 × 4) = 34 kW
3°) La puissance absorbée par l’eau est liée au pourcentage d’absorption :
Soit
L’énergie absorbée par l’eau est définie par : Wabsorbée = Pabsorbée × t
Soit
A.N. : = 1,7.108 J
4°) L’énergie absorbée par l’eau permettant d’en élever la température est définie par :
Wabsorbée = meau × (ceau)ℓ × soit =
A.N. : = = 0,51 °C

- 3/5 -
IV – TITRAGE CONDUCTIMETRIQUE
1) Facteur de dilution :
V
V
Ff
A.N. :
10
0,10
100
F
2) - On rince la pipette jaugée de 10 mL avec de l’eau distillée puis avec la solution mère d’acide
chlorhydrique.
- On prélève grâce à la pipette jaugée 10 mL d’acide chlorhydrique préalablement versé dans un
bécher
- On verse ce volume dans une fiole jaugée de 100 mL
- On ajoute de l’eau distillée au ¾ de la fiole
- On agite par retournements successifs
- On complète avec de l’eau distillée jusqu’au trait de jauge
3)
4)
OH3
=
HOH )l(2
HHO )aq(
=
OH2
)aq(
3HOOH
)l(2OH2
5) Graphiquement l’abscisse du point d’intersection des deux droites est le volume à l’équivalence
mL3,10VE
Solution titrante : Na+ + HO-
de volume VE
de concentration CS connue
Solution titrée H3O+ + Cl-
de volume Vf =100 mL
de concentration inconnue
burette
Bécher
Agitateur
magnétique
Sonde conductimétrique

- 4/5 -
Solution titrée H2O2
de volume Vf =10,0mL
de concentration C = ?
Solution titrante : K+ + MnO4-
de volume V1 = 19,6mL
de concentration C1 = 2,0.10-2mol.L-1
burette
Bécher
Agitateur
magnétique
6)
ClOHOHHCl 32
donc
CClOH3
OHNaNaOH
donc
S
CHONa
A l’équivalence tous les réactifs sont consommés.
0xCV Ef
fE VCx
0xVC EES
ESE VCx
ESf VCVC
f
ES
VVC
C
f
ES
OVVC
FCFC
A.N. :
1
3
3
OL.mol103,0
10.100 10.3,10100,0
10C
V – TITRAGE H2O2 PAR KMNO4
1)
e5H8MnO )aq(
)aq(
4
=
)2(OH4Mn )l(2
2)aq(
)aq(22OH
=
)5(e2H2O )aq()g(2
)aq()aq(4
)aq(
22 H16MnO2OH5
H10O5OH8Mn22)l(2
2)aq(
)aq()aq(4
)aq(
22 H6MnO2OH5
)g(2)l(2
2)aq(O5OH8Mn2
Equation
OH3
+
)aq(
HO
2H2O(l)
Etat
Avancement
Quantité de matière (en mol)
initial
0
C.Vf
CS.VE
Excès car solvant
intermédiaire
x
C.Vf - x
CS.VE - x
Excès car solvant
final
XE
C.Vf – xE
CS.VE – xE
Excès car solvant

- 5/5 -
4
OH
4MnOKKMnO 2
14 CMnOK
2)
1
V
est appelé volume à l’équivalence
Lorsque
1
V
a été introduit tous les réactifs sont consommés.
3)
4) donc
A l’équivalence, tous les réactifs sont consommés
0x2VC E11
2
VC
x11
E
0x5CV E
5
CV
xE
Donc
5
CV
2
VC 11
donc
V
5
2
VC
C11
A.N. :
12
3
32 L.mol10.8,9
10.0,102510.6,1910.0,2
C
Equation
2
)aq(MnO4
+ 6
)aq(H
+ 5
)aq(OH 22
2Mn2+ + 8H2O(l) + 5O2(g)
Etat
Avancement
Quantité de matière (en mol)
initial
0
C1.V1
Excès
C.V
0
Excès car
solvant
0
intermédiaire
x
C1.V1 - 2x
Excès
C.V - 5x
2x
Excès car
solvant
5x
final
xf
C1.V1 - 2xE
Excès
C.V - 5xE
2xE
Excès car
solvant
5xE
1
/
5
100%