Essais en adjuvant

Les essais cliniques
en sénologie
- Oncologie Médicale -
Décembre 2011
Institut Claudius Regaud
Mise à jour : 10.11.2012

Essais en adjuvant
→ICR , étude PHACS
→UNICANCER , étude APHINITY (HER2+)
→Roche : étude SAFEHER (HER2+)
→UNICANCER , étude GERICO 11/PACS 10 (≥70 ans, RE+,pN+)
Essais en néoadjuvant
Essais en métastatique
● tumeurs HER2 +
→AMGEN: AMG 386 (cohorte B)
→Roche PHEREXA
→Roche PERUSE
→Roche: T-DM1 phase I : insuffisance hépatique
→
Boehringer:
Afatinib + trastuzumab (phase I)
Les essais en cours
Décembre 2011
→
Boehringer:
Afatinib + trastuzumab (phase I)
● tumeurs triples négatives
→Bayer: étude Résilience
→NOVARTIS , étude BELLE 4 (1° ligne)
● tumeurs RH+ et HER2 neg
→Bayer: étude Résilience
→ICR, Oxytam
→ICR, étude miRHO
→NOVARTIS , étude BELLE 4 (1° ligne) +
→NOVARTIS , étude BELLE 2 (progression sous AI)
● tous types histologiques
→ICR, METAL 3
→Bayer, phase I Eribuline + sorafénib

Les essais cliniques
en adjuvant
Décembre 2011

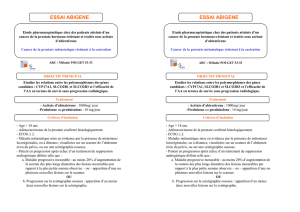
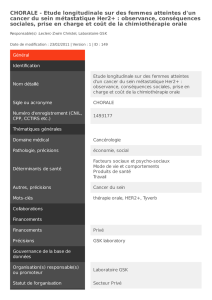
Protocole PHACS : Pharmacocinétique du tamoxifène et des
anti-aromatases, corrélation avec les caractéristiques
pharmacogénétiques.
Promoteur : Institut Claudius Regaud
PI : Henri Roché
Objectif principal : Évaluer les corrélations entre les paramètres
pharmacocinétiques et pharmacogénomiques des traitements hormonaux
adjuvant des cancers du sein (dans les 3 1° années)
Principaux critères d’inclusion :
- femme d’âge ≥18 ans
- carcinome infiltrant M0. Tout traitement antérieur par
chimiothérapie est permis, y compris par trastuzumab
- cancer RH+ (RE et/ou RP +)
- OMS ≤2
- avant l’initiation du traitement adjuvant par hormonothérapie (Tam,
Ana,
Létro
ou
Exém)
et
ce
quelque
soit
le
schéma
choisi
par
Décembre 2011
Ana,
Létro
ou
Exém)
et
ce
quelque
soit
le
schéma
choisi
par
l’investigateur (séquentiel ou non)
Principaux critères de non inclusion :
- patiente déjà traitée pour ce cancer du sein et recevant déjà une
hormonothérapie
Schéma de l’étude :
- les patientes reçoivent l’HT choisie par l’investigateur.
- avant le début du traitement : prélèvements sanguin pour
pharmacogénomie.
- avant le début du traitement puis tous les 6 mois pendant 3 ans :
prélèvements sanguins pour pharmacocinétique
- avant le début du traitement puis tous les 6 mois pendant 3 ans :
évaluation des effets secondaires par la patiente et l’investigateur
Autres centres ONCOMIP investigateurs :
- Clinique Saint Jean du Languedoc , CH de Montauban
- CH de Cahors, Clinique Pasteur Atrium et le CH de Rodez
- CH de Castres-Mazamet

Protocole APHINITY : Adjuvant Pertuzumab and Herceptin IN
Initial TherapY. Tumeurs HER2+
Promoteur : UNICANCER
Objectif principal : Comparer la survie sans maladie invasive entre les eux
bras (chimio + trastuzumab + placebo vs chimio + trastuzumab +
pertuzumab)
Principaux critères d’inclusion :
- femme d’âge ≥18 ans
- carcinome infiltrant M0.
- pN0 ou pN+ dès que la taille est > 10 mm
- Tumeurs HER2+ (ICH ou CISH)
- FEVg ≥55%
-Principaux critères de non inclusion :
- Tout T4
-
Antécédent
de
cancer
du
sein
invasif
Décembre 2011
-
Antécédent
de
cancer
du
sein
invasif
Schéma de l’étude :
- les patientes reçoivent soit une chimio par anthracycline puis taxane
(type FEC 100 puis TXT) soit du TCH de Slamon + le trastuzumab +/-
le pertuzumab.
- Le (ou les) anticorps monoclonaux est (sont) adminsitré(s) durant 1
an (18 injections) dès le taxane
- !! Relecture centralisée du statut HER2 (bloc)
- !! La randomisation doit avoir lieu au plus tard 7 semaines après la
chirurgie et le J1C1 au plus tard 8 semaines après la chirurgie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%