Examen 2005 2

CHIMIE ORGANIQUE II (CHM-19078) - Professeur Thierry Ollevier
Examen partiel n°2 - mercredi 23 mars 2005 (15h30-17h20)
Cet examen est d'une durée de 110 minutes. Inscrivez votre nom, prénom et code d'étudiant sur chacun des cahiers
d'examen que vous utilisez. Cet examen comporte 10 questions. Il est noté sur 100 points (10 points par question) et
constitue 30 % de la note globale du cours. Dans le cas de la question 5, retranscrivez clairement vos réponses dans
votre cahier d'examen.
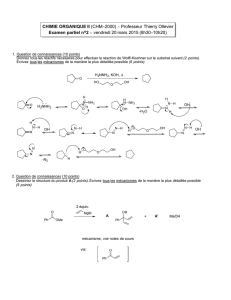
1. Question de connaissances (10 points)
Dessinez la structure du produit A
(2 points)
. Écrivez tous les mécanismes de la manière la plus détaillée possible
(8 points)
.
2. Question de connaissances (10 points)
Dessinez la structure du produit A
(1 point)
. Donnez le nom de la réaction
(1 point)
.
Écrivez tous les mécanismes de la manière la plus détaillée possible pour toutes les étapes
(8 points)
.
A
3. Question de connaissances (10 points)
Dessinez la structure du produit A
(3 points)
. Donnez le nom de la réaction
(1 point)
.
Écrivez tous les mécanismes de la manière la plus détaillée possible
(6 points)
.
4. Question de connaissances (10 points)
Dessinez la structure du produit A
(2 points)
. Écrivez tous les mécanismes de la manière la plus détaillée possible
en incluant les produits secondaires minéraux
(8 points)
.
NH2NH2, NaOH
diéthylène glycol
Δ
O
A
CO2HCH2N2
O
CH3CO3HA
OH
O
SOBr2A
5. Question de vrai ou faux (10 points)
Donnez la bonne réponse "vrai" ou "faux"
(2 points par question).
Indiquez votre réponse dans le cahier d'examen !
7.1. La réaction d'un ester avec 2 équivalents d'un réactif organolithien (RLi) est une réaction de réduction.
Vrai ou faux ?
7.2. La réduction d'un ester au DIBAL conduit toujours à l'alcool correspondant. Vrai ou faux ?
7.3. La transformation d'un acide carboxylique en chlorure d'acide par le chlorure de thionyle
est accompagnée d'un dégagement de monoxyde de carbone. Vrai ou faux ?
7.4. La diméthylamine réagit plus rapidement sur un ester dérivé de l'acide acétique que sur l'anhydride
acétique (dérivé de l'acide acétique). Vrai ou faux ?
7.5. L'hydrolyse d'un lactame conduit toujours à un acide aminé. Vrai ou faux ?

6. Question d'exercices (10 points)
Donnez la structure des produits
(2 points par produit)
des réactions suivantes.
Les mécanismes ne sont pas demandés.
6.1.
6.2.
A
B
HO H
O
O
1 équiv. CH3MgBr
OEt
O
1) 2 équiv.
MgBr
2) H2O
6.3.
Me OMe
O O 1) LiAlH4 en excès
2) H3O+
6.4.
Me OH
OPCl5
6.5.
n
Bu OH
O1) MeLi en excès
2) H3O+
C
D
E
7. Question d'exercices (10 points)
Donnez la structure des produits
(2 points par produit)
des réactions suivantes.
Les mécanismes ne sont pas demandés.
7.1.
7.2.
A
B
H O
O
7.3.
Me
t
Bu
OMCPBA
7.4.
7.5. EtONa
C
D
E
NH2
HN
O
O
1) LiAlH4
2) H2O
MeEtO
OO 1) NaBH4 en excès
2) H3O+
O
O
EtOH

8. Question d'exercices (10 points)
Donnez la structure des réactifs ou des produits manquants (A à E)
(2 points par réponse)
des réactions suivantes.
Les mécanismes ne sont pas demandés.
8.1.
8.2.
A
B
8.3.
8.4.
CD
E
MeO OSiMe2
t
Bu
O
1 équiv. DIBAL
Toluène, -90°C
O
OH
O
OH
O
Cl
1 équiv.
C4H4O3
C2H4O2
+
n
Bu NH2
n
Bu N
H
O
n
Bu N
H
HO CH3
OHO HBr
9. Question de raisonnement (10 points)
Écrivez un mécanisme détaillé pour les réactions suivantes
(5 points pour 9.1., 5 points pour 9.2.)
. S'il s'agit d'une
réaction nouvelle (9.2.), déduisez le mécanisme en fonction des principes généraux vus au cours.
Dessinez toutes les structures.
9.1.
NH2
MeO Me
O
O
H+ cat.
O
MeO Me
O
NH2
+ +
H2O
9.2.
NH
Me OMe
OH-
H2O
O
Me NH2
MeOH
+
10. Question de raisonnement (10 points)
Le composé B est un précurseur de l'acide scopadulcique qui possède une activité antivirale importante.
Dressez la liste dans l'ordre de toutes les réactions à effectuer pour passer du composé A au composé B.
Donnez les noms des réactions, dites de quelle transformation il s'agit et donnez en détail tous les réactifs nécessaires
pour chaque étape (par exemple : "étape d'estérification de Fischer : conversion d'un acide carboxylique en ester,
réactifs : alcool, H2SO4"). Les mécanismes ne sont pas demandés. Pour plus de clarté, dessinez les structures des
composés obtenus après chaque étape et discutez chacune des étapes dans l'ordre logique d'une synthèse
raisonnable à effectuer dans un laboratoire.
O O
OSiMe3
CN
BnO
OH
O2CPh
CO2Me
BnO
Plusieurs étapes
A B
Bn
1
/
3
100%