r - Canalblog

PRINCIPALES FONCTIONS
RENCONTRÉES EN BIOCHIMIE
H
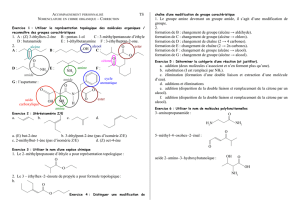
1 – FONCTION ALCOOL
R – C – OH
Alcool secondaire
(alcool II)
Alcool primaire
(alcool I)
R1 – C – OH
H
H
R2
La biochimie ne s’intéresse pas aux alcools tertiaires.
On retrouve des alcools I et II dans les oses, certains acides aminés…
1
C. Lacombe

- formation d’ester avec un acide par élimination
d’une molécule d’eau : exemple, les glycérides
1 – FONCTION ALCOOL
2
C.#Lacombe#

oxydation : dans les organismes, elle se fait généralement
progressivement
R – CH2OH R – CHO R – CH R – C – OH
Alcool I Aldéhyde Acétal Acide
instable carboxylique
R – CHOH – R’ R – C – R’
Alcool II Cétone
-H2 +H2O -H2
OH
OH
-H2
O
1 – FONCTION ALCOOL
3#
C.#Lacombe#
O

- formation d’un éther entre 2 molécules d’alcool par
élimination d’une molécule d’eau :
R – OH + HO – R’ R – O – R’ +H2O
éther
1 – FONCTION ALCOOL
4#
C.#Lacombe#

2 - FONCTIONS ALDÉHYDE ET CÉTONE
aldéhyde : R – C cétone : R – C – R’
Ces deux fonctions se retrouvent particulièrement
dans les oses
- oxydation
R – CHO R – CH R – COOH
O
H
O
+H2O -H2
OH
OH
aldéhyde acétal instable acide carboxylique
5
C. Lacombe
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%