I. Présentation
1. Définition
Un acide α-aminé ou α-aminoacide est un composé possédant deux groupes fonctionnels, l’un acide (-
COOH), l’autre amine (-NH2), fixés sur un même atome de carbone.
Sa formule générale s’écrit :
Dans cette formule, R n’est pas toujours un groupement alkyle mais peut contenir un noyau aromatique,
un atome de soufre ou des groupements fonctionnels tels que : alcool, amine, acide carboxylique…..
2. nomenclature
Pour nommer Les acides α-Aminés, on recherche le nom de l’acide carboxylique de même squelette
carboné, puis on intercale le mot << 2-amino >> après le mot <<acide >>. Exemples :
II. éléments de Stéréochimie
1. Carbone asymétrique
C’est un carbone tétragonal lié à quatre atomes ou groupements tous différents. On le repère
habituellement par un astérisque (*) C*.
2. Chiralité
Une molécule chirale est une molécule qui n’est pas superposable à son image dans un miroir plan. Une
molécule, ou un objet, qui possède un centre ou un plan de symétrie n’est pas chiral.
3. Enantiomères
Deux isomères de configuration sont dits énantiomères s’ils sont des images l’un de l’autre dans un miroir
plan et non superposables.

Une molécule comportant plusieurs atomes de carbone asymétriques peut être achirale.
Un mélange racémique est constitué de quantité égale de molécules de deux énantiomères.
Activité optique : c’est l’aptitude d’une molécule à dévier la lumière.
4. Représentation spatiale
La représentation de Cram permet une schématisation rapide des carbones tétraédriques en utilisant les
conventions suivantes :
liaison dans le plan de la figure
liaison vers l’avant
liaison vers l’arrière
C
O
OH
CH2
NH2
Glycine
C
représentation de Cram d’un carbone tétraédrique
représentation de Cram de la glycine
5. Représentation de Fischer et configuration D ou L
Conventions à connaître :
La molécule est représentée en forme de croix avec le carbone porteur des fonctions amines et acides
au milieu
Le groupe COOH en haut, le groupe R en bas
Les traits verticaux représentent des liaisons vers l’arrière, les traits horizontaux représentent des
liaisons vers l’avant.
Il existe deux types de configuration D ou L : Quand le groupe amine est à droite c’est la configuration D.
CO2H
H NH2
R
Quand le groupe amine est à gauche c’est la configuration L.
CO2H
NH2H
R
III. propriétés
1. Amphion ou Zwittérion
La dissolution d’un acide α-aminé dans l’eau est suivie d’une réaction acido-basique intramoléculaire :
Une telle solution contient principalement un ion dipolaire appelé Zwittérion ou Amphion :

On l’interprète comme un transfert de proton H+ du groupe –COOH au groupe –NH2.
Dans la suite du cours le Zwittérion sera noté Z pour nous affranchir de la lourdeur d’écriture.
2. Acido-basicité
3. Domaines de prédominance
Remarque : pHi isoélectrique
il existe un pH appelé pH
isoélectrique où la concentration en ion zwittérion est maximale.
En ce point
4. Liaison peptidique
a. Définition
Les acides aminés peuvent se lier les uns aux autres par une liaison peptidique. La liaison peptidique se fait entre
le groupement acide (COOH) d'un acide aminé et le groupement amine (NH2) de l'autre. Au cours de la réaction,
une molécule d'eau est éliminée. Il s'agit donc encore une fois d'une réaction de condensation.
L'union de plusieurs acides aminés forme un polypeptide

Exemple
Considérons un mélange équimolaire de deux acides α-aminés, la condensation entre ces deux peut se
faire de différentes manières et on obtient en milieu quatre dipeptides différents.
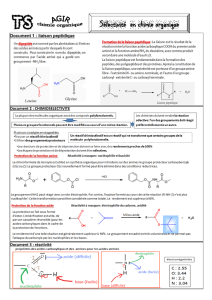
b. Synthèse sélective
Si on veut obtenir un seul dipeptide (par exemple HGly-AlaOH ou glycine terminal N) à partir d’un mélange
équimolaire de glycine et d’alanine, on doit empêcher les autres réactions (2,3 et 4) qui sont des réactions
parasites pour cette synthèse. Pour cela, il faut bloquer les groupes qui ne participent pas à la réaction et
activer les groupes qui y participent.
1ère étape : blocage du groupe –COOH de l’alanine en le transformant en ester.
2ème étape : blocage du groupe –NH2 de la glycine en le transformant en amide.

3ème étape : activation du groupe –COOH de la glycine en le transformant en chlorure d’acyle
4ème étape : formation de la liaison peptidique
5ème étape : régénération des groupes bloqués
c. Protéine
Ce sont des macromolécules formées par l’enchainement d’acides α-aminés reliés entre eux par une
peptidique.
Les protéines sont des molécules très variées. Notre organisme en fabriquerait quelque chose comme 100
000 différentes les unes des autres. Chacune de ces protéines a une forme tridimensionnelle et des
propriétés chimiques qui lui sont propres. Les protéines remplissent de nombreux rôles dans la cellule.
1
/
5
100%