Récidives locales après traitement du cancer du sein : implications

diagnostiquées. Toutes ces patientes ont été régulièrement sui-
vies au centre : tous les six mois pendant cinq ans, puis annuel-
lement, et faisaient des mammographies bilatérales annuelles.
Dans 77 % des cas, le diagnostic de récidive a été porté à l’occa-
sion d’une visite programmée, et, dans 23 % des cas, entre deux
examens, soit par les patientes elles-mêmes, soit par leur méde-
cin gynécologue ou généraliste. Cette proportion était constante
tout au long de la période de suivi, y compris après 10 ans.
Site de récidive
De façon un peu artificielle, on sépare les récidives survenant
dans le site tumoral initial (dans le même quadrant) ou à proxi-
mité, et les récidives survenant à distance dans le sein.
Selon le recul, la proportion de ces deux types varie, les réci-
dives dans le même quadrant étant plus fréquentes dans les cinq
premières années de suivi. À 15 ans, les proportions s’équili-
brent, les récidives survenant pour moitié dans le même site et
pour moitié ailleurs, dans le sein traité (2).
Cinétique et variations du risque de récidive
Le risque annuel n’est pas constant au cours du temps. Il a ten-
dance à augmenter durant les quatre ou cinq premières années
après le traitement, puis il décroît progressivement pour devenir
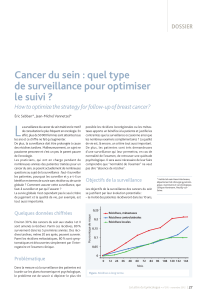
constant vers la dixième année. Cette variation est illustrée par la
figure 1. Durant les premières années, elle dépend des facteurs de
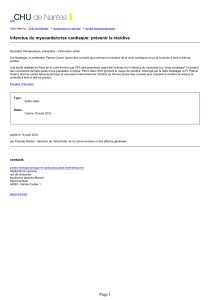
risque initiaux, dominés par l’âge au diagnostic : plus l’âge est
jeune, plus le risque est élevé (figure 2), et cette variation est pra-
tiquement linéaire. Outre le facteur de l’âge, le risque est augmenté
dans les tumeurs de haut grade, de prolifération élevée, en
l’absence de récepteurs hormonaux et en présence d’emboles vas-
culaires péritumoraux. Ces éléments doivent être pris en compte
dans l’adaptation des protocoles de suivi.
Les traitements associés ont également une influence sur le
risque de rechute : l’absence de berges saines après chirurgie
augmente le risque. Les traitements médicaux (chimiothérapie,
hormonothérapie) contribuent à réduire le risque de récidive.
L
e suivi des patientes traitées pour un cancer du sein a
plusieurs objectifs : détecter une rechute locorégionale,
controlatérale ou métastatique, prendre en charge les
complications et les séquelles éventuelles du traitement, évaluer
les résultats à long terme.
Le suivi locorégional est fondé sur un examen clinique et des
mammographies effectuées à intervalle régulier. La fréquence et
la durée des examens de suivi ont été établies de façon empirique,
et leur impact sur l’évolution de la maladie est mal connu.
L’adaptation de ces modalités de suivi aux critères de risque et au
pronostic est mal évaluée. La mise en pratique de ce suivi peut
varier beaucoup en fonction des habitudes des centres, de l’impli-
cation des médecins libéraux, et de l’information des patientes.
Nous envisagerons successivement les caractères des récidives
mammaires et controlatérales, l’efficacité de la détection systé-
matique et l’impact pronostique du suivi des patientes.
RÉCIDIVES MAMMAIRES HOMOLATÉRALES
APRÈS TRAITEMENT CONSERVATEUR DU SEIN
Le traitement conservateur associe une chirurgie d’exérèse de la
tumeur mammaire primitive avec des berges saines, suivie
d’une radiothérapie de l’ensemble de la glande mammaire (1).
Fréquence
Le risque de récidive homolatérale est en moyenne de 1% par an.
Le risque cumulé augmente avec le temps et n’atteint jamais de
plateau, les patientes restant exposées toute leur vie à ce risque.
Diagnostic des récidives locales
Le diagnostic d’une récidive locale est parfois difficile, surtout
lorsque le sein est dense et modifié par le traitement. La compa-
raison des examens cliniques systématiques et de l’imagerie
(mammographie, échographie) avec les examens précédents
permet de détecter des modifications qui ne sont pas toujours
spécifiques (masse palpable, opacité spiculée, microcalcifica-
tions). La suspicion d’une récidive doit conduire à effectuer des
prélèvements cytologiques ou biopsiques, guidés par l’imagerie.
Le tableau I montre les résultats d’une étude effectuée à l’insti-
tut Curie, sur 2 850 patientes suivies pendant une période
médiane de 12 ans, chez qui 386 récidives mammaires ont été
DOSSIER
7
La Lettre du Sénologue - suppl. 1 au n° 29 - juillet-août-septembre 2005
Récidives locales après traitement du cancer du sein :
implications pour le suivi des patientes traitées
Patterns of local recurrences after treatment of breast cancer: implications for follow-up
●A Fourquet
1
, A Renard
1
, A Savignoni
2
, A. de la Rochefordière
1
, R.J. Salmon
3
pour le Groupe d’étude des cancers du sein
Mots-clés : Cancer du sein, Récidive locale, Pronostic, Suivi.
Keywords: Breast cancer, Local recurrence, Prognosis, Follow-up.
*Départements de radiothérapie, institut Curie, Paris.
** Département biostatistiques, institut Curie, Paris.
*** Département chirugie, institut Curie, Paris.
Période de suivi (ans) Circonstances de diagnostic (%)
Suivi programmé Intervalle
0-5 79 21
5-10 74 26
> 10 77 23
Ensemble 77 23
Tableau I. Circonstances de la découverte des récidives locales après
traitement conservateur du sein à l’institut Curie.

Traitement des récidives locales
Le traitement standard d’une récidive survenant dans le sein
irradié est la mastectomie. Des tentatives de second traitement
conservateur ont été effectuées, avec ou sans réirradiation : ces
études portent sur de petits effectifs sélectionnés (faible taille de
la récidive, carcinome in situ) et font état de taux de deuxième
rechute élevés. Une réirradiation du sein à doses efficaces
expose à un risque élevé de séquelles.
Pronostic des récidives locales
Dans la série de l’institut Curie, la survie après diagnostic d’une
récidive était de 65 % à 10 ans, et la survie sans métastase de
56 %. Ces taux sont comparables à ceux d’autres études portant
sur de grandes séries de patientes (tableau II).
La question de savoir si la survenue d’une récidive locale a une
influence sur le risque métastatique et la survie des patientes a
longtemps été débattue. Globalement, la comparaison entre le taux
de survie des patientes qui ont eu une récidive locale et le taux de
celles qui n’en ont pas eu a donné des résultats contradictoires,
certaines études ne montrant pas de différence, d’autres mettant en
évidence une survie moins bonne chez celles qui avaient récidivé.
Les différences observées dans ces études tiennent avant tout aux
différences de recul de patientes traitées: les études avec un long
recul montraient moins souvent une différence (2).
De multiples facteurs interviennent dans le pronostic des réci-
dives locales, liés aux caractéristiques de la tumeur primitive, à
celles de la récidive locale et aux traitements de la récidive. Le
tableauIII montre les résultats de l’analyse multifactorielle du
risque de métastase chez les 386 patientes qui avaient une réci-
dive locale isolée. La précocité de la récidive (moins de 2 ans)
et un grade élevé sont logiquement associés à un risque métasta-
tique élevé. La détection précoce d’une récidive de petite taille
est associée à un moindre risque, de même que sa localisation
dans un autre site que la tumeur initiale. Cela se retrouve égale-
ment dans le risque de décès, où la survenue d’une récidive non
palpable (détectée par l’imagerie) et dans un autre site est asso-
ciée à une meilleure survie. Ces observations ont également été
rapportées dans d’autres études : selon les paramètres étudiés, y
sont retrouvés comme facteurs péjoratifs, la précocité de la réci-
dive locale (5, 6, 8-12) et, comme facteur favorisant, d’une part,
la détection à un stade précoce (cancer in situ, tumeur supé-
rieure à 1 cm, tumeur non palpable [13]), d’autre part, la surve-
nue dans un autre site.
RÉCIDIVE LOCALE APRÈS MASTECTOMIE
Le risque de survenue d’une récidive sur la paroi thoracique varie
de 0,5 à 1,5% par an. Ces récidives se manifestent le plus souvent
par des tumeurs palpables, souvent enchâssées dans le derme,
proches de la cicatrice de mastectomie. Elles peuvent prendre
l’aspect de nodules de perméation, avec un aspect inflammatoire
ou ulcéré. Elles sont parfois multiples et confluentes.
Le risque de récidive pariétale est déterminé par :
–les caractéristiques de la tumeur mammaire primitive (taille,
DOSSIER
8
La Lettre du Sénologue - suppl. 1 au n° 29 - juillet-août-septembre 2005
Nombre Nombre Suivi Taux Survie
Auteur de de médian après estimé (%)
patientes récidives récidive (mois) à
Van Tienhoven (3) 851 67 74 5 ans 59
Fowble (4) 1030 65 24 5 ans 73
Galper (5) 2102 341 85 5 ans 81
Kurtz (6) 1245 52 72 10 ans 64
Haffty (7) 973 73 85 10 ans 71
Institut Curie 2 850 386 85 10 ans 65
Tableau II. Survie après récidive mammaire homolatérale. Données de
la littérature.
Paramètres Variables Risque relatif p
Premier cancer
–ganglions axillaires pN1 vs pN0 2,29 0,0001
–grade II-III vs I 2,23 0,008
Récidive mammaire
–grade III vs I 3,06 0,003
–délai (ans) ≤2 vs >2 2,62 0,0005
–taille (mm) > 15 vs ≤15 2,24 0,0002
–localisation Même site vs autre 1,5 0,06
Tableau III. Analyse multifactorielle du risque de métastase après réci-
dive mammaire à l’institut Curie : 386 récidives, recul médian : 85 mois.
001015
0
3,0
2,5
2,0
1,5
1,0
0,5
Récidives annuelles (%)
Intervalle (ans)
Figure 1. Variations annuelles du risque de récidive mammaire à l’insti-
tut Curie : 2 209 patientes, 303 récidives, suivi médian : 9,5 ans, courbes
lissées.
15
12
9
6
3
0
0123 45 678910
Intervalle (ans)
%
Âge 23-35 ; n = 128
Âge 36-40 ; n = 226
Âge 41-55 ; n = 1 071
Figure 2. Variations annuelles du risque de récidive en fonction de l’âge
au diagnostic à l’institut Curie : 1 424 patientes non ménopausées, suivi
médian : 10 ans.

–être fondé sur un examen clinique et des mammographies
bilatérales effectuées dans les mêmes conditions, permettant
ainsi des comparaisons systématiques ;
–être adapté aux facteurs de risques initiaux, aux traitements et
au délai écoulé depuis le traitement du cancer du sein initial ;
–être prolongé durant la vie entière.
Ce suivi doit comporter un examen clinique tous les six mois pen-
dant cinqans, puis annuel durant toute la vie, et des mammogra-
phies annuelles, bilatérales en cas de traitement conservateur du
sein et unilatérale en cas de mastectomie (1). Ce schéma doit être
modifié, surtout dans les cinq premières années après le diagnos-
tic, afin de prendre en compte les variations du risque annuel. ■
R
ÉFÉRENCES
B
IBLIOGRAPHIQUES
1.Mauriac L. Standards, options et recommandations: cancers du sein infiltrants
non métastatiques [2eédition, mise à jour, version abrégée]. Bull Cancer
2002;89(2):207-24.
2.Freedman GM, Anderson PR, Hanlon AL et al. Pattern of local recurrence
after conservative surgery and whole-breast irradiation. Int J Radiat Oncol Biol
Phys 2005;61(5):1328-36.
3.Van Tienhoven G, Voogd AC, Peterse JL et al. Prognosis after treatment for
loco-regional recurrence after mastectomy or breast conserving therapy in two
randomised trials (EORTC 10801 and DBCG-82TM). EORTC Breast Cancer
Cooperative Group and the Danish Breast Cancer Cooperative Group. Eur J
Cancer 1999;35(1):32-8.
4.Fowble B, Solin LJ, Schultz DJ et al. Breast recurrence following conservative
surgery and radiation: patterns of failure, prognosis, and pathologic findings
from mastectomy specimens with implications for treatment. Int J Radiat Oncol
Biol Phys 1990;19(4):833-42.
5.Galper S, Blood E, Gelman R et al. Prognosis after local recurrence after
conservative surgery and radiation for early-stage breast cancer. Int J Radiat
Oncol Biol Phys 2005;61(2):348-57.
6.Kurtz JM, Amalric R, Brandone H et al. Local recurrence after breast-conser-
ving surgery and radiotherapy. Frequency, time course, and prognosis. Cancer
1989;63(10):1912-7.
7.Haffty BG, Fischer D, Beinfield M, McKhann C. Prognosis following local
recurrence in the conservatively treated breast cancer patient. Int J Radiat Oncol
Biol Phys 1991;21(2):293-8.
8.Fourquet A, Campana F, Zafrani B et al. Prognostic factors of breast recurrence
in the conservative management of early breast cancer: a 25-year follow-up. Int J
Radiat Oncol Biol Phys 1989;17(4):719-25.
9.Veronesi U, Marubini E, Del Vecchio M et al. Local recurrences and distant
metastases after conservative breast cancer treatments: partly independent
events. J Natl Cancer Inst 1995;87(1):19-27.
10.Haffty BG, Reiss M, Beinfield M et al. Ipsilateral breast tumor recurrence as
a predictor of distant disease: implications for systemic therapy at the time of
local relapse. J Clin Oncol 1996;14(1):52-7.
11.Touboul E, Buffat L, Belkacemi Y et al. Local recurrences and distant
metastases after breast-conserving surgery and radiation therapy for early
breast cancer. Int J Radiat Oncol Biol Phys 1999;43(1):25-38.
12.Schmoor C, Sauerbrei W, Bastert G, Schumacher M. Role of isolated locore-
gional recurrence of breast cancer: results of four prospective studies. J Clin
Oncol 2000;18(8):1696-708.
13.Voogd AC, van Tienhoven G, Peterse HL et al. Local recurrence after breast
conservation therapy for early stage breast carcinoma: detection, treatment, and
outcome in 266 patients. Dutch Study Group on Local Recurrence after Breast
Conservation (BORST). Cancer 1999;85(2):437-46.
14.Group EBCTC. Favourable and unfavourable effects on long-term survival of
radiotherapy for early breast cancer: an overview of the randomised trials. Early
Breast Cancer Trialists’ Collaborative Group. Lancet 2000;355(9217):1757-70.
15.De la Rochefordiere A, Mouret-Fourme E, Asselain B et al. Metachronous
contralateral breast cancer as first event of relapse. Int J Radiat Oncol Biol Phys
1996;36(3):615-21.
16.Ciatto S, Miccinesi G, Zappa M. Prognostic impact of the early detection of
metachronous contralateral breast cancer. Eur J Cancer 2004;40(10):1496-
501.
9
La Lettre du Sénologue - suppl. 1 au n° 29 - juillet-août-septembre 2005
envahissement ganglionnaire axillaire, extension cutanée ou
musculaire profonde) constituent les critères classiques de risque
de récidive et d’indication d’une radiothérapie pariétale. À ces
critères s’ajoutent un âge jeune, des caractéristiques tumorales
“agressives” (grade élevé, prolifération élevée, absence de récep-
teurs hormonaux, emboles vasculaires) ;
–les traitements reçus : la radiothérapie pariétale diminue le
risque de récidive pariétale des deux tiers à 20 ans (14). La chi-
miothérapie et l’hormonothérapie adjuvante réduisent également
le risque de récidive locale.
Les récidives pariétales sont associées à un risque métastatique
plus élevé que les récidives après traitement conservateur du
sein. La probabilité de survie à 5 ans après une récidive pariétale
est en moyenne de 50 % d’après les études publiées, avec un
risque de métastases secondaires qui varie de 40 à 70 %. Ce
risque dépend du délai d’apparition de la récidive (les récidives
précoces sont de plus mauvais pronostic), de son caractère isolé
ou associé à une récidive ganglionnaire, du nombre de nodules
de récidive, de leur caractère inflammatoire ou non et des traite-
ments de la récidive.
CANCER DU SEIN CONTROLATÉRAL
Les femmes qui ont eu un cancer du sein ont un risque accru
d’avoir un cancer dans l’autre sein. Ce risque varie de 0,5 à 1%
par an selon les études et est en moyenne de 0,8% par an (15). Il
est augmenté chez les femmes jeunes, chez les femmes qui ont un
risque familial ou génétique de cancer du sein et chez celles qui
ont un cancer du sein lobulaire (16). Le risque est diminué par les
traitements adjuvants (chimiothérapie et hormonothérapie).
Les cancers du sein controlatéraux dépistés lors du suivi régulier
du premier cancer sont diagnostiqués à un stade plus précoce
que le primitif. Le pronostic des cancers controlatéraux est plus
défavorable lorsqu’ils sont diagnostiqués à un stade de tumeur
palpable. Le délai d’apparition du cancer controlatéral constitue
également un facteur de risque, la survenue précoce ayant un
pronostic plus péjoratif.
Le suivi régulier et le dépistage des cancers du sein controlaté-
raux par mammographie ont donc un impact certain sur la détec-
tion précoce de ces cancers et sur leur pronostic vital.
CONCLUSION : PROTOCOLE DE SUIVI
Le suivi régulier des femmes traitées pour un cancer du sein per-
met un diagnostic précoce des récidives locales (sein conservé ou
paroi thoracique) et d’un cancer controlatéral. Il est démontré que
ce diagnostic précoce a une influence sur la survie à long terme.
Le risque annuel moyen de survenue d’un événement local (réci-
dive ou controlatéral) chez une femme traitée pour un cancer du
sein peut être estimé à environ 1,8% par an, soit un risque cumulé
de 36% à 20 ans. Ce risque varie en fonction de multiples facteurs
liés à l’âge, au diagnostic et à l’existence de facteurs de risques
familiaux et génétiques, aux caractéristiques de la tumeur primi-
tive et aux traitements reçus. Il justifie d’un véritable dépistage
secondaire qui doit suivre les principes suivants:
–être systématique et régulier ;
1
/
3
100%