Cancers du sein avec atteinte ganglionnaire : suivi à long terme de l

24 | La Lettre du Sénologue • n° 48 - avril-mai-juin 2010
San Antonio Breast Cancer Symposium 2009
DOSSIER THÉMaTIQUE
Cancer du sein avec atteinte
ganglionnaire : suivi à long
terme de l’étude PACS 01 (FNCLCC)
Breast cancer with ganglion syndrome: PACS 01 study
B. Coudert1, M. Campone2, M. Spielmann3, L.N. Syman4, F. Eichler5, D. Serin6, T. Delozier7,
G. Romieu8, J.L. Canon9, H. Orfeuvre10, G. Piot11, T. Petit12, P. Chollet13, G. Jerusalem14,
B. Audhuy15, C. Veyret16, X. Beaudouin17, J.C. Eymard18, A.L. Martin19, H. Roché20
L
’objectif de cette analyse était de définir le
bénéfice à 8 ans en termes de survie sans réci-
dive (SSR) et de survie globale (SG) de l’admi-
nistration séquentielle de docétaxel après 3 cycles
de FEC 100 chez des patientes ayant un cancer du
sein avec atteinte ganglionnaire.
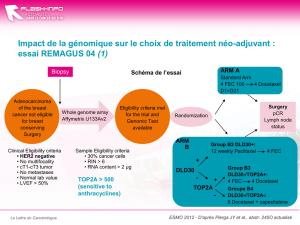
Les patientes opérées non prétraitées étaient rando-
misées pour recevoir soit 6 cycles de FEC 100, soit
3 cycles de FEC 100 suivis de 3 cycles de docétaxel.
La radiothérapie était obligatoire après chirurgie
conservatrice, et l’hormonothérapie était donnée
pour 5 ans si un des deux récepteurs hormonaux était
positif. Les autres critères d’inclusion étaient l’âge
inférieur à 65 ans, l’atteinte d’au moins un ganglion,
l’absence de métastase, et des fonctions cardiaque,
hématologique et rénale normales.
L’objectif principal de cette étude de phase III, multi-
centrique, ouverte, prospective et randomisée était la
survie sans récidive à 5 ans. Les résultats à 5 ans ont
déjà été publiés (1).
Entre juin 1997 et mars 2000, 1 999 patientes avaient
été recrutées. Leurs caractéristiques principales étaient
bien réparties selon les deux groupes de traitement
concernant l’âge, la chirurgie conservatrice, le grade 3,
les récepteurs hormonaux négatifs, l’atteinte ganglion-
naire de grade 1 à 3. Les traitements ont été complets
pour 95 % et 93,4 % des patientes dans les bras A et
B respectivement.
Avec un suivi médian de 92,8 mois, 639 femmes
ont expérimenté au moins un événement : 124 réci-
dives locales ou locorégionales, 421 métastases, 68
cancers du sein controlatéral et 26 décès. Au total,
71 seconds cancers et 383 décès ont été enregistrés.
La SSR à 8 ans était de 65,8 % avec 6 FEC 100, et
de 70,2 % avec 3 FEC 100-3 docétaxel. La régres-
sion multivariée ajustée pour l’âge et le nombre
de ganglions positifs a montré une réduction de
15 % dans le risque de récidive avec 3 FEC 100-3
docétaxel. Les taux de survie à 8 ans ont été de
78 % avec 6 FEC 100 et de 83,2 % avec 3 FEC 100-3
docétaxel. L’analyse multivariée ajustée sur l’âge
avec un nombre de ganglions positifs a montré une
réduction de 25 % dans le risque relatif de décès
avec 3 FEC 100-3 docétaxel. L’analyse en sous-
groupe montre toujours une réduction du risque
en faveur de 3 FEC100-3 docétaxel : diminution
du risque de récidive de 18 % pour les femmes de
moins de 50 ans et de 24 % pour les femmes de
plus de 50 ans ; diminution du risque de récidive de
15 % pour l’atteinte ganglionnaire de grade 1 à 3
et de 17 % pour l’atteinte ganglionnaire supérieure
à 4 ; diminution du risque de décès de 19 % pour
les femmes de moins de 50 ans et de 30 % pour
les femmes de plus de 50 ans ; diminution de 32 %
pour l’atteinte ganglionnaire de grade 1 à 3 et de
19 % pour l’atteinte ganglionnaire supérieure à 4.
Au final, à 8 ans, le schéma 3 FEC 100-3 docétaxel
permet une réduction du risque de survie sans réci-
dive et du risque de décès chez les patientes opérées
d’un cancer du sein avec atteinte ganglionnaire.
La conclusion de cet abstract confirme à 8 ans le
bénéfice déjà rapporté à 5 ans en termes de SSR
et de SG par l’adjonction de docétaxel au FEC100.
Le bénéfice en termes de SSR et de SG par l’adjonc-
tion des taxanes aux anthracyclines dans les traite-
ments adjuvants des cancers du sein a été confirmé
par plusieurs méta-analyses, dont la dernière est
celle de De Laurentiis et al. (2). Les résultats du
PACS 01 vont donc dans le même sens, avec des
bénéfices qui se confirment avec le temps. ■
1. Centre Georges-François Leclerc,
Dijon. 2. Centre René-Gauducheau,
Saint Herblain. 3. Institut Gustave-
Roussy,Villejuif. 4. Clinique universi-
taire St-Luc, Belgique.
5. CHRU Strasbourg. 6. Institut
Sainte-Catherine, Avignon. 7. Centre
François-Baclesse, Caen. 8. Centre
Val-d’Aurelle, Montpellier. 9. Grand
hôpital Charleroi, Belgique.
10. CH Fleyriat, Bourg-en-Bresse.
11. CMC Les Ormeaux, Le Havre.
12. Centre Paul-Strauss, Strasbourg.
13. Centre Jean-Perrin, Clermont-
Ferrand. 14. CHU Sart-Tilman,
Belgique. 15. CH Colmar. 16. Centre
Henri-Becquerel, Rouen. 17. Hôpital
Jolimont, Belgique. 18. Institut
Jean-Godinot, Reims. 19. Fédération
nationale des centres de lutte contre
le cancer. 20. Institut Claudius-
Regaud, Toulouse.
Références
bibliographiques
1. Roché H, Fumoleau P, Spiel-
mann M. Sequential adjuvant
epirubicin-based and docetaxel
chemotherapy for node-posi-
tive breast cancer patients: the
FNCLCC PACS 01 Trial. J Clin Oncol
2006;24(36):5664-71.
2. De Laurentiis M, Cancello G,
D’Agostino D et al. Taxane-based
combinations as adjuvant chemo-
therapy of early breast cancer: a
meta-analysis of randomized trials.
J Clin Oncol 2008; 26:44-53.
1
/
1
100%