Les effets secondaires des nouveaux traitements du cancer du rein

Les effets secondaires
des nouveaux traitements
du cancer du rein
Irène Asmane, Philippe Barthélémy, Stefano Kim, Brigitte Duclos,
Jean-Pierre Bergerat, Jean-Emmanuel Kurtz
Département d’hématologie et d’oncologie, Hôpitaux universitaires de Strasbourg,
1 Avenue Molière, 67098 Strasbourg Cedex
Le cancer du rein avancé a longtemps été considéré comme une tumeur de très mauvais
pronostic, en raison du manque de thérapeutiques efficaces, ou de leur toxicité rédhibitoire,
particulièrement pour l’immunothérapie. Ces dernières années ont été marquées par l’avène-
ment des thérapeutiques ciblées, comprenant d’une part des anticorps monoclonaux (beva-
cizumab), et d’autre part des petites molécules, ciblant les récepteurs à tyrosine kinase (suni-
tinib et sorafenib) ou la protéine mTOR (temsirolimus). Ces traitements innovants ont
profondément modifié notre stratégie thérapeutique dans cette affection, mais entraînent
par ailleurs un nouveau spectre d’effets secondaires. Dans cette revue, nous décrivons l’arse-
nal des thérapeutiques ciblées dont nous disposons à ce jour dans le cancer du rein dans le
cadre de l’AMM, en précisant leur mode d’action et leur indication. Nous décrivons leur
profil de toxicité, les conseils de prise en charge au quotidien tant pour l’oncologue que
pour l’omnipraticien, dans le but d’améliorer leur tolérance, la compliance des patients,
garants d’une efficacité maximale.
Mots clés : cancer du rein, thérapie ciblée, antiangiogénique
Le carcinome rénal à cellules
conventionnelles est d’emblée
métastatique dans 30 % des cas,
avec une médiane de survie globale
de 12 mois quand il est traité par l’as-
sociation interleukine2 (Il-2) et
interféron-α(IFNα) [1]. L’avènement
des thérapeutiques ciblées a révolu-
tionné la prise en charge de ces
patients, amélioré leur survie au prix
d’effets secondaires distincts de ceux
de l’immunothérapie. Il existe actuel-
lement plusieurs de ces nouveaux
agents dans le traitement du carci-
nome rénal à cellules conventionnel-
les métastatique (CRM). La stratégie de
leur utilisation répond à des critères
pronostiques, mais tient également
compte de leur profil de toxicité. En
effet, l’introduction des thérapies
ciblées a entraîné l’apparition d’un
nouveau spectre d’effets indésirables,
qu’il est important de connaître pour
optimiser la prise en charge quoti-
dienne de ces patients. Outre les indi-
cations actuelles dans le cadre de
l’AMM, nous présentons ici les princi-
pales toxicités de ces traitements dans
le cancer du rein métastatique, ainsi
que les mesures permettant de les pré-
venir ou de les atténuer.
Quels sont les facteurs
pronostiques du CRM ?
Pour Motzer et al., ces facteurs
pronostiques sont mixtes : cliniques
et biologiques (tableau 1) [2]. À
l’aide de ces critères, l’équipe du
MSKCC (Memorial Sloan Kettering
Cancer Center) a identifié trois grou-
pes de patients : bon pronostic (0 fac-
teur sur 5) ; pronostic intermédiaire
(1 à 2 facteurs sur 5) et mauvais pro-
nostic (plus de 2 facteurs sur 5) [2-4].
m
t
Tirés à part : J.-E. Kurtz
doi: 10.1684/met.2008.0175
mt, vol. 14, n° 5-6, septembre-décembre 2008
Dossier
277
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

De quels agents disposons-nous
et quelles sont leurs indications ?
Première ligne thérapeutique
Sunitinib
Le sunitinib (Sutent
®
) est un inhibiteur de récepteurs à
activité tyrosine kinase (RTK), dont les VEGFR-2, PDGFR,
FLT-3 et c-KIT, entraînant un effet antiangiogénique, en
partie par inhibition de la prolifération péricytaire. Le suni-
tinib est administré par voie orale à la dose de 50 mg/jour,
quatre semaines sur six. Cette indication repose sur les
résultats de l’étude de phase III de Motzer et al. [5], com-
parant le sunitinib à l’IFNαà 9 MUI 3 fois/semaine chez
des patients en première ligne thérapeutique, dont plus de
90 % relevaient des groupes à risque bas et intermédiaire
selon les critères du MSKCC. Les résultats étaient claire-
ment en faveur du sunitinib, avec un bénéfice pour tous
les groupes pronostiques, puisque la survie sans progres-
sion était de 11 mois vs 5 mois (p < 10
-6
). Le taux de
réponse était de 31 % vs 6 % (p < 10
-6
). L’amélioration
de la qualité de vie était également significative en faveur
du sunitinib (p < 0,001). Nous ne disposons pas pour le
moment de résultats sur la survie globale, la médiane de
survie n’ayant pas été atteinte.
Bevacizumab
Le bevacizumab (Avastin
®
) est un anticorps monoclo-
nal dirigé contre le vascular endothelial growth factor
(VEGF), dont les indications comprennent actuellement,
outre le cancer du rein, les cancers du sein, colorectal et
du poumon. L’AMM du bevacizumab en association à
l’IFNαdans le cancer du rein repose sur une étude de
phase III ayant randomisé 325 patients présentant un can-
cer du rein métastatique en 1
re
ligne thérapeutique [6].
Celle-ci a comparé l’association bevacizumab (10 mg/kg
toutes les deux semaines) plus IFNα(9 MUI 3 fois par
semaine), à un placebo associé à l’IFNα. La médiane de
survie sans progression était de 10,2 mois vs 5,4 mois
(p = 0,0001) pour le groupe témoin avec, en analyse de
sous-groupes, une différence très significative pour le
groupe de « bon pronostic » (12,9 vs 7,6 mois
p < 0,001). Ces résultats ont permis l’obtention de
l’AMM pour le bevacizumab en association à l’IFNα,
chez les patients « de bon pronostic » suivant la classifi-
cation du MSKCC.
Temsirolimus
Le temsirolimus (Torisel
®
) est un inhibiteur de la pro-
téine mTOR, composante de la signalisation intracellu-
laire dans la croissance, la prolifération cellulaire ainsi
que la réponse au stress hypoxique [7, 8]. Le temsirolimus
se lie à FKBP-12 pour former le complexe FKBP-
12/temsirolimus, qui va inhiber mTOR et entraîner une
inhibition de la traduction des protéines régulatrices de
la progression dans le cycle cellulaire et de l’angiogenèse
(dont HIF1αet 2α). Une étude de phase III multicentrique
dans le CRM a comparé, en première ligne thérapeutique,
chez des patients de mauvais pronostic, l’IFNα(n = 207
patients) au temsirolimus 25 mg/semaine (n = 209
patients), et à l’association d’IFNαet de temsirolimus
15 mg/semaine (n = 210 patients) [9]. Cette étude portait
sur des patients présentant un cancer du rein avancé de
mauvais pronostic (critères du MSKCC, plus présence
d’au moins 2 sites métastatiques). Chez les patients rece-
vant du temsirolimus en monothérapie, la médiane de
survie globale était significativement augmentée par rap-
port au groupe association et au groupe IFNαavec res-
pectivement : 10,9 mois vs 7,3 mois (p = 0,0078) vs
8,4 mois. La différence était également significative pour
la survie sans progression avec respectivement : 3,8 mois
vs 3,7 mois vs 1,9 mois. La proportion de patients avec
une maladie contrôlée (stable au moins 6 mois ou avec
une réponse objective) était plus importante dans le
groupe temsirolimus seul que dans le groupe association
(32,1 % vs 28,1 %, p < 0,001) et IFNα(15,5%, p = 0,002)
probablement en raison des doses plus faibles de temsiro-
limus, et d’une augmentation du nombre d’événements
indésirables dans ce groupe. Par ailleurs, le temps sans
symptôme lié à la maladie ni toxicité était significative-
ment supérieur dans le groupe temsirolimus (7,3 mois)
vs interféron (5,7 mois) ; (p = 0,021).
Deuxième ligne thérapeutique
Sorafenib
Le sorafenib/Nexavar
®
est un autre inhibiteur multi-
cible de récepteurs à tyrosine kinase, ciblant les raf-
kinases, VEGFR1, 2, 3 ; PDGFRβ; FLT3, c-kit, et RET
receptor tyrosine kinase [10, 11]. La dose recommandée
est de 2 ×400 mg/j en continu par voie orale, chez des
patients en échec d’une première ligne de traitement [12].
Cette indication repose sur les résultats d’une étude de
phase III, comparant le sorafenib à un placebo, chez des
patients de risque bas ou intermédiaire selon les critères
du MSKCC [12]. Plus de 80 % des patients avaient au
préalable été traités par immunothérapie. La médiane de
survie sans progression était de 5,5 mois vs 2,8 mois
(p < 0,01). Le taux de réponse partielle était de 10 %
dans le groupe sorafenib contre 2 % dans le groupe pla-
cebo (p < 0,001). Par ailleurs, le sorafenib peut être admi-
nistré en première ligne chez les patients ayant des
contre-indications aux traitements de première ligne.
Tableau 1. Critères pronostiques du MSKCC [2]
Taux de LDH > 1,5 N
Taux d’hémoglobine < N
Calcémie corrigée > 2,5 mmol/L
Score de Karnofsky < 80
Délai entre le diagnostic et le début du traitement < 1 an
mt, vol. 14, n° 5-6, septembre-décembre 2008
Dossier
278
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

L’ensemble de ces agents offre à présent aux oncolo-
gues médicaux un arsenal thérapeutique qui remplace
presque entièrement les thérapeutiques utilisées ces der-
nières années dans le traitement du CRM, même s’il per-
siste quelques rares indications d’immunothérapie chez
des patients très sélectionnés. Le caractère novateur de
ces thérapies ciblées, de même que leur mécanisme d’ac-
tion, entraînent l’apparition de nouveaux effets secondai-
res. Leur connaissance et les moyens d’y remédier sont
indispensables, tant au spécialiste qu’au médecin généra-
liste. En effet, l’efficacité du traitement est intimement liée
à la compliance du patient, elle-même étant fonction du
retentissement des effets indésirables.
Quels sont les effets secondaires
des thérapies ciblées dans le CRM
et comment y remédier ?
Les effets secondaires observés lors d’un traitement
par thérapies ciblées dans le CRM peuvent être classés
selon leur nature, selon qu’il s’agisse de la toxicité sur la
peau et les phanères, le tractus digestif ou le système car-
dio-vasculaire. D’autres effets secondaires, tels que l’as-
thénie, sont également fréquents. L’asthénie et la fatigue
sont les principales plaintes exprimées par les patients,
avec un retentissement important sur leur qualité de vie.
Quel que soit le traitement administré, il s’agit d’une com-
plication d’origine multifactorielle, qui doit faire recher-
cher une anémie, une hypothyroïdie, une déshydratation,
une anorexie [13].
Atteinte cardiovasculaire
L’atteinte cardiovasculaire est au premier plan des
effets secondaires des inhibiteurs de RTK, conséquence
directe de leur action anti-angiogénique. Il s’agit d’une
toxicité fréquente, dont les complications tant cardiaques
que vasculaires sont potentiellement graves, et qui
requiert une surveillance attentive et un traitement pré-
coce et adapté [13].
Hypertension artérielle
L’hypertension artérielle sous sorafenib et sunitinib est
une complication usuelle, survenant de novo ou aggra-
vant une HTA préexistante. Elle touche de 16 à 42,6 %
des patients, dont 5 % environ de grades 3-4 [14]. Cette
complication est également fréquente chez les patients
traités par bevacizumab à 10 ou 15 mg/kg, pour lesquels
l’incidence est de 25,4 % avec un risque relatif de surve-
nue d’une HTA de 7,5 comparé au groupe témoin [15]
(tableau 2) :
L’augmentation progressive des pressions artérielles
systoliques et diastoliques apparaît durant les trois pre-
mières semaines de traitement, persistant pendant au
moins 18 semaines [16]. Dans le contexte d’une HTA
sous sorafenib, il convient de rechercher des signes évo-
cateurs de leucoencéphalopathie (cf. infra).
Les mécanismes impliqués dans la physiopathologie
de la survenue d’une HTA sous antiangiogéniques sont
multiples. En premier lieu, il s’agit d’une altération de la
fonction endothéliale, conséquence d’une angiogenèse
imparfaite. Celle-ci est liée à une inhibition de la voie
du VEGFR, on observe une diminution du nombre d’arté-
rioles et de capillaires, et donc de la surface vasculaire, ce
qui provoque une augmentation des résistances vasculai-
res périphériques [17, 18]. C’est le phénomène de raréfac-
tion vasculaire. La dysfonction endothéliale résulte égale-
ment d’une diminution de la synthèse de NO et une
augmentation du stress oxydatif. Un autre mécanisme
semble également en jeu, par la voie de l’angiotensine
II. Des protéines kinases intracellulaires comme EGFR,
PDGFR, Ser-Thr kinase participent à la régulation de la
pression artérielle par régulation de l’activation de la
voie de l’angiotensine II. Ces protéines sont également
des cibles du sorafenib et du sunitinib, qui altèrent ainsi
le fonctionnement du système rénine-angiotensine [19].
Toutefois, le rôle de la voie de l’angiotensine II dans le
développement de l’HTA associée au sorafenib apparaît
limité, alors que la dysfonction endothéliale secondaire à
la raréfaction vasculaire semble en revanche capitale [16].
Les patients atteints de cancer du rein seraient peut-
être plus susceptibles de développer une HTA, du fait de
leur âge, des antécédents de néphrectomie, de dysfonc-
tion rénale, de l’utilisation de produits de contraste iodés,
de la déshydratation, majorant la toxicité du sorafenib.
Toutefois, il n’y a pas de différence d’incidence d’HTA
entre les patients traités par sorafenib pour un cancer du
rein ou pour une autre affection (23,6 vs 23 %, respecti-
vement) [14]. Il se pourrait pourtant que l’amplitude de
l’augmentation de la pression artérielle induite par le sora-
fenib masque des variations plus faibles, reliées à la pré-
sence d’un cancer du rein, tout en connaissant la capacité
de sécrétion de VEGF par la tumeur rénale [20]. Aucune
corrélation n’a été établie entre l’incidence de l’HTA et la
concentration plasmatique des antiangiogéniques.
Cependant, nous savons à présent que la présence d’une
HTA, en particulier de grade 3, est liée à une plus grande
efficacité du sunitinib. La survenue d’une HTA pourrait
Tableau 2. Fréquence et sévérité de l’HTA (adapté de [13])
HTA Tous grades Grades 3 et 4
Sunitinib [5] 24 % 8 % (grades 3)
IFNα[2] 1 % 1 %
Sorafenib [12] 17 % 4 %
Placebo 2 % < 1 %
mt, vol. 14, n° 5-6, septembre-décembre 2008 279
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

donc devenir un facteur prédictif de réponse au traitement
par cette molécule [21].
Toxicité cardiaque
La cardiotoxicité associée au sunitinib a initialement
été décrite par Chu et al. dans une étude rétrospective,
chez 75 patients traités par sunitinib à 50 mg/j pendant
4 cycles, pour une tumeur stromale gastro-intestinale
imatinib-résistante [24]. Dans cette étude, 8 patients
(11 %) avaient présenté un événement cardiaque : choc
cardiogénique conduisant au décès (1 patient), infarctus
du myocarde (1 patient) et 6 poussées d’insuffisance car-
diaque congestive. Par ailleurs, 50 % des patients traités
avaient présenté une HTA lors du premier cycle de traite-
ment et 36 % présentaient une baisse de leur fraction
d’éjection ventriculaire gauche, déjà rapportée par
Motzer et al. [5]. Le seul facteur de risque pouvant expli-
quer ces événements était un antécédent de coronaropa-
thie. Une incidence aussi élevée de complications cardia-
ques graves, dans l’étude de Chu et al., doit être mise en
balance avec les antécédents des patients, tous prétraités
par imatinib, et dont 20 % avaient un antécédent de trai-
tement par anthracyclines [24]. La physiopathologie de
cette toxicité repose vraisemblablement sur l’activation
de la voie intrinsèque de l’apoptose. Ainsi, sous l’action
du sunitinib, la kinase ribosomale S6 [25] est inhibée,
conduisant à la libération du facteur pro-apoptotique
bcl2, l’activation de la voie intrinsèque de l’apoptose et
la déplétion d’ATP, laquelle conduit à une dysfonction
ventriculaire. Par ailleurs, le sunitinib provoque l’inactiva-
tion de la kinase AMP dépendante, ce qui est crucial dans
la réponse cellulaire à l’hypoxie et dans la survie des car-
diomyocytes.
La toxicité cardiaque induite par le sorafenib ne doit
pas être méconnue. Ainsi, dans l’étude de phase III [12],
l’ischémie myocardique était significativement (p=
0,01) plus fréquente dans le groupe sorafenib (n= 12,
soit 3 %), que dans le groupe placebo (n= 2, soit
0,4 %), restant dans des proportions moins inquiétantes.
La physiopathologie de la toxicité cardiaque induite par
le sorafenib repose sur l’inhibition des kinases RAF1 et
BRAF, ce qui altère la survie des cardiomyocytes en
situation de stress [25]. En effet, ces kinases sont impli-
quées dans la survie des cardiomyocytes ; la délétion de
RAF1 provoquant une dilatation et une hypocontracti-
lité myocardique par apoptose et fibrose des cardiomyo-
cytes.
La toxicité cardiaque de ces deux agents a été confir-
mée dans une étude récente, portant sur 74 patients traités
pour un CRM [26] : 25 patients ont présenté des événe-
ments cardiovasculaires (11 pour le sunitinib, 14 pour le
sorafenib), dont 13 avec des symptômes d’angor, 12 avec
des modifications électriques, 17 avec une élévation des
CKMB et 9 patients avec une élévation de la troponine.
L’échocardiographie a mis en évidence une altération de
la FEVG chez 9 patients, une dysfonction contractile chez
7 patients, des troubles de la relaxation chez 1 patient et
un épanchement péricardique chez 1 patient. Ces événe-
ments survenaient chez les patients traités par sunitinib ou
sorafenib, sans différence significative selon le traitement.
Après arrêt transitoire de ces agents chez les patients
symptomatiques ainsi qu’un traitement par carvedilol et
statines, tous les patients ont récupéré sur le plan fonc-
tionnel, permettant la réintroduction des inhibiteurs de
RTK.
Prise en charge
–Prescrire une mesure tensionnelle hebdomadaire pen-
dant les 6 premières semaines de traitement par sorafenib ou
sunitinib.
–Prescription d’un antihypertenseur, idéalement un inhi-
biteur de l’enzyme de conversion ou un sartan. Les médica-
ments antihypertenseurs de choix sont l’énalapril (IEC) et le
candesartan (anti-ARAII) qui peuvent inhiber l’angiogenèse
myocardique induite par le VEGF [22, 23]. Il faut par ailleurs
prêter une attention particulière aux interactions médicamen-
teuses. En effet, le sorafenib est métabolisé par le CYP3A4,
donc les inhibiteurs du CYP3A4 tels que les inhibiteurs calci-
ques non dihydropyrimidiques (vérapamil, diltiazem) peu-
vent augmenter la concentration plasmatique du sorafenib.
–Interruption temporaire ou définitive du traitement en
cas d’HTA incontrôlée ou sévère (Grade 3-4).
Prise en charge
–Surveillance clinique et monitoring par ECG et écho-
graphie cardiaque avant le début du traitement et à chaque
cycle [13].
–Contre-indication au sunitinib en cas d’antécédent de
coronaropathie et/ou de QT long à l’ECG.
–Respect d’une fenêtre thérapeutique entre l’initiation
d’un traitement par sorafenib après progression sous suniti-
nib. Le risque d’insuffisance cardiaque aiguë est alors majoré,
dans le cas d’un délai inférieur à 2 à 3 semaines [27, 28].
–Arrêt définitif du sunitinib en cas de poussée d’insuffi-
sance cardiaque, dans l’attente d’arguments autorisant sa
réintroduction plus ou moins différée.
–Traitement par bêtabloquant, statines en cas de pous-
sée d’insuffisance cardiaque. Un traitement anticoagulant est
à discuter [26].
–En l’absence d’insuffisance cardiaque cliniquement
décelable, arrêt du traitement ou diminution des doses si la
FEVG est inférieure à 50 % avec une diminution de plus de
20 % par rapport à la valeur initiale [13].
mt, vol. 14, n° 5-6, septembre-décembre 2008
Dossier
280
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Atteinte cutanée
Syndrome pied-main (SPM)
Il s’agit d’un effet secondaire commun au sunitinib et
au sorafenib, distinct du SPM induit par la chimiothérapie
de type 5-FU, capécitabine, ou doxorubicine en formula-
tion liposomale, car il se présente sous une forme plus
hyperkératosique [29]. Il apparaît dans les six premières
semaines et surtout dans la première quinzaine de début
de traitement, puis va progressivement diminuer en inten-
sité. Les patients présentent des dysesthésies et des pares-
thésies, qui précèdent l’apparition d’un érythème avec
œdème, puis d’une hyperkératose avec une sécheresse
cutanée et/ou une peau craquelée, avec desquamation
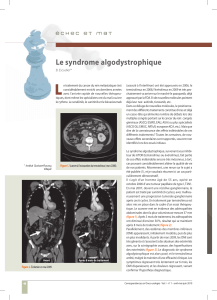
(figures 1 et 2). Il existe une prédominance topographique
au niveau des zones de pression. Différents niveaux de
gravité sont observés (tableau 3) [30]. La symptomatolo-
gie est dose-dépendante, peut nécessiter un arrêt tempo-
raire du traitement, et n’empêche pas systématiquement
sa réintroduction.
La physiopathologie reste encore inconnue, mais on
suggère actuellement un effet toxique direct [31, 32].
Les biopsies cutanées montrent une hyperkératose associée
à un infiltrat inflammatoire et un œdème du derme, une
dilatation vasculaire, avec une altération de la paroi sans
réelle image de vascularite. La fragilisation des capillaires
est probablement le mécanisme principal mais non unique.
Une hyperexpression de récepteurs cibles au niveau des
kératinocytes est une hypothèse également envisagée,
étant donné le blocage de la maturation cellulaire avec
modification de la différenciation des kératinocytes, et
apoptose associée à une inflammation non spécifique.
Rash cutané
Outre le syndrome pied-main, il existe également une
toxicité cutanée propre au sorafenib et qui concerne tous
les inhibiteurs d’EGFR. Il s’agit d’un rash érythémateux
papulo-pustuleux prédominant au niveau du visage et
de la partie supérieure du thorax, qui survient à l’initiation
du traitement, mais également à distance. Il s’apparente
cliniquement aux manifestations de la dermatite sébor-
rhéique [29]. Il faut le distinguer des réactions allergiques
Figure 1. Atteinte de la paume des mains après un cycle de suni-
tinib à 50 mg/j.
Figure 2. Atteinte plantaire chez le même patient.
Prise en charge [29]
–Soins de pédicure et l’application d’une lotion hydra-
tante avant traitement et dès les premiers symptômes car la
précocité du traitement local émollient est capitale pour évi-
ter l’aggravation. L’application d’une crème hydratante doit
être renouvelée plusieurs fois par jour, selon l’épaisseur de la
couche cornée. En cas d’échec, il est possible de recourir à
l’application de vaseline salicylée.
–Conseiller le port des chaussettes en coton, de chaus-
sures souples, de gants nocturnes avec lotion hydratante.
–En cas de réaction inflammatoire importante : prescrip-
tion de corticoïdes en topiques (bétaméthasone) une applica-
tion en couche épaisse le soir pendant 10 à 15 jours.
–Si échec avec retentissement fonctionnel ou décolle-
ment cutané : réduction transitoire des doses à 2 ×200 mg
de sorafenib en une prise/jour.
–En cas de toxicité de grade ≥3, arrêt temporaire du trai-
tement jusqu’à cicatrisation puis réintroduction à une dose
réduite
mt, vol. 14, n° 5-6, septembre-décembre 2008 281
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%