Le syndrome de Takotsubo : au cœur de l`état de mal épileptique

doi: 10.1684/epi.2010.0320
Le syndrome de Takotsubo :
au cœur de l’état
de mal épileptique
Shirley Spagnolo
1
, Hervé Outin
2
1
Service de réanimation polyvalente, hôpital Roger-Salengro, CHRU Lille,
rue du Professeur-Émile-Laine, 59037 Lille cedex, France
2
Service de réanimation médicochirurgicale, centre hospitalier intercommunal
de Poissy-Saint-Germain-en-Laye, 10, rue du Champ-Gaillard, 78303 Poissy cedex, France
Résumé. Le syndrome de Takotsubo correspond à une défaillance cardiaque aiguë gauche, conséquence
d’un stress physique ou émotionnel et liée à une décharge catécholaminergique. Ce tableau clinique est le plus sou-
vent décrit chez la femme de plus de 60 ans. Le terme Takotsubo fait référence à l’amphore utilisée par les pêcheurs
japonais pour la pêche des poulpes. Ce vase à la base élargie et au collet étroit rappelle la forme échographique du
ventricule gauche observée en échographie cardiaque transthoracique. Parmi les différents facteurs déclenchants
depuis une dizaine d’années, des cas de syndrome de Takotsubo ont été rapportés dans un contexte d’état de mal
épileptique. La base du traitement, après élimination d’une thrombose coronaire par la coronarographie, est la
prise en charge symptomatique de la défaillance cardiaque gauche avec, parallèlement, le traitement du facteur
déclenchant. Le pronostic de ce syndrome est favorable avec une récupération ad integrum de la fonction cardiaque
dans la majorité des cas en quelques semaines. Une association possible aux décès inexpliqués chez certains patients
épileptiques pourrait ouvrir la voie à des travaux de recherche dans une population ciblée de patients épileptiques à
haut risque visant à la prévention d’un déséquilibre catécholaminergique au cours des crises épileptiques.
Mots clés :épilepsie,cardiomyopathie aiguë,physiopathologie
Abstract. Takotsubo cardiomyopathy: in the heart of status epilepticus
Takotsubo cardiomyopathy, an acute left cardiac failure, is the consequence of a physical or emotionnal stress. A link
with catecholaminergic storm could exist. The term “Takotsubo”refers to a jar that is used in Japan for trapping octopi.
This shape looks like the peculiar LV ballooning evident on left ventriculogram. Among different triggers, since ten
years, Takotsubo syndromes have been reported with status epilepticus. Treatment, after coronary thrombosis
removal, includes symptomatic treatment of cardiac failure and removal of trigger. Takotsubo syndrome resolves in
a short time with normalisation of the left ventricle function. A possible association with unexpected death in epileptic
patients could enhance research for prevention of catecholaminergic storm during seizures.
Key words:epilepsy,acute cardiomyopathy,pathogenesis
La première description du syndrome de
Takotsubo date de 1991 par Dote et al. Il s’agit
d’une défaillance cardiaque gauche aiguë dont
l’appellation a varié au cours du temps : broken
heart disease, myocardial stunning disease,
neurogenic cardiopathy, ampulla cardiomyopathy,
transient left ventricular dysfunction et, depuis
2002, stress induced cardiomyopathy.
Épilepsie et cœur
Épilepsie et cœur
Épilepsies 2010 ; 22 (3) : 212-6
Tirés à part :
S. Spagnolo
Épilepsies, vol. 22, n° 3, juillet-août-septembre 2010 212
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

L’ensemble de ces dénominations regroupe les manifesta-
tions liées à un stress physique ou émotionnel responsable d’une
décharge catécholaminergique entraînant des modifications du
fonctionnement ventriculaire gauche, notamment apical.
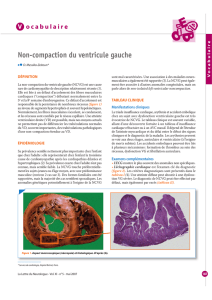
Le terme Takotsubo fait référence à l’amphore utilisée par
les pêcheurs japonais pour la pêche des poulpes. Ce vase à la
base élargie et au col étroit rappelle la forme du ventricule gau-
che pouvant être observée en échographie cardiaque transtho-
racique lors de situations telles qu’un stress émotionnel
(annonce du décès d’un proche, d’une maladie grave,
dispute…) ou physique (intervention chirurgicale…). Parmi
ces différents facteurs déclenchants, depuis quelques années,
des cas de syndrome de Takotsubo ont été rapportés dans un
contexte d’état de mal épileptique (Sakuragi et al., 2007 ; Bosca
et al., 2008 ; Lemke et al., 2008 ; Legriel et al., 2008).
Physiopathologie
La physiopathologie de ce syndrome est discutée. La prédomi-
nance initiale des descriptions provenant du Japon a fait sus-
pecter un terrain ethnique prédisposant. Il existe, par ailleurs,
un polymorphisme des gènes affectant la réponse périphérique
aux catécholamines, ce qui explique une réponse cardiaque
individuelle vis-à-vis du stress (Zaroff et al., 2006 ; Brotman
et al., 2007).
Une plus grande fréquence de ce syndrome chez les femmes
ménopausées souligne une possible influence hormonale
(Taddei et al., 1996).
L’augmentation du taux de catécholamines systémiques
serait l’élément central de la physiopathologie du Takotsubo.
Celles-ci, notamment la noradrénaline, auraient un effet
toxique sur les cardiomyocytes : activation permanente des
canaux calciques, lésions membranaires et spasmes macro-
et/ou microvasculaires. Ainsi, les taux plasmatiques de noradré-
naline et d’adrénaline sont plus élevés chez les patients présen-
tant un Takotsubo, en comparaison avec les patients présentant
un infarctus du myocarde en phase aiguë (Wittstein et al.,2005).
Selon des données expérimentales, le stress secondaire à une
immobilisation chez le rat active le système sympathique
adrénergique entraînant un sus décalage du segment ST sur
l’électrocardiogramme (ECG) et une ballonisation du ventri-
cule gauche. Une prévention du syndrome serait donc possible
par blocage adrénergique alpha et bêta (Ueyama et al., 2006).
Parallèlement, un trouble du métabolisme des acides gras et
du glucose a été décrit et confirmé par un défaut de captation
cellulaire du F-18 fluorodéoxyglucose dans les cardiomyocytes
du territoire akinétique des patients présentant un Takotsubo
(De Boeck et al., 2007 ; Yoshida et al., 2007).
L’hypothèse d’un vasospasme coronaire est évoquée par
Dote et al. (1991). Devant les discordances d’incidence de
vasospasme coronarien provocable par Méthergin
®
chez les
patients présentant un syndrome de Takotsubo (0 à 43 %
selon les séries et 28 % dans la méta-analyse de Gianni et al.,
2006), l’hypothèse d’une dysfonction microvasculaire a été
évoquée. Dans deux séries de patients dont le bilan comprenait
une coronarographie, un allongement du délai de perfusion
dans les artères coronaires épicardiques à la phase aiguë
du syndrome de Takotsubo a été décrit (Bybee et al., 2004).
Ces résultats arguaient pour un mécanisme à l’échelle
microvasculaire.
Présentation clinique
La présentation clinique est homogène : il s’agit d’un tableau
évocateur d’un syndrome coronarien aigu, survenant chez une
femme, dans 90 % des cas, dont l’âge moyen varie entre 58 et
77 ans. Les pathologies préexistantes associées liées au terrain
ont une prévalence identique à celle d’une population de la
même tranche d’âge. Devant un tableau de syndrome corona-
rien aigu, le diagnostic de Takotsubo est retenu dans plus de
1 % des cas (Kurowski et al., 2007).
Sur le plan paraclinique
Sur le plan paraclinique, quatre éléments sont essentiels :
l’ECG, l’échographie cardiaque transthoracique, la coronaro-
graphie et le dosage des enzymes myocardiques.
Les modifications ECG sont compatibles avec un syndrome
coronarien aigu : élévation du segment ST, modification de
l’onde T, allongement du segment QT. Cependant, certaines
différences ont été relevées :
–il n’est pas retrouvé de signe du miroir ;
–la fréquence des anomalies des ondes Q est moindre ;
–l’élévation du segment ST est plus fréquente dans les dériva-
tions V4V6 que V1V3 ;
–la mesure de l’espace QT corrigée est significativement plus
longue en cas de syndrome de Takotsubo (Ogura et al., 2003).
Dans le contexte d’une cardiopathie de stress secondaire à
une pathologie neurologique, les modifications de l’ECG
seraient la manifestation d’une dysrégulation du système
nerveux autonome pouvant être liée à une lésion de la repré-
sentation corticale du système nerveux autonome.
Échographie cardiaque transthoracique
L’échographie cardiaque transthoracique est l’examen clé
du diagnostic. On constate une base du ventricule gauche
hyperkinétique associée à une akinésie apicale entraînant un
ballonnement apical et une diminution sévère de la fraction
d’éjection du ventricule gauche. L’étendue de la zone d’akinésie
ne correspond pas à un territoire vasculaire coronarien.
Ces mêmes anomalies peuvent être mises en évidence lors d’une
ventriculographie réalisable au moment de la coronarographie.
Le syndrome de Takotsubo : au cœur de l’état de mal épileptique
Épilepsies, vol. 22, n° 3, juillet-août-septembre 2010
213
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

La confirmation du syndrome de Takotsubo implique, dans
la majorité des cas, la réalisation d’une coronarographie en
urgence permettant d’éliminer une thrombose coronaire
ayant une prise en charge spécifique.
Enzymes myocardiques
L’élévation des enzymes myocardiques et notamment de la
troponine est peu marquée en comparaison de l’étendue et de
la sévérité de la dysfonction myocardique. Ces modifications
n’ont pas de profil spécifique.
Données anatomopathologiques
Les données anatomopathologiques connues dans ce
syndrome proviennent de biopsies endocardiques réalisées :
–dans le cadre du bilan étiologique de la survenue brutale
d’une dysfonction cardiaque gauche sans étiologie thrombo-
tique en coronarographie ;
–lors d’autopsie.
Les lésions décrites sont une fibrose interstitielle avec peu
d’infiltrat cellulaire (Abe et al., 2003). On note également
l’absence de génome viral, la présence dans le cytoplasme des
cardiomyocytes de vacuoles remplies de glycogène en faveur
d’une privation énergétique et la « désorganisation en bandes »
des protéines contractiles des cardiomyocytes (Nef et al., 2007).
Ces lésions sont identiques à celles constatées chez l’animal
soumis à une perfusion prolongée de catécholamines (Ueyama
et al., 2006). Dans les rares cas où une biopsie de contrôle était
réalisée, après récupération clinique, on constatait la régression
totale des anomalies anatomopathologiques.
Prise en charge thérapeutique
Actuellement, il n’existe pas d’étude randomisée portant sur
la prise en charge thérapeutique idéale de ce syndrome. La base
du traitement, après élimination d’une thrombose coronaire
par la coronarographie, est la prise en charge symptomatique
de la défaillance cardiaque gauche associée parallèlement à la
recherche et à la prise en charge du facteur déclenchant. En
cas de choc cardiogénique (survenant en phase aiguë dans
4,2 % des cas selon Gianni et al., 2006), il peut être nécessaire
d’introduire des inotropes positifs et des vasopresseurs. Ces trai-
tements font cependant l’objet de controverses du fait du lien
possible entre les taux élevés de catécholamines associés au
phénomène de sidération myocardique (Kurisu et al., 2005).
Ces patients nécessitent un monitoring de leurs constantes
(pression artérielle, fréquence cardiaque et saturation en oxy-
gène), compte tenu du risque d’instabilité hémodynamique et
de trouble de la conduction cardiaque (épisodes de fibrillation
ventriculaire rapportés dans 1,5 % des cas) (Gianni et al.,
2006).
Le pronostic de ce syndrome est en règle favorable avec
une récupération ad integrum de la fonction cardiaque dans la
majorité des cas en quelques semaines (Aurigemma et Tighe,
2006). Cependant, la mortalité rapportée pendant l’hospitalisa-
tion est de 1,1 % (Gianni et al., 2006).
Pathologies neurologiques associées
Parmi les pathologies neurologiques associées au syndrome
de Takotsubo, cinq cas d’état de mal épileptique généralisé
sont rapportés dans la littérature (Sakuragi et al., 2007 ; Weeks
et al., 2007 ; Lemke et al., 2008 ; Bosca et al., 2008 ; Legriel
et al., 2008). Depuis de nombreuses années, il est fait état de
manifestations neurovégétatives au cours de l’état de mal
épileptique généralisé. Meierkord et al. (1994) décrivaient la
survenue d’un « orage catécholaminergique » au décours d’un
état de mal épileptique, avec une augmentation des taux plas-
matiques de noradrénaline et d’adrénaline dans les 30 minutes
suivant le début des crises, secondaire à l’activation du système
nerveux autonome sympathique. Ces phénomènes étaient déjà
très largement décrits dans d’autres pathologies neurologiques
telles l’hémorragie sous-arachnoïdienne et le syndrome de
Guillain-Barré (Kono et al., 1994 ; Lee et al., 2006), mais
l’appellation du syndrome cardiologique associé différait : on
parlait de neurogenic stunned myocardium. On trouve dans la
littérature de nombreuses descriptions d’épisodes de détresse
respiratoire aiguë à la phase initiale de prise en charge de
certaines pathologies neurologiques (dont l’état de mal épilep-
tique) ou neurochirurgicales, dénommées « œdème pulmo-
naire neurogène ». Ces épisodes respiratoires sont probable-
ment en relation avec une augmentation du taux de
catécholamines circulantes retentissant sur la fonction
cardiaque. Le rôle de la dysfonction cardiaque gauche dans la
survenue de l’œdème pulmonaire dit « neurogène » a été expé-
rimentalement démontré par Johnston et al. (1996). Sur un
modèle de brebis épileptiques, un état de mal convulsif était
provoqué. Les pressions artérielle, pulmonaire et de l’oreillette
gauche étaient maintenues fixes par canulation des gros
vaisseaux. Cette manipulation empêchait l’augmentation du
flux lymphatique pulmonaire. Dans ce contexte, on notait
l’absence de formation d’œdème pulmonaire lors de l’état de
mal convulsif. Ces résultats montraient donc l’importance du
mécanisme cardiogénique dans la formation de l’œdème
pulmonaire neurogène.
L’augmentation de la perméabilité capillaire pulmonaire
dans l’œdème pulmonaire neurogène a également été utilisée
comme argument pour l’existence d’un mécanisme ne faisant
pas intervenir le système cardiovasculaire. En effet, dans une
étude animale sur l’état de mal convulsif, une augmentation
de la conductance transcapillaire de l’albumine au niveau pul-
monaire était en faveur d’une augmentation de la perméabilité
capillaire (Simon et al., 1984). Cependant, Johnston et al.
(1996) constataient que le contrôle des facteurs hémo-
dynamiques dans la circulation pulmonaire au cours des crises
convulsives entraînait la disparition de l’augmentation du flux
S. Spagnolo, H. Outin
Épilepsies, vol. 22, n° 3, juillet-août-septembre 2010 214
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

transcapillaire : un mécanisme non cardiogénique surajouté
n’était donc pas nécessaire pour expliquer l’augmentation de
perméabilité capillaire, mais était la conséquence de la sévérité
de l’augmentation de pression transcapillaire résultant de la
décharge catécholaminergique.
La relecture de ces éléments permet d’aboutir à la conclu-
sion que le syndrome de Takotsubo est caractérisé par son
apparence échographique, alors que le syndrome de sidération
myocardique neurogène est défini par la lésion neurologique
l’ayant entraîné (Shimizu et al., 2008).
Un des intérêts de l’étude de ce syndrome de dysfonction
ventriculaire gauche transitoire, que sa dénomination soit
celle, actuelle, de syndrome de Takotsubo, ou plus ancienne,
de sidération myocardique neurogène, réside dans son associa-
tion possible aux décès inexpliqués survenant chez les patients
épileptiques (SUDEP [Sudden Unexpected Death in EPilepsy])
(Stöllberger et Finsterer, 2004) ou au décours d’épisodes d’état
de mal épileptique. Les facteurs de risque associés à ces morts
subites sont connus : début précoce de la maladie épileptique,
nature généralisée des crises et sexe masculin. En revanche, les
mécanismes physiopathologiques restent discutés : arythmies
cardiaques, dysautonomie, syndrome d’apnées du sommeil ?
Les données anatomopathologiques myocardiques dans le
cadre de cette pathologie sont similaires à celles décrites dans
le syndrome de Takotsubo : fibrose myocardique interstitielle,
vacuolisation myocytaire et fibrose périvasculaire prédominant
au niveau des terminaisons nerveuses myocardiques du sys-
tème nerveux autonome et sans lésion coronaire (Chin et al.,
2005). De la même façon, plusieurs auteurs rapportent la pré-
sence de lésions myocardiques de « nécrose de contraction en
bandes » chez la majorité des patients décédés après un état de
mal épileptique. Ces lésions correspondraient à une nécrose en
état d’hypercontraction des myofilaments des cellules myocar-
diques. Ces anomalies sont situées dans le myocarde adjacent à
l’insertion des terminaisons nerveuses sympathiques, ce qui
suggère que l’hypersécrétion catécholaminergique locale pour-
rait être le mécanisme de formation de ces zones de nécroses
en bandes. Par ailleurs, l’innervation sympathique du cœur
suivant le système conductif cardiaque, les anomalies ECG et
les épisodes d’arythmies pourraient également être expliqués
(Samuels, 1993).
Différents travaux rapportaient la formation de zone de
nécrose en bandes myocardiques similaires à celles décrites en
cas de « décharge catécholaminergique », en cas de lésion au
niveau hypothalamique (Melville et al., 1973), du cortex
limbique, de la formation réticulaire mésencéphalique et des
ganglions stellaires (Hawkins et Clower, 1971). La quantité
de catécholamines libérée dans le myocarde pourrait être
influencée par la durée et l’intensité des crises. Ce phénomène
pourrait expliquer la survenue d’un syndrome de Takotsubo en
cas d’état de mal épileptique et sa non-récurrence en cas de
crise épileptique non prolongée.
La progression des connaissances sur l’association de ces
deux entités pourrait ouvrir la voie à des travaux de recherche
dans une population ciblée de patients épileptiques à haut
risque visant à la prévention d’un déséquilibre catéchola-
minergique au cours des crises épileptiques.
□
Conflit d’intérêts : aucun.
Références
Abe Y, Kondo M, Matsuoka R, et al. Assessment of clinical features in
transient left ventricular apical ballooning. J Am Coll Cardiol 2003 ; 41 :
737-42.
Aurigemma GP, Tighe DA. Echocardiography and reversible left
ventricular dysfunction. Am J Med 2006 ; 119 : 18-21.
Bosca ME, Valero C, Pareja AI, et al. Takotsubo cardiomyopathy and
status epilepticus: a case report. Eur J Neurol 2008 ; 15 : e34-5.
Brotman DJ, Golden SH, Wittstein IS. The cardiovascular toll of
stress. Lancet 2007 ; 370 : 1089-100.
Bybee KA, Prasad A, Barsness GW, et al. Clinical characteristics and
thrombolysis in myocardial infarction frame counts in women with tran-
sient left ventricular apical ballooning syndrome. Am J Cardiol 2004 ; 94 :
343-6.
Chin PS, Branch KR, Becker KJ. Postictal neurogenic stunned myocar-
dium. Neurology 2005 ; 64 : 1977-8.
De Boeck BWL, Verburg FA, Hobbelink M, et al. Reversible 18-FDG
defects on myocardial PET: is this myocardial resurrection? Int J Cardiol
2007 ; 127 : 175-8.
Dote K, Sato H, Uchinda AT, Ishihara M. Myocardial stunning due to
simultaneous multivessel coronary spasms: a review of 5 cases. J Cardiol
1991 ; 21 : 203-14.
Gianni M, Dentali F, Grandi AM, et al. Apical ballooning syndrome or
takotsubo cardiomyopathy: a systematic review. Eur Heart J 2006 ; 27 :
1523-9.
Hawkins WE, Clower BR. Myocardial damage after head trauma and
simulated intracranial haemorrhage in mice: the role of the autonomic
nervous system. Cardiovasc Res 1971 ; 5 : 524-9.
Johnston S, Darragh T, Simon R. Postictal pulmonary edema requires-
pulmonary vascular pressure increases. Epilepsia 1996 ; 37 : 428-32.
Kono T, Morita H, Kuroiwa T, et al. Left ventricular wall motion
abnormalities in patients with subarachnoid hemorrhage: neurogenic
stunned myocardium. J Am Coll Cardiol 1994 ; 24 : 636-40.
Kurowski V, Kaiser A, von Hof K, et al. Apical and midventricular
transient left ventricular dysfunction syndrome (takotsubo cardiomyopa-
thy): frequency, mechanisms, and prognosis. Chest 2007 ; 132 : 809-16.
Kurisu S, Inoue I, Kawagoe T, et al. Takotsubo-like transient biventri-
cular dysfunction with pressure gradients. Int Med 2005 ; 44 : 727-32.
Lee VH, Connolly HM, Fulgham JR, et al. Takotsubo cardiomyopathy
in aneurysmal subarachnoid hemorrhage: an underappreciated ventricu-
lar dysfunction. J Neurosurg 2006 ; 105 : 264-70.
Legriel S, Bruneel F, Dalle L, et al. Recurrent takotsubo cardiomyopa-
thy triggered by convulsive status epilepticus. Neurocrit Care 2008 ; 9 :
118-21.
Lemke DM, Hussain SI, Wolfe TJ. Takotsubo cardiomyopathy associa-
ted with seizures. Neurocrit Care 2008 ; 9 : 112-7.
Meierkord H, Shorvon S, Lightman SL. Plama concentrations of
prolactin, noradrenaline, vassopressine and oxytocyn during and after a
prolonged epileptic seizure. Acta neurol Scand 1994 ; 90 : 73-7.
Melville KI, Garvey HL, Gillis RA. Neurogenic lesions of heart muscle.
Recent Adv Stud Cardiac Struct Metab 1973 ; 2 : 433-47.
Nef HM, Mollmann H, Kostin S, et al. Takotsubo cardiomyopathy:
intraindividual structural analysis in theacute phase and after functionnal
recovery. Eur Heart J 2007 ; 28 : 2456-64.
Le syndrome de Takotsubo : au cœur de l’état de mal épileptique
Épilepsies, vol. 22, n° 3, juillet-août-septembre 2010
215
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Ogura R, Hiasa Y, Takahashi T, et al. Specific findings of the standard
12-lead ECG in patients with takotsubo cardiomyopathy. Circ J 2003 ; 67 :
687-90.
Sakuragi S, Tokunaga N, Okawa K, et al. A case of takotsubo cardio-
myopathy associated with epileptic seizure: reversible left ventricular
wall motion abnormality and ST-segment elevation. Heart Vessels 2007 ;
22 : 59-63.
Samuels MA. Neurally induced cardiac damage. Neurol Clin 1993 ; 11 :
273-92.
Shimizu M, Kagawa A, Takano T, et al. Neurogenic stunned myocar-
dium associated with status epileptics and postictal catecholamine surge.
Intern Med 2008 ; 47 : 269-73.
Simon RP, Aminoff MJ, Benowitz NL. Changes in plasma catechola-
mines after tonic-clonic seizures. Neurology 1984 ; 34 : 255-7.
Stöllberger C, Finsterer J. Cardiorespiratory findings in sudden
unexplained/unexpected death in epilepsy (SUDEP). Epilepsy Res 2004 ;
59 : 51-60.
Taddei S, Virdis A, Ghiadoni L, et al. Menopause is associated with
endothelial dysfunction in women. Hypertension 1996 ; 28 : 576-82.
Ueyama T, Tanioku T, Nuta J, et al. Research report. Estrogen alters
c-Fos response to immobilization stress in the brain of ovariectomized
rats. Brain Research 2006 ; 1084 : 67-79.
Weeks SG, Alvarez N, Pillay N, et al. Takotsubo cardiomyopathy
secondary to seizures. Can J Neurol Sci 2007 ; 34 : 105-6.
Wittstein IS, Thiemann DR, Lima JA, et al. Neurohumoral feature of
myocardial stunning due to sudden emotionnal stress. N Engl J Med
2005 ; 352 : 539-48.
Yoshida T, Hibino T, Kako N, et al. A pathophysiologic study of takot-
subo cardiomyopathy with F-18 fluorodeoxyglucose positron emission
tomography. Eur Heart J 2007 ; 28 : 2598-604.
Zaroff JG, Pawlikowska L, Miss JC, et al. Adrenoceptor polymor-
phisms and the risk of cardiac injury and dysfunction after subarachnoid
hemorrhage. Stroke 2006 ; 37 : 1680-5.
S. Spagnolo, H. Outin
Épilepsies, vol. 22, n° 3, juillet-août-septembre 2010 216
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
1
/
5
100%