L`infarctus du myocarde

L’infarctus du myocarde
Conférence UV internat
14 mars 2006

Définition
L'infarctus du myocarde (IDM) est une
nécrose ischémique du myocarde dont
l'étendue dépasse 2 cm2. Il correspond
généralement à une thrombose occlusive
brutale d'une artère coronaire. Cette
définition classique de l'IDM correspond à
une réelle entité diagnostique (associant
douleur et sus décalage persistant de ST) et
thérapeutique.

Définition (2)
Une nouvelle définition de l'infarctus a été
proposée récemment (conférence de consensus
européenne et américaine, 2000) qui est différente
car elle repose sur une définition biologique
(ascension des marqueurs de l'infarctus -
troponines et MB-CK). Cette définition est plus
large car elle inclue aussi des infarctus "
rudimentaires ", " sans onde Q ", ou sans sus
décalage initial du segment ST.

Epidémiologie
L'infarctus du myocarde constitue une urgence
cardiologique absolue dont l'incidence reste
encore élevée avec 120 000 cas par an en France.
Son pronostic reste grave puisque l'IDM est
responsable encore de 10 à 12% de la mortalité
totale annuelle chez l'adulte.
Cardiopathies ischémiques = 1ère cause de décès
dans les pays développés

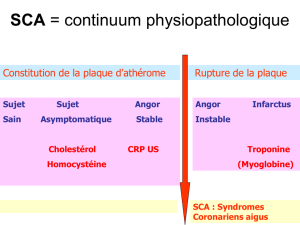
Physiopathologie
L'infarctus résulte d'une THROMBOSE CORONAIRE
AIGUË, elle-même secondaire à une fracture de plaque
d’athérome (au niveau de l’intima de l’artère) entraînant
l'agrégation plaquettaire puis l'occlusion coronaire.
Les conséquences myocardiques sont la DESTRUCTION
CELLULAIRE se propageant de l'endocarde jusqu'à
l'épicarde.
La nécrose myocardique entraîne une altération de la
fonction pompe du ventricule gauche (insuffisance
ventriculaire gauche, parfois insuffisance ventriculaire
droite) dès qu'elle atteint ou dépasse 20% du myocarde ;
elle est incompatible avec la survie lorsqu'elle atteint 40%
de la masse myocardique (choc cardiogénique).
La conséquence de cette nécrose est l'apparition d'une zone
myocardique fibreuse non contractile.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
1
/
25
100%