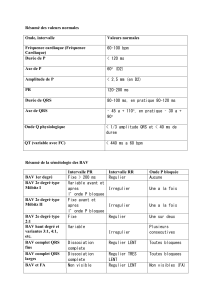
Échographie Doppler fœtaux et diagnostic du bloc auriculo

Échographie Doppler fœtaux et diagnostic du bloc auriculo
ventriculaire congénital d’origine immunologique.
C.Mrazguia, I.Brahem, A.Hammami, S.Armi, A.Falfoul
Service de gynécologie obstétrique hôpital régional de Nabeul
Introduction :
Les blocs auriculo ventriculaires (BAV) d’origine immunologique, liés à la présence dans le sérum maternel d’anticorps
anti-Ro/SS-A et/ou anti-La/SS-B représentent un peu moins de 70 % des BAV congénitaux.
Ils sont classiquement diagnostiqués entre 20 et 24 semaines d’aménorrhée (SA). Leur évolution est emaillée d’une
mortalité d’environ 16 à 20 %. L’enjeu d’une prise en charge précoce, si possible in utero, est donc grand. L’échographie et le
Doppler tiennent une place centrale dans l’approche diagnostique, pronostique et thérapeutique.
Notre but à travers un cas clinique , est de rapporter les modalités de dépistage et de prise en charge chez les fœtus à
risque de BAV congénital surtout en présence de pathologie auto immune.
Observation :
Il s’agit de Mme XX âgée de 26 ans G1P0 suivie pour une connectivite (lupus érythémateux disséminé), Le bilan
immunologique fait, montrait des anticorps anti-SS-A positifs. La patiente a été surveillée en diagnostic anténatal par des
échographies fréquentes pour dépister un BAV et ceci à partir de 20SA.
L’écho morphologie n’a pas montré d’anomalies morphologiques mais le doppler a décelé un BAV.
Le traitement par les corticoïdes a été entamé. Une consultation tous les mois a été faite jusqu’à 36SA 3j quand la
patiente a consulté en début de travail. L’accouchement par voie basse s’est fait d’un nouveau né de sexe masculin pesant
3500g Apgar 7/9/10 qui a été transféré dans un service de néonatologie de 3ème niveau ou le suivi a été fait en collaboration
avec le service de cardiologie.

Discussion :
Au moins une fois sur deux le B.A.V. est isolé, c’est à dire sans malformation cardiaque ; l’origine immunologique est
alors hautement probable. Depuis MORQUIO (1) à la fin du 19ème siècle, PLANT en 1945 et MICHAELSON en 1972, des
publications plus récentes sont venues confirmer la resposabilité de facteurs immunogénétiques maternels dans la
genèse des troubles de la conduction chez le foetus .
C’est SCOTT5 (2) qui en 1983 en apporte la preuve la plus convaicante. Cet auteur met en évidence un anticorps
nucléaire appelé Anti-RO ou Anti-SSA chez 83 % des 41 mères ayant mis au monde un enfaant atteint de B.A.V.
congénital. Cet anticorps est également retrouvé dans le sérum des enfants pendant les premières semaines de la vie.
Pendant longtemps, le BAV congénital a été considéré comme relativement bénin et bien toléré, mais les études
récentes montrent qu'il peut être responsable d'asthénie, d'intolérance à l'effort, de lipothymies, de syncopes ou de
mort subite non prévisible.
la maladie immunologique de la mère en est la cause, expliquant le caractère parfois familial de l'affection. Son origine
congénitale est indiscutable s'il a été diagnostiqué dès la naissance ou même in utero. Les anticorps maternels
traversent le placenta et passent dans la circulation fœtale. Le tissu cardiaque fœtal, y compris le tissu de conduction,
est riche en antigène Ro intracellulaire. les Ac anti Ro sont capables d'induire une inflammation myocardique
spécifique qui altère de façon permanente le tissu de conduction du coeur foetal en développement.
En présence d’anti SSA et d’anti SSB, il y’a un risque de 2,5% de BAV chez le 1er enfant et un risque de 12-25% de
donner naissance à un 2ème enfant avec un BAV (3)
D’après le registre des lupus érythémateux avec BAV, les mères des enfants atteints de B.A.V. congénital peuvent
présenter des critères biologiques et chimiques de Lupus Erythémateux Disséminé dans 17% , de Syndrome sec dans
24% , de Syndrome auto immun indifférencié dans 20% . La mère est asymptomatique dans 33 % (3)
Quelques observations de BAV familial ont été rapportées. Il serait transmis sur le mode autosomique dominant. Il se
rencontre dans la même famille ou sur plusieurs générations.
Le dépistage fait appel au monitoring obstérical et se résume en la constatation d’une bradycardie soutenue sans
signes ni contextes de souffrance fœtale. Ainsi la constatation sur le tracé du RCF d’une bradycardie stable, soutenue
inférieur à 100 bpm ayant conservé de petites oscillations mais sans ralentissemen’ indépendant des contractions
utérines du travail doit faire évoquer le diagnostic de bloc auriculo- ventriculaire . (4)

Le diagnostic est établi à l’examen échocardiographique, réalisé au mieux, par un cardiopédiatre rompu à
cette exploration ; L’échocardiographie devant une suspicion de B.A.V devrait en assurer le diagnostic
rythmologique (écho TM) et identifier les anomaliess morphologiques (écho bidimensionnelle) éventuellement
associées au B.A.V. Le pronostic du B.A.V sera déterminé par l’echo doppler. La fréquence ventriculaire est basse
et a une valeur pronostic. En dessous de 60 bpm, il y a risque d’asystolie foetale ou d’arythmie ventriculaire grave
(4-5). D’où la nécessité d’une surveillance rigoureuse de ce paramètre.
Les modalités de la naissance et la prise en charge du nouveau né seront fonction de son évolution.
L’accouchement par voie basse est autorisé sauf en cas d’insuffisance cardiaque ou pour des raisons obstéricales.
Le diagnostic cardiologique, en étude bidimensionnelle, poursuivra deux objectifs : apprécier la tolérance
générale du B.A.V. et identifier les cardiopathies associées
Conclusion :
Les BAV congénitaux immunologiques sont associés à une lourde morbimortalité.
L’échographie-Doppler est essentielle pour leur dépistage dans la population à risque et pour leur
caractérisation. D’autres marqueurs, s’ils existent, méritent d’être identifiés et le rythme du dépistage
échographique reste à être mieux précisé. En cas de BAV complet, l’échographie reste le seul moyen efficace de
surveillance du fœtus, elle permet une évaluation pronostique. Elle doit guider la conduite à tenir obstétricale en
vue d’une éventuelle électrostimulation cardiaque à la naissance.
BIBLIOGRAPHIE :
(1) MORQUIO L - Sur une maladie infantile et familliale caractérisée par des modifications permanentes du pouls, des attaques syncopales et
épileptiques, et la mort subite. Arch. Mal. Enf., 1887; 4; 467.
(2) SCOTT J.S, MADDISON P.J, TAYLOR P.V et AL - Connective tissue disease antiboldies to rjbonucleoprotein and congenital heart block. N. Engl. J.
Med. 1983 ; 309 ; 209-212
(3) CARREIRA P, GUTTIEREZ–LARRAYA F, GOMEZ–REINO JJ - Successful intrauterine therapy with dexamethasone for fetal myocarditis and heart
block in a woman with systemic lupus erythematosus. J. RHEUMATOL 1993; 20: 1204-1207.
(4) FERMONT L, KACHANER J, SICRE P, PIECHAUD J.F, VILLAIN E - Diagnostic et traitement des troubles du rythme in utero. In relier J.P ; Progrès en
Néonatologie (7) - KARGER, BALE, 1987 : 11-23
(5) CRAWFORD D, CHAPMAN M, ALLAN L – The assessment of persistent bradycardia in prenatal life. Br J Obstet gynaecol 1985; 92 : 941-4
1
/
3
100%