Physique Sup PCSI1 Lycée Carnot – DIJON F. Mauny OPTIQUE LOI

Physique Sup PCSI1 Lycée Carnot – DIJON F. Mauny
PROGRAMME DE COLLE n°18 Semaine du 20/03 au 26/03
P
LAN DU COURS
:
M
OUVEMENTS DANS UN CHAMPS DE FORCE CENTRALE CONSERVATIF
M
OUVEMENTS DANS UN CHAMPS DE FORCE CENTRALE CONSERVATIF
1. Mouvements à forces centrales.
1.1 Force centrale, centre d’interaction.
1.2 Conservation du moment cinétique.
1.3 Un mouvement nécessairement plan.
1.4 Loi des Aires
2. Cas de forces centrales conservatives.
2.1 Energie potentielle, conservation de l’énergie mécanique.
2.2 Energie potentielle effective.
2.3 Etats liés et états de diffusion.
3. Cas des champs newtoniens.
3.1 Définition. Lois de forces naturelles. Energies potentielles.
3.2 Nature des trajectoires.
Equation polaire et interprétation dans le cas d’un système lié ou d’un système en état de diffusion.
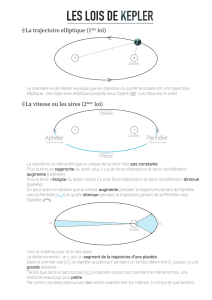
3.3 Lois de Kepler.
Enoncé des trois lois de Kepler et confrontation aux résultats plus formels établis en cours.
4. Mouvement circulaire en champs newtoniens.
4.1 Satellite à trajectoire circulaire.
4.2 Satellite géostationnaire.
4.3 Lois de Kepler sur le cas circulaire.
Démonstration de la troisième loi de Kepler pour une orbite circulaire. Généralisation (admise) au cas d’une trajectoire elliptique.
5. Energie mécanique.
5.1 Energie mécanique sur une trajectoire circulaire.
5.2 Energie mécanique sur une trajectoire elliptique.
5.3 Vitesses cosmiques : Vitesse en orbite basse ; Vitesse de libération.
5.4 Processus de mise en orbite, orbite de transfert.
O
PTIQUE
L
OI DE
M
ALUS
(polycopié, bilan de l’étude en travaux pratique)
Onde lumineuse, polarisation rectiligne.
Loi de Malus, justification
.
Polarisation rotatoire, loi de Biot.
T
HERMODYNAMIQUE
I
NTRODUCTION A LA DESCRIPTION DES SYSTEMES THERMODYNAMIQUES
L’objectif de cette partie est de donner les outils permettant une définition opérationnelle d’un système. L’introduction de l’équation d’état
du gaz parfait est l’occasion d’exercer ces capacités sur des exemples simples faisant intervenir des bilans de matière.
1. Définitions et généralités : système thermodynamique, systèmes isolés, fermés, ouverts. phase : phase gazeuse, phases
condensées liquide ou solide.
2. Description macroscopique d’un système.
2.1 Variables d'état.
Volume, température, pression.

Physique Sup PCSI1 Lycée Carnot – DIJON F. Mauny
2.2 Variables extensives, variables intensives.
3. Equilibre thermodynamique.
3.1 Définition, cas d’un système isolé ou non.
3.2 Condition d’équilibre :
Equilibre mécanique pour un système soumis aux seules forces de pression.
Condition d’équilibre thermique.
Exemple sur un gaz dans un cylindre fermé par un piston. Exemple pour une phase condensée indilatable et incompressible.
4. Equation d’état.
4.1 Cas du gaz parfait.
4.2 Cas des phases condensées (modèle du fluide incompressible et indilatable).
4.3 Volumes molaires, volumes massiques. Exemple pour l’air et pour l’eau dans différentes conditions.
4.4 Densité d’un fluide.
5. Mélange idéal de gaz parfaits.
5.1 Idéalité du mélange.
5.2 Pression partielle, loi de Dalton
5.3 Masse molaire moyenne.
TOUT EXERCICE SUR LES MOUVEMENTS A FORCE CENTRALE (voir programme de colle semaine 17)
P
ROGRAMME DE REFERENCE
:
Le bloc 5 est motivé par ses nombreuses applications. On se limite à discuter la nature de la trajectoire sur un graphe donnant l’énergie
potentielle effective et on ne poursuit l’étude dans le cas d’un champ newtonien (lois de Kepler) que dans le cas d'une trajectoire circulaire. Le
caractère elliptique des trajectoires associées à un état lié est affirmé sans qu’aucune étude géométrique des ellipses ne soit prévue ; on utilise
dans ce cas les constantes du mouvement (moment cinétique et énergie mécanique) pour exprimer l’énergie de la trajectoire elliptique en
fonction du demi-grand axe. Enfin l’approche de l’expérience de Rutherford est exclusivement documentaire : tout calcul de la déviation est
exclu, il s’agit en revanche d'utiliser le graphe de l'énergie potentielle effective pour relier la distance minimale d'approche à l'énergie mise en
jeu.
Notions et contenus
Capacités exigibles
5. Mouvements dans un champ de force centrale conservatif
Point matériel soumis à un seul champ de force centrale. Déduire de la loi du moment cinétique la conservation du
moment cinétique.
Connaître les conséquences de la conservation du
moment cinétique : mouvement plan, loi des aires.
Énergie potentielle effective. État lié et état de diffusion. Exprimer la conservation de l’énergie mécanique et
construire une énergie potentielle effective.
Décrire qualitativement le mouvement radial à l’aide de
l’énergie potentielle effective. Relier le caractère borné à la
valeur de l’énergie mécanique.
Approche documentaire : Relier l’échelle spatiale
sondée à l’énergie mise en jeu lors d’une collision en
s’appuyant sur l’expérience de Rutherford.
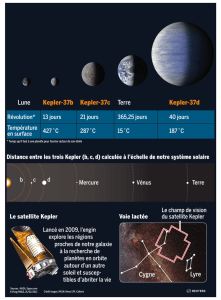
Champ newtonien. Lois de Kepler. Énoncer les lois de Kepler pour les planètes et les
transposer au cas des satellites terrestres.
Cas particulier du mouvement circulaire : satellite, planète. Montrer que le mouvement est uniforme et savoir calculer
sa période.
Établir la troisième loi de Kepler dans le cas particulier de
la trajectoire circulaire. Exploiter sans démonstration sa

Physique Sup PCSI1 Lycée Carnot – DIJON F. Mauny
généralisation au cas d’une trajectoire elliptique.
Satellite géostationnaire. Calculer l’altitude du satellite et justifier sa localisation
dans le plan équatorial.
Énergie mécanique dans le cas du mouvement
circulaire puis dans le cas du mouvement elliptique.
Exprimer l’énergie mécanique pour le
mouvement circulaire.
Exprimer l’énergie mécanique pour le
mouvement elliptique en fonction du
demi-grand axe.
Vitesses cosmiques : vitesse en orbite basse et vitesse
de libération.
Exprimer ces vitesses et connaître leur
ordre de grandeur en dynamique
terrestre.
1. Descriptions microscopique et macroscopique
d’un système à l'équilibre
Système thermodynamique. Identifier un système ouvert, un système
fermé, un système isolé.
État d’équilibre d’un système soumis aux seules forces
de pression.
Pression, température, volume, équation d’état.
Grandeur extensive, grandeur intensive.
Exemples du gaz parfait et d’une phase condensée
indilatable et incompressible.
Calculer une pression à partir d’une condition
d’équilibre mécanique.
Déduire une température d’une condition
d’équilibre thermique.
Connaître quelques ordres de grandeur de
volumes molaires ou massiques dans les
conditions usuelles de pression et de
température.
Connaître et utiliser l’équation d’état des gaz
parfaits.
1
/
3
100%