Série 1 - TuniSchool

Collège Sadiki
Passage entre les dérivés d’acides
(Pour les 4èmeSc.Exp seulement)
Série chimie n° : 12bis
Site web : http://cherchari.legtux.org / Facebook : https://www.facebook.com/mhamed.cherchari Cherchari
A- Rappel :
Les dérivés d’acides :
Dérivé d’acide
Ester
Chlorure d’acyle
Anhydride d’acide
Amide
Formule
générale :
Formule brute
CnH2nO2
Cn+1H2n+1OCl
CnH2n+1ON
Masse molaire
M=………….
M=…………..
M=……….
Exemple
………………………
…………….
………………………
………………………
……………..
………………
Préparation d’un ester :
Préparation d’un amide :
Nonsubstitué :
Monosubstitué :
''
32
'
Chlorure d acyle Chlorure d hydrogène
R C Cl HCl
Ammoniac Amide nonsubstitué
NH R C NH
Anhydride d acide Acide carboxylique
R C O C R R COOH
O
O
O
O
CH3-C
O
N-H
H
-O-
C-CH3
CH3-C
O
O
Cl
CH3-C
O
O-CH3
CH3-C
O
-O-
C-R
R-C
O
O
R-C
O
Cl
R-C
O
O-R’
R-C
O
N-R1
R2
''
''
'
Chlorure d acyle Chlorure d hydrogène
R C Cl HCl
Alcool Ester
R OH R C O R
Anhydride d acide Acide carboxylique
R C O C R R COOH
O
O
O
O
''
min
''
2
'
Chlorure d acyle Chlorure d hydrogène
R C Cl HCl
A e primaire Amide monosubstitué
R NH R C NHR
Anhydride d acide Acide carboxylique
R C O C R R COOH
O
O
O
45

Collège Sadiki
Passage entre les dérivés d’acides
(Pour les 4èmeSc.Exp seulement)
Série chimie n° : 12bis
Site web : http://cherchari.legtux.org / Facebook : https://www.facebook.com/mhamed.cherchari Cherchari
Disubstitué :
Remarque importante :
Si l’ammoniac est en excès on obtient le résultat suivant :
Si l’amine est en excès on obtient le résultat suivant :
B- Applications directes :
On donne les masse molaires atomiques en g/mol : C=12 ; O=16 ; N =14 ; Cl=35,5 et H=1
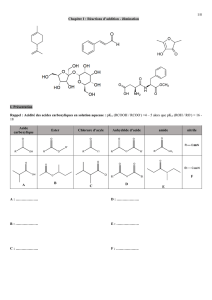
Exercice 1 :
1. Donner le nom des espèces chimiques suivantes et entourer le groupe fonctionnel.
a. C2H5-NH2 b. CH3-(-CH2-)3-NH2 c. d.
e. f.
2. donner la fonction organique de chaque composé.
Exercice 2 :
1. Compléter les équations suivantes :
a. ……. + NH3 → + HCl
b. + ….. → + …..
''
min sec
' " ' "
'
Chlorure d acyle Chlorure d hydrogène
R C Cl HCl
A e ondaire Amide disubstitué
R NHR R C NR R
Anhydride d acide Acide carboxylique
R C O C R R COOH
O
O
O
O
'
'4
232
''
4
Chlorure d ammonium
Chlorure d acyle NH Cl
R C Cl Ammoniac Amide nonsubstitué
NH R C NH
Anhydride d acide Carboxylate d ammonium
R C O C R R COONH
O
O
O
O
O
'
''3
min
2 ' '
2
''
'
3
Chlorure d alkylammonium
Chlorure d acyle R NH Cl
R C Cl A e primaire Amide monosubstitué
R NH R C NHR
Anhydride d acide Carboxylate d alkylammonium
R C O C R R COONH R
O
O
O
C
O
C2H5O C
OC2H5
C
O
CH3O C
OCH3
C
O
CH3N
HCH3
C
O
Cl
CH2
CH
CH3
CH3
C
O
NH2
CH2
CH2
CH3
C
O
Cl
CH2
CH2
CH3
C
O
NH
CH2
CH2
CH3
CH3
CH2
46

Collège Sadiki
Passage entre les dérivés d’acides
(Pour les 4èmeSc.Exp seulement)
Série chimie n° : 12bis
Site web : http://cherchari.legtux.org / Facebook : https://www.facebook.com/mhamed.cherchari Cherchari
2. Donner les noms et les formules semi-développées des réactifs (anhydride d’acide et ammoniac ou
amine) permettant d’obtenir les espèces chimiques suivantes :
a. b.
Exercice n° 3
Nommer les composés suivants et préciser pour chacun la fonction chimique à laquelle il appartient :
a- CH3-CH2-CO-O-CO-CH2-CH3. b- H-COOC2H5.
c-/ C3H7CONH-CH3. d- CH3-CH2-CH2-COCl.
C- Exercices de synthèse :
Exercice n° 1
On veut préparer du butanoate de propyle par action d’un alcool sur un chlorure d’acyle ou sur un
anhydride acide. Ecrire l’équation bilan pour chacune des deux réactions chimiques en précisant les
formules semi-développées et les noms des réactifs et des produits formés.
Exercice n° 2
1-En faisant agir du chlorure de thionyle SOCl2 ou du pentachlorure de phosphore PCl5
sur un acide carboxylique A, on obtient un corps B. La masse molaire de B vaut 92,5 g/mol
a) Quelle est la fonction chimique de B ?
b) Déterminer le nom et la formule semi-développée de l’acide A
2-Le corps B réagit avec l’ammoniac pour donner un corps organique cristallisé C. Quel
est ce corps ? Le nommer et écrire l’équation bilan de la réaction.
3-On se propose de préparer un ester comportant trois carbones à partir du méthanol. Pour parvenir à
ce résultat, écrire les équations des réactions qui peuvent se produire. Donner le nom de l’ester et
comparer les caractères de ces réactions.
Exercice n° 3
Une Amine saturée A contient 31,2%, en masse d’azote.
a. Donner sa formule brute b et écrire les formules semi-développées possibles pour A.
b. La réaction de l’amine A avec le chlorure d’éthaoyle a conduit à la N,N-diméthyléthanamide B
* Écrire la formule semi-développée de B. Préciser sa fonction chimique.
* En déduire la formule semi-développée de l’amine A et Ecrire les équations des réactions mis en jeu.
Exercice n° 4
Soit un composé organique de formule R1 - NH - R2
a-Quelle est la fonction chimique de ce composé ? R1 et R2 sont des groupes alkyles comportant au
moins un atome de carbone.
b-Quelle est la formule brute d’une amide dont la molécule renferme n atome ?
c-Un Amide du type R1-CO- NH – R2 contient en masse 16,09% d’azote. Quelle est sa
formule brute ? Ecrire la formule semi-développée et tous les isomères (amides)
d-L ‘un de ceux-ci est obtenu par réaction entre la méthylamine et le chlorure de propanoyle. Ecrire
l’équation bilan de la réaction et donner le nom de l’amide obtenu
C
O
CH3NH2
C
O
C6H5N
HC2H5
C
O
47
1
/
3
100%