Réactions d`Addition

1/8
Chapitre I : Réactions d’addition - élimination
I. Présentation
Rappel : Acidité des acides carboxyliques en solution aqueuse : pKA (RCOOH / RCOO-) ≈4 – 5 alors que pKA (ROH / RO-) ≈ 16 -
18
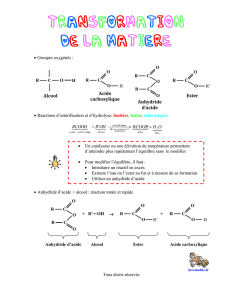
Acide
carboxylique
Ester
Chlorure d’acyle
Anhydride d’acide
amide
nitrile
A
B
C
D
E
F
A : ………………. D : ……………….
B : ………………. E : ……………….
C : ………………. F : ……………….
R OH
O
R O
O
R'
RCl
O
RO
O O
R'
RNH2
O
R C N
OH
O
O
O
Cl
O
Et O
OO
Et
N
O
Et C N

2/8
II. Réactivité : réaction d’addition - élimination
1. Electrophilie du carbone fonctionnel
2. Réaction d’addition – élimination (AN/E) : bilan et mécanisme général
Nu-
AN
acide carboxylique activé
ou dérivé d'acide
intermédiaire
tétraédrique
E
Z-
nucléophile
Attention :
3. Cas particulier des acides carboxyliques ( Z = OH):
Ion hydroxyde = très mauvais nucléofuge
Nécessité d’activer le groupe carboxyle :
- en milieu acide :
- en transformant l’acide carboxylique en dérivé d’acide :
Passage au chlorure d’acyle :
Passage à l’anhydride :

3/8
4. Réactivité comparée des dérivés d’acide
effets électroniques:
La réaction d’AN/E est facilitée si :
activé H+
activé H+ ou HO-
activé H+
activé H+
Bilan :
III. Synthèse des esters et des amides
1. A partir d’un chlorure d’acyle ou d’un anhydride
a. Synthèse des esters : REACTION QUASI-QUANTITATIVE OU TOTALE
Bilan :
A partir d’un chlorure d’acyle et d’un alcool :
Pour éviter la formation d’HCl(g) toxique, on réalise cette réaction en présence de pyridine, une base faible (pKa PyrH+/Pyr =
5,2) très peu nucléophile, qui joue aussi le rôle de solvant. Le bilan devient :

4/8
A partir d’un anhydride et d’un alcool :
Mécanisme avec un chlorure d’acyle:
.......
.......
.......
.......
b. Synthèse des amides : REACTION QUASI-QUANTITATIVE OU TOTALE
Bilan :
A partir d’un chlorure d’acyle et d’une amine :
HCl
=
Pour éviter la formation d’HCl(g) toxique, on réalise cette réaction en présence de pyridine, une base faible. Le bilan devient :
=
A partir d’un anhydride et d’une amine (qui peut jouer le rôle de base) :
=

5/8
Mécanisme avec un anhydride (d’acide):
CH3CH2COO-
CH3CH2COOH
......
.....
......
2. Synthèse d’un ester à partir d’un acide carboxylique :
Estérification de Fischer- REACTION EQUILIBREE RENDEMENT 67%
Bilan :
Mécanisme : valable sur des alcools primaires et secondaires
Mécanisme (en notant R’OH l’alcool et RCOOH l’acide carboxylique) :
(échange intramoléculaire
de protons)
3)
déprotonation: régénération du catalyseur acide
protonation: activation de l'acide carboxylique
H2O
A/B
AN
prototropie
E
A/B
2)
4)
1)
H+
 6
6
 7
7
 8
8
1
/
8
100%