d u C N H I M Béthanéchol

Dossier
Dossier
du CNHIM
Revue d’évaluation sur le médicament
Le Point sur
Fiche
Fiche
Fiche
Béthanéchol
Nutrition parentérale :
3 - Maladies inflammatoires
chroniques de l’intestin
Approche
pharmaco-économique
Cytochromes P 450 et
interactions médicamenteuses
Centre National Hospitalier d’Information sur le Médicament
ISSN 0223.5242
Publication bimestrielle
2000, XX, 1 SOMMAIRE
2000, XXI, 1

Dossier du CNHIM
Dossier du CNHIM
2000 Tome XXI, 1
Tous les articles publiés dans DOSSIER sont le fruit d'un travail col-
lectif, sur le fond et sur la forme, entre les Rédacteurs-Signataires, le
Comité de Rédaction, et la Rédaction du CNHIM d'une part, le
Comité de lecture et certains experts, spécialistes du sujet traité,
d'autre part. Sur chaque sujet, DOSSIER du CNHIM ne publie donc
pas les opinions de tel ou tel, mais réalise une analyse scientifique cri-
tique, la plus objective possible.
Directeur de la Publication :J.M. Kaiser
RÉDACTION
Rédacteur en chef :M.C. Husson
Secrétaire de rédaction :C. Fréville
Comité de rédaction :
D. Dardelle (), I. Debrix (Paris), C. Demange (St Dié), J.E. Fontan
(Paris), C. Guérin (Paris), B. Sarrut (Paris).
Secrétariat :M. Bouchot, F. Prince
COMITÉ DE LECTURE : C. Advenier (Versailles), P. Assayag
(Paris), A. Baumelou (Paris), P. Beaufils (Paris), C. Buffet (Bicêtre), D.
Brossard (Saint-Germain en Laye), D. Cabrol (Paris), A. Certain (Paris),
A. Escousse (Dijon), J.M. Extra (Paris), P. Faure (Paris), M. Feuilhade
de Chauvin (Paris), P. Gayral (Paris), P.M. Girard (Paris), J.C. Koffel
(Strasbourg), P. Maire (Lyon), C. Montagnier (Bayonne), M. Ollagnier
(St Etienne), B. Quinet (Paris), Ch. M. Samama (Paris), X. Sauvageon
(Paris), E. Singlas (Paris), G. Vedel (Paris), J.M. Vetel (Le Mans), T. Vial
(Lyon)
IMPRESSION :Express Service Est - 19, Bd Georges Bidault,
77183 Croissy-Beaubourg - Rythme de parution: 6 numéros par an
N° ISSN 0223.5242. N° de commission paritaire: 71987
CENTRE NATIONAL HOSPITALIER
D'INFORMATION SUR LE MÉDICAMENT (CNHIM)
7, rue du Fer à Moulin 75005 Paris - Tél. : + 33(0) 1 44 08 77 77 -
Fax : + 33(0) 1 43 36 76 49 - Email : [email protected]
Le CNHIM est une association indépendante à but non lucratif (loi
1901) dont la vocation est de dispenser une information rigoureuse
et scientifique sur le médicament.
Président :J.M. Kaiser
Président fondateur :A. Mangeot †
Directeur :M.C. Husson
Promotion :C. Grevot
Secrétariat-Abonnement :M. Bouchot, F. Prince
Conseil d'Administration :H. Allemand (Paris), P. Arnaud
(Rouen), A. Baumelou (Paris), A. Becker (Paris) , F. Berthet (St
Maurice), M.C. Bongrand (Marseille), O. Brault (Paris), S. Ferry
(Lyon), J.E. Fontan (Paris), B. Fragonard (Paris), M.C. Gaillot
(Paris), F. Gimenez (Paris), A. Graftieaux (Chalon sur Marne), G.
Hazebroucq (Paris), G. Johanet (Paris), J.M. Kaiser (Paris), PJ.
Lancry (Paris), J.F. Latour (Lyon), A.V. Lebelle (Angers), R.
Leverge (Paris), A.M. Liebbe (Compiègne), C. Penot-Ragon
(Marseille), JP Reynier (Marseille), M. Ricatte (Paris), A. Sarfati
(Ivry), B. Sarrut (Paris), B. Van Bockstael (Lomme), G. Willoquet
(Évry).
Les articles de Dossier du CNHIM sont indexés dans BIBLIO-
GRAPHIF ®. Le CNHIM a la propriété des textes publiés dans ce
numéro et se réserve tous les droits de reproduction (même partiel-
le), d’adaptation, de traduction, pour tous les pays et par quelque
procédé que ce soit (loi du 11 mars 1957, art. 40 et 41 du Code
Pénal art. 425).
Sommair
Sommaire
e
Échos du CNHIM Marie Caroline Husson
Le Point sur :
Béthanéchol
Éditorial Docteur Patrick
Tounian
Introduction
Pathologie et traitement actuel du RGO de l’enfant et du
nourrisson :
-Symptomatologie et moyens d’exploration du RGO chez l’enfant
et le nourrisson
-Traitements disponibles et stratégie
Préparations hospitalières de béthanéchol à usage pédia-
trique
-Forme PCH - AGAM
-Autres formes préparées en France par les pharmaciens
hospitaliers
Chlorure de béthanéchol à usage pédiatrique
-Propriétés physico-chimiques
-Propriétés pharmacodynamiques
-Propriétés pharmacocinétiques
Études cliniques chez l’enfant et le nourrisson
-Études cliniques non retenues
-Études cliniques comparatives randomisées
-Bilan des études cliniques
Place du béthanéchol dans la stratégie thérapeutique
-Intérêt du béthanéchol
-Comparaison béthanéchol - cisapride
Conclusion
Fiche : Nutrition parentérale :
3-Maladies inflammatoires chroniques de l’intestin
Fiche : Approche pharmaco-économique :
évaluation pharmaco-médico-économique de stratégies
thérapeutiques : éléments de méthodologie
Fiche : Cytochromes P450
et interactions médicamenteuses
2
3
5
5
10
17
17
18
18
20
20
20
20
23
23
26
40
52
Tarif 2000 (prix TTC)
Abonnement :Institutions hospitalières et Particuliers : 941,00 F,
Laboratoires : 1882,00 F,
Numéro:Institutions hospitalières et Particuliers : 178,00F
Laboratoires : 355,00 F (tarif dégressif envisageable).

Dossier 2000, XXI, 1 2
É
Échos du CNHIM
chos du CNHIM
Une nouvelle approche des évaluations de Dossier du CNHIM : la pharmaco-économie
Le sommaire de ce numéro 1 du nouveau millénaire, atypique voire disparate, témoigne de compétences bien spé-
cifiques de la profession de pharmacien des hôpitaux.
Tout d’abord un point sur le béthanéchol utilisé chez l’enfant et le nourrisson dans le traitement du reflux gastro-
œsophagien en seconde intention.
Ce médicament est dépourvu d’AMM en France. Il est fabriqué par quelques pharmacies hospitalières, la pharmacie cen-
trale des hôpitaux de l’AP-HP en particulier, sous le statut de préparation hospitalière.
Puis, une fiche, la troisième d’une série destinée à faire le point sur la place de la nutrition parentérale dans diffé-
rents contextes physiopathologiques spécifiques (1 - généralités, 2 - pancréatites, déjà traités), ici, les maladies inflamma-
toires chroniques de l’intestin, le Crohn en particulier (la prochaine traitera du sujet âgé).
Ensuite, une fiche de synthèse sur l’implication des différentes familles de cytochromes P450 connues à ce jour,
dans le métabolisme de divers médicaments, et les conséquences cliniques que cela peut entraîner au niveau des interac-
tions entre plusieurs médicaments en particulier.
Enfin, une dernière fiche, sur laquelle je souhaite attirer l’attention. Volontairement dense et informatif, cet article
présente des éléments de méthodologie utilisés dans les études de pharmaco-économie. Rédigé sous la houlette de Marie
Christine Woronoff-Lemsi (CHU de Besançon), il marque le départ d’une nouvelle approche, complémentaire, qui sera
désormais traitée dans les «évaluations thérapeutiques», ou les «points sur» de Dossier du CNHIM.
C’est un projet qui me tenait à cœur depuis plusieurs années, mais qui restait difficile à mettre en place.
Voilà qui est fait, je m’en réjouis.
En effet, dans le contexte actuel de maîtrise des dépenses de santé, et donc de choix les plus éclairés possible entre
plusieurs stratégies thérapeutiques - en termes de bénéfices obtenus au plan de la santé publique et des coûts correspon-
dants - la seule évaluation clinique ne suffit pas.
Notre objectif ici n’est pas de décortiquer les études économiques publiées comme les essais cliniques, mais de
les analyser, et de produire des conclusions permettant leur utilisation comme outil d’aide à la décision. Seules les études
impliquant les médicaments traités dans l’article seront sélectionnées, et cette sélection s’appuiera sur les recommanda-
tions édictées par M. Drummond*.
Merci à notre collègue de Besançon et son équipe d’initier ce travail.
Je forme le vœu que cette nouvelle implication de Dossier du CNHIM participe à la crédibilité que la pharmaco-
économie cherche encore à acquérir .
Marie Caroline Husson
Rédactrice en chef
Directrice du CNHIM
*Michael F. Drummond, Bernie JO’Brien, Greg L Stoddart, Georges W Torrance. Méthodes d’évaluation économique des pro-
grammes de santé. 2è édition. Traduction de MO Carrère. Paris, Ed Economica, 1998.

Dossier 2000, XXI, 1 3
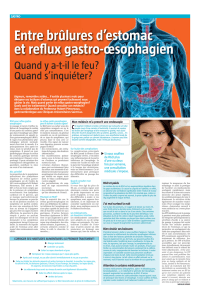
Le reflux gastro-œsophagien est-il LA maladie du nourrisson ?
On serait tenté de répondre positivement à la question-titre tant le reflux gastro-œsophagien (RGO) est rendu responsable
d'une multitude de maux chez le nourrisson. En effet, les pleurs (souvent attribués à des «coliques»!), les troubles du som-
meil, les difficultés à boire, l'irritabilité, les rhinopharyngites itératives, les otites répétées lui sont fréquemment attribués.
Mais la responsabilité du RGO est en fait loin d'être toujours évidente. Le RGO a également longtemps été considéré
comme une des causes principales de la mort subite du nourrisson. Les travaux récents qui ont montré que les nourrissons
allongés sur le dos faisaient deux fois moins de mort subite que ceux allongés sur le ventre a déculpabilisé en partie le
RGO puisque la position sur le dos aggrave significativement le RGO, comparée à la position sur le ventre.
La prescription excessive de certaines explorations du RGO est une des conséquences directes de cette accusation abusi-
ve. Ainsi, le moindre nourrisson qui pleure n'échappe pas à l'endoscopie digestive qui découvre la fameuse œsophagite
congestive (parfois dénommée de grade 1 pour faire plus savant), fournissant enfin une origine à ces pleurs, légitimement
angoissants, et soulageant alors parents et médecin traitant. Notre expérience démontre ô combien cette attitude est peu
justifiée et entachée de nombreuses erreurs, quant à l'appréciation de l'état de la muqueuse du bas-œsophage.
L'inexpérience de certains endoscopistes, ou la nécessaire rentabilité du coûteux matériel d'endoscopie, sont des explica-
tions possibles à ces "erreurs".
Ces nombreuses suspicions diagnostiques de RGO aboutissent bien évidemment à des traitements anti-reflux intempestifs.
On peut bien sûr constater, et se réjouir, que la sténose peptique de l'œsophage, qui constituait jadis une des complications
les plus redoutables du RGO, ne se voie plus de nos jours. Il est donc nécessaire de traiter les RGO du nourrisson, mais
point trop n'en faut ! Jusqu'à un temps pas encore très éloigné, le cisapride était presque autant prescrit aux nourrissons
que la vitamine D et le fluor, alors que dans la grande majorité des cas, de simples mesures posturales et diététiques étaient
suffisantes pour venir à bout de minimes régurgitations non compliquées.
Mais voilà que le cisapride fait peur car d'exceptionnelles observations de troubles du rythme cardiaque ont été rapportées,
dans tous les cas du fait d'une posologie élevée ou d'une association médicamenteuse proscrite. Ceci a conduit à une dimi-
nution de sa prescription, toutefois rapidement remplacée par celle de métoclopramide ou de dompéridone. Il est d'ailleurs
remarquable de noter qu'aucun travail randomisé et contrôlé n'a fait la preuve formelle de l'efficacité de ces deux dernières
thérapeutiques dans le RGO du nourrisson. Une fois encore, ce procès fait au cisapride est abusif. Comme tout médica-
ment il est nécessaire de respecter ses posologies et les associations médicamenteuses interdites.
Finalement, évitons d'accuser le RGO de tous les maux du nourrisson, mais sachons distinguer de banales régurgitations
d'un vrai RGO compliqué qui, lui, justifie bien sûr un traitement adapté et efficace. Ce traitement devra toujours débuter
par des mesures diététiques et posturales, clairement développée dans l'article qui suit, et, en cas d'échec de ces dernières,
aboutir à la prescription de prokinétiques. Le chef de file de ces derniers demeure le cisapride car il est le seul à avoir fait
la preuve de son efficacité dans des essais cliniques bien conduits. Il peut bien sur provoquer des effets indésirables, mais
les plus graves sont dus à des règles de prescriptions non suivies.
Et le béthanéchol dans tout cela ? Sa place dans le traitement du RGO est parfaitement précisée dans le travail qui suit. Il
doit en effet rester pour l'instant une thérapeutique de deuxième intention, car non seulement son efficacité dans le RGO
du nourrisson reste à démontrer, mais de plus ses effets indésirables sont probablement plus fréquents que pour le cisapride.
Docteur Patrick Tounian
Gastroentérologie et nutrition pédiatriques
É
Éditorial
ditorial

BÉTHANÉCHOL
DANS LE TRAITEMENT DU REFLUX GASTRO-ŒSOPHAGIEN
DE L'ENFANT ET DU NOURRISSON
Aymeric Moty*, Bernard Sarrut*
et la participation du comité de rédaction
*SIMP : Service d’information médicopharmaceutique de la PCH AP-HP
Remerciements : C. Faure (Paris), G. Hazebroucq (Paris), P. Tounian (Paris)
Dossier 2000, XXI, 1
Le Point sur
4
Résumé
Le chlorure de béthanéchol est un produit ancien, utilisé chez l’adulte dans plusieurs indications urologiques et digestives.
En pédiatrie, il est utilisé pour le traitement du reflux gastro-œsophagien primaire (RGO) chez l’enfant et le nourrisson.
Aucune spécialité contenant du béthanéchol n’a d’autorisation de mise sur le marché (AMM) en France.
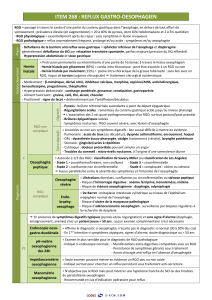
Le RGO est défini comme le passage involontaire d’une partie du contenu gastrique dans l’œsophage. Les RGO primaires
peuvent être classés en 2 catégories : le RGO non compliqué ayant pour seule manifestation des régurgitations, plus fré-
quentes en période post-prandiale, et le RGO dit compliqué car provoquant ou aggravant certaines affections (digestives,
oto-rhino-laryngées, broncho-pulmonaire, malaises graves du nourrisson et apnées).
Les méthodes d’exploration et de diagnostic du RGO ou de ses complications sont assez nombreuses, chacune ayant sa
spécificité, ses avantages et ses inconvénients : 1) la pH-métrie œsophagienne permet la mise en évidence d’un RGO acide
compliqué, non évident cliniquement ; 2) la fibroscopie œso-gastro-duodénale, examen de référence pour le diagnostic
d’œsophagite ; 3) l’examen radiologique ou technique du transit œso-gastro-duodénal (TOGD) permet de faire le bilan du
RGO avant la décision chirurgicale ; 4) la manométrie œsophagienne permet d’évaluer la motricité œsophagienne notam-
ment du sphincter inférieur œsophagien ; 5) l’échographie permet la recherche d’anomalies anatomiques ; 6) la scintigra-
phie au technétium permet l’étude de la vidange gastrique. Seule la pH-métrie œsophagienne permet de poser le diagnos-
tic du RGO.
Le but du traitement du RGO est de soulager les symptômes, de cicatriser les lésions éventuelles d’œsophagite et de pré-
venir les récidives et les complications. Selon l’ESPGAN (European Society of Paediatric Gastroenterology and
Nutrition), la prise en charge du RGO peut se faire en 5 phases : 1) rassurer les parents, administrer des médicaments épais-
sissants ; 2) administrer des prokinétiques : cisapride (et si les symptômes persistent dompéridone, métoclopramide) ; 3)
en thérapie adjuvante aux phases 1 et 2 : position anti-Trendelenburg (décubitus ventral avec une inclinaison de 30°, tête
surélevée) ; 4) anti H2(cimétidine, ranitidine) ou inhibiteurs de la pompe à protons (oméprazole) ; 5) chirurgie. Certains
auteurs ont recours aux antiacides. Le béthanéchol qui peut être classé dans les prokinétiques n’est pas explicitement pro-
posé dans le schéma proposé par l'ESPGAN. La place de la diététique reste discutée.
La Pharmacie Centrale des Hôpitaux de l’Assistance Publique - Hôpitaux de Paris (PCH - AGAM) fabrique un comprimé
dispersible à 1 mg de béthanéchol à usage pédiatrique. Il existe d’autres préparations hospitalières de béthanéchol.
Le béthanéchol est un parasympathomimétique direct, possédant des propriétés prokinétiques. Les données pharmacoci-
nétiques sont quasiment inexistantes.
Les essais cliniques contrôlés sont rares. L’étude d’Euler montre une efficacité statistique sur le gain de poids à 6 semaines
grâce à la diminution du nombre de vomissements. L’étude de Levi ne trouve pas de différence significative sur les scores
cliniques et le nombre de reflux entre le groupe béthanéchol et le groupe MAALOX® (anti-acide). Quelques effets indési-
rables ont été retrouvés : étourdissement, maux de tête, augmentation des vomissements, douleurs de la poitrine, anorexie,
bronchoconstriction. Il semble nécessaire de disposer d’études cliniques complémentaires pour confirmer les résultats dis-
ponibles.
Sa prescription ne se conçoit qu’après échec des autres moyens médicaux et après étude de la pression du sphincter infé-
rieur œsophagien par manométrie, son efficacité semblant en effet optimale en cas d’hypotonie sphinctérienne. Dans la
pratique, le béthanéchol est réservé aux RGO sévères de l’enfant et du nourrisson, le plus souvent après échec ou contre-
indication du traitement par le cisapride (toxicité cardiaque, nombreuses interactions médicamenteuses donnant lieu à des
torsades de pointes et à un allongement du QT) et après inefficacité constatée des mesures diététiques (laits épaissis) et
posturales.
Mots clés :béthanéchol, cisapride, enfant, nourrisson, pH-métrie, reflux gastroœsophagien,
Le Point sur Béthanéchol
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
1
/
54
100%