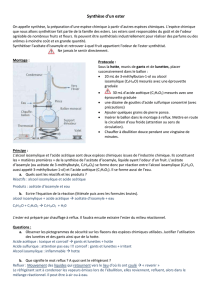
Synthèse Acétate Isoamyle : TP Chimie Organique

Sortie
d’eau
Entrée
d’eau
TP C5 SYNTHESE D’UN COMPOSE ODORANT, L’ACETATE D’ISOAMYLE
OBJECTIFS : Savoir mettre en œuvre une TECHNIQUE DE SYNTHESE CHIMIQUE
Savoir isoler le produit synthétisé
I) BUT DE LA MANIPULATION
Faire la synthèse d'un ester odorant : l'acétate d'isoamyle.
Données:
Masse volumique ( g.cm-3 )
Température d'ébullition (°C)
Solubilité dans l'eau pure
Acide acétique
1,05
118
très grande
Alcool isoamylique
0,81
128,5
faible
Acétate d'isoamyle
0,87
142
très faible
L'alcool isoamylique n'est absolument pas consommable et l'acide acétique est dangereux à manipuler.
II) MANIPULATION
1) REACTION D’ESTERIFICATION SOUS CHAUFFAGE A REFLUX
a) Dans un ballon (posé sur un valet si le fond n'est pas plat), introduire
successivement, à l'aide de la même éprouvette graduée (rincée entre les deux
mesures ) : 10 mL d'alcool isoamylique
puis 15 mL d'acide acétique pur (dit glacial).
b) Ajouter, avec précaution, quelques gouttes d'acide sulfurique concentré puis 3 à 5
grains de pierre ponce.
c) Réaliser le montage de chauffage à reflux en vous aidant du schéma :
d) Faire circuler l'eau froide dans le réfrigérant puis porter le mélange à ébullition
douce pendant environ 20 min.
e) Observer le reflux vers le ballon : le condensât qui se forme sur la paroi froide dans
le bas du réfrigérant retombe dans le ballon.
f) Au bout de 20 min, débrancher et enlever le chauffe-ballon.
g) Laisser refroidir le mélange réactionnel toujours sous reflux, d'abord à l'air, puis
dans une cuve contenant de l’eau froide.
2) LAVAGES ET DECANTATION
a) Dans le ballon (posé sur un valet si le fond n'est pas plat), ajouter environ 50 mL d'une solution concentrée de
chlorure de sodium (= eau salée).
b) Agiter doucement, puis transvaser le tout dans une ampoule à décanter, tout en retenant les grains de pierre
ponce.
Deux phases se séparent :
La phase organique supérieure contient l'ester, une partie de l'alcool qui n'a pas réagi et un peu d'acide acétique.
La phase aqueuse inférieure contient l'acide sulfurique et la majeure partie de l'acide acétique restant.
c) Evacuer, dans le ballon initial, la phase aqueuse inférieure et récupérer la phase organique dans un bécher.
d) A la phase organique, ajouter environ 50 mL d'une solution saturée d'hydrogénocarbonate de sodium. Cela
permet de neutraliser l’acidité du mélange formé (= transformer l'acide acétique en acétate de sodium).
Attention, une forte effervescence se produit, due à la formation de dioxyde de carbone.
e) Agiter avec l'agitateur en verre jusqu'à la fin de l'effervescence, puis remettre la solution dans l'ampoule à
décanter.
f) Agiter le mélange dans l'ampoule à décanter puis laisser à nouveau les phases se séparer avant d'évacuer
soigneusement toute la phase aqueuse dont on vérifiera, à l'aide d'un papier pH, qu'elle est encore légèrement
basique.
g) Recueillir l'ester odorant dans un bécher.
III) QUESTIONS
REACTION D’ESTERIFICATION SOUS CHAUFFAGE A REFLUX
1) Annoter le schéma de la page 2.
2) Indiquer le rôle du chauffage.
3) Que signifie le mot reflux ?

4) A quoi sert la colonne réfrigérante ? Que se
passerait-il si on ne mettait pas de colonne
réfrigérante ?
5) Quel est le rôle de la pierre ponce?
6) Pourquoi le réfrigérant doit-il rester ouvert
à l'extrémité supérieure ?
LAVAGES ET DECANTATION
7) Quel est le rôle de la solution concentrée de chlorure de sodium ? Indiquer le nom de cette étape.
8) Quel est le rôle de la solution saturée d'hydrogénocarbonate de sodium ? Indiquer le nom de cette étape et des
produits formés.
9)
a) Dessiner l'ampoule à décanter en indiquant où est la phase aqueuse
et la phase organique. Justifier les positions.
b) Indiquer dans quelle phase se trouve l'acétate d'isoamyle lors de la
décantation. Justifier.
c) Quelle est l’odeur de l’ester synthétisé ?
10) Compléter l'équation bilan de la réaction chimique de synthèse de l'acétate d'ïsoamyle :
Alcool isoamylique
+
Acide acétique
→
Acétate d'isoamyle
+
Eau
C5H12O
+
C2H4O2
→
………………………………
+
H20

LISTE DU MATERIEL.
Au bureau.
Elèves.
Verrerie et Matériel
Produits
- Ballon
- Condenseur à boules (réfrigérant)
- Plaque chauffante
- Support, noix, tiges, pinces
- 2 éprouvettes 25mL
- ampoule à décanter + support
- erlenmeyer + bouchon
- agitateur en verre
-
- Chiffon, éponge
- Lunettes, gants
- Acide sulfurique concentré
- Acide acétique pur
- Alcool isoamylique (3-méthylbutan-1-
ol)
- Solution saturée de NaHCO3
- Pierre pince
- Solution concentrée de NaCl
- Papier pH
1
/
3
100%