Mécanismes d`action du BCG : vers une approche

ARTICLE DE REVUE Progrès en Urologie (2000), 10, 1118-1126
1118
Mécanismes d’action du BCG : vers une approche thérapeutique
individualisée (ATI)?
Fabien SAINT, Jean-Jacques PATARD, Laurent SALOMON, Walid ALAMÉ, Antony CICCO,
Claude-Clément ABBOU, Dominique CHOPIN
Service d’Urologie, Hôpital Henri Mondor, Créteil, France
Les tumeurs superficielles de vessie sont caractérisées
par un fort potentiel de récidive et de progression, avec
cependant de grandes variations en fonction du stade et
du grade tumoral [47]. Ainsi , une tumeur T1G3 a 40%
de risque de progresser et un carcinome in situ (CIS) 60
à 80% [27, 31]. Le BCG est actuellement le traitement
préventif, de référence de la récidive et de la progres-
sion des tumeurs superficielles de vessie à haut risque
(CIS, PT1G3) [15]. De plus, ce traitement pourrait être
plus efficace si l’on procédait à des cures d’entretien ou
de réintroduction même si ce principe demande encore
une évaluation [28, 29, 44, 76]. Les résultats généraux
du BCG sont de l’ordre de 70% de patients sans récidi-
ve à 5 ans et de 45% de patients sans récidive à 15 ans
[70]. Les mécanismes d’action qui permettent au BCG
de réduire la récidive et la progression tumorale sont
associés à la présence d’infiltrats inflammatoires après
traitement [54, 57], à la production de cytokines uri-
naires produites par les lymphocytes T helper de type
Th1 (IL2) [18] ou à l’activation de cellules cyto-
toxiques (Natural Killer cells (NK), BCG Activated
Killer cells (BAK), Lymphokines Activated Killer cells
(LAK), lymphocytes gamma delta) [6]. Bien que les
mécanismes antitumoraux de cette réponse ne soient
pas complètement élucidé il est commode de distinguer
trois phases : une phase d’adhésion-internalisation, une
Manuscrit reçu : avril 2000, accepté : septembre 2000
Adresse pour correspondance : Dr. F.Saint, Service d’Urologie, Hôpital Henri
Mondor, 51, avenue du Maréchal de Lattre de Tassigny, 94010 Créteil Cedex.
e-mail : [email protected]
RESUME
La connaissance de l’immunité anti-tumorale et des mécanismes permettant à la
tumeur de s'affranchir de la surveillance immunitaire de l’hôte, a permis de pro-
gresser dans la compréhension des mécanismes d’action du Bacille Calmette-Guérin
(BCG). En effet, la réponse immunitaire locale endo-vésicale est intimement liée à
l’interaction de trois systèmes : l’hôte (le malade), le BCG (les mycobactéries) et la
tumeur. De cette interaction va naître une cascade d’évènements immunologiques,
dont certains seront indispensables à l’action protectrice du BCG contre la récidive
et la progression tumorale. On considère actuellement qu’il existe trois phases dans
la réponse immunitaire au BCG. Tout d’abord, le BCG adhère à l’urothélium puis
est phagocyté par des cellules présentatrices d’antigènes. A cette phase correspond la
libération précoce de cytokines dites inflammatoires (l’IL1, l’IL6, l’IL8). Ces cyto-
kines pourraient être en cause dans certains effets indésirables mais elles pourraient
également participer aux phénomènes cytotoxiques.
La deuxième phase est la reconnaissance des antigènes bactériens par des lympho-
cytes auxiliaires CD4, qui libèrent principalement de l’IL2 et de l’IFN (réponse
Th1). Cette activation cellulaire va aboutir à la troisième phase qui est l’amplifica-
tion de populations cytotoxiques capables de tuer les cellules tumorales: CD8, lym-
phocytes , macrophages, NK, LAK, BAK. Toutes ces cellules produisent elles aussi
des cytokines qui participent à la régulation de la réponse immunitaire.
La compréhension de ces mécanismes d’action, le dosage des cytokines urinaires, une
meilleure définition des cellules cytotoxiques et de leur rôle, l’évaluation moléculaire
de la tumeur et probablement certaines caractéristiques génétiques de l’hôte per-
mettront de proposer des protocoles d’immunisation plus efficaces en définissant une
approche thérapeutique individualisée (ATI).
Mots clés : Cancer de vessie, vaccin BCG, immunothérapie.

1119
phase de présentation antigénique, et enfin une phase
de cytotoxicité [53].
Actuellement, le mode d’action du BCG ne peut cepen-
dant plus être réduit à ces trois phases. En effet, de nou-
veaux facteurs liés à l’hôte et à la tumeur semblent
pouvoir conditionner la réponse au BCG. Le but de cet
article est donc de faire le point sur les connaissances
actuelles des mécanismes d’action du BCG en insis-
tant sur les interactions entre l’hôte, le BCG et la
tumeur. Ces interactions suggèrent la nécessité d’une
prise en charge personnalisée de type : approche théra-
peutique individuelle (ATI); cette approche prenant en
compte les caractères liés à l’hôte, à la tumeur et à la
réponse immunitaire. En effet, la détermination de pro-
tocoles d’immunisation plus efficaces (définition de la
dose, du nombre d’instillations, du type de traitement
d’entretien) doit probablement être associée à une
meilleure connaissance pré thérapeutique des trois enti-
tés fondamentales que sont: l’hôte, le BCG et la
tumeur.
LA REPONSE IMMUNE LOCALE
ENDOVESICALE APRES BCG
Le rôle de l’hôte
La réponse immunitaire aux infections par des germes
intracellulaires tels que les salmonelles, les leishma-
nioses ou les mycobactéries, et donc le BCG, est variable
et sans doute liée à l’hôte [69]. Chez la souris, un gène de
résistance à la vaccination par le BCG a été identifié. Ce
gène Nramp 1 (natural resistance associated macrophage
proteine) est impliqué dans la réponse T à la vaccination
par les mycobactéries [42]. Le produit de ce gène expri-
mé par les macrophages joue un rôle dans l’expression
des molécules de classe II du CMH, dans la présentation
antigénique chez l’homme et donc potentiellement dans
la réponse inflammatoire [42,69]. De plus Nramp1 pour-
rait contrôler la réplication des germes intracellulaires
par l’intermédiaire des phagozomes fabriqués par la cel-
lule infectée [24]. Il pourrait aussi inhiber le développe-
ment des mycobactéries en favorisant la production de
NO (Nitric oxide), puissant agent antimycobactérien [2].
Chez l’homme, les fonctions codées par Nramp 1 chez la
souris, seraient sous la dépendance de plusieurs gènes,
dont certains ont déjà été isolés sur le bras court du chro-
mosome 2 (2q35) [38]. L’identification de ces gènes et de
leur polymorphisme pourrait dans l’avenir être utile pour
prédire la réponse au BCG. Ce polymorphisme intéresse
aussi les antigènes du groupe HLA de classe II qui sont
impliqués dans la réponse aux mycobactéries [12].
La réponse immunitaire aux mycobactéries et au BCG
La réponse immunitaire aux mycobactéries est liée à
l’infection des cellules présentatrices d’antigènes
(monocytes, macrophages, cellules dendritiques) et est
associée à la production de cytokines telles l’IFN ,
l’IL12 et l’IL15. Ces cytokines participent à l’activa-
tion des lymphocytes T helper (CD4+) et peuvent don-
ner naissance : aux cellules T helper 1 (Th1) (produc-
trices d’IFN et d’IL2) associées à une forme localisée
de tuberculose ou T helper 2 (Th2) (productrices d’IL4
et d’IL10) et associées à une forme généralisée de la
maladie [70].
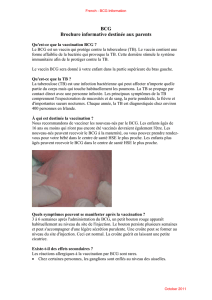
Lors de l’instillation endovésicale de BCG, les évène-
ments immunologiques sont assez comparables à ceux
rencontrés au cours des infections par les mycobacté-
ries et l’on peut distinguer trois phases: la phase d’ini-
tiation-internalisation, la phase de présentation antigé-
nique et la phase cytotoxique (Figure 1). Ces deux der-
nières correspondant à la phase effectrice.
La phase d’initiation est caractérisée par le contact
entre le BCG et l’urothélium. C’est RATLIFF en 1988
qui a montré dans un travail expérimental chez la sou-
ris, l’importance de l’adhésion du BCG aux cellules
urothéliales par l’intermédiaire de molécules d’adhé-
sion comme la fibronectine [40, 59, 60].
L’augmentation de la liaison à la fibronectine pouvant
majorer l’activité du BCG [32]. Cette adhésion des
mycobactéries peut aussi se faire par les glycosamino-
glycanes [66]. A partir de ce contact, les bacilles peu-
vent être phagocytés par les macrophages qui appar-
tiennent au groupe des cellules présentatrices d’anti-
gènes ou être internalisés dans les cellules urothéliales
ou les cellules tumorales [3]. En 1992, LA
TTIME
a
démontré que les cellules urothéliales pouvaient se
comporter comme des cellules présentatrices d’anti-
gènes [45]. Cette étape d’adhésion, de pénétration et
d’activation des cellules présentatrices d’antigènes est
F. Saint et coll., Progrès en Urologie (2000), 10 1118-1126
Figure 1. Représentation schématique de la réponse immuni -
taire au BCG : adhésion, internalisation, présentation antigé -
nique et cytotoxicité.Les communications entre les cellules
immuno-compétentes étant modulées par la production de
cytokines.La réponse Th1 (IL 2, IFN ) était associée à une
réponse antitumorale efficace.

une étape importante de la réponse aux mycobactéries
et de la réponse au BCG [20].
La phase effectrice est caractérisée par la présentation
par les cellules présentatrices d’antigènes (APC) aux
lymphocytes T auxiliaires, de certaines des protéines de
constitution du BCG ou produites par sa dégradation
(protéines immunogéniques) puis par l’activation de
cellules cytotoxiques (Figure 2). Après l’infection par
les mycobactéries, les macrophages associés aux autres
cellules présentatrices d’antigènes, dont font partie les
cellules urothéliales [20, 45], manufacturent les anti-
gènes mycobactériens et relarguent un certain nombre
de cytokines (IL1, IL6, IL8, IL10, IL12, TNF , IFN ,
IFN ) [5, 18, 54]. Ces cytokines sont indispensables au
recrutement des cellules immunocompétentes (lympho-
cytes T, macrophages et des polynucléaires neutro-
philes) qui infiltrent la paroi vésicale en grand nombre
au cours des instillations [19, 57] et ce, parallèlement à
la surexpression de molécules d’adhésion (ICAM1) et
de costimulation (B7). Ces cytokines amplifient proba-
blement les phénomènes de présentation antigénique en
majorant la présence de molécules d’adhésion comme
cela a été démontré in vitro pour l’IFN gamma [34].
Les formes solubles de ces molécules d’adhésion
(ICAM1) sont aussi retrouvées dans les urines après
BCG endo-vésical [36], ainsi qu’une surexpression des
molécules du complexe majeur d’histocompatibilité
(CMH) de classe I et II par les cellules urothéliales [36,
67, 71]. Ces molécules du CMH de classe I et II sont
impliquées dans les phénomènes de présentation anti-
génique [45, 58] puisque les antigènes exogènes sont
habituellement présentés par les molécules du CMH de
classe II et les antigènes endogènes par les molécules
de CMH de classe I. Les molécules du CMH de classe
II sont exprimées uniquement par les APC (macro-
phages, monocytes, lymphocytes B, cellules dendri-
tiques, cellules endothéliales) alors que les molécules
du CMH de classe I sont exprimées par toutes les autres
cellules (sauf les hématies et les ovocytes). Ces anti-
gènes exogènes sont dégradés par les lysosomes et
ensuite présentés à la surface des cellules présentatrices
d’antigènes, liés aux molécules du CMH de classe II.
Ce complexe peptide antigène et molécules du CMH
de classe II est alors présenté au CD4+ (T helper) [1].
Dans ce système l'IFN stimule le pouvoir de phagocy-
tose des macrophages et leur production d'endotoxines.
Ces phénomènes sont associés à une surexpression des
molécules d'adhésion ICAM1, LFA3 (APC) et de costi-
mulation B7-1 et B7-2 (APC), CD28 (lymphocytes T);
ils amplifient probablement la réponse associée aux
phénomènes de présentation antigénique [16]. Les anti-
gènes endogènes sont liés aux molécules du CMH de
classe I après avoir été préparés dans le réticulum
endoplasmique et adressés à la surface des cellules où
ils sont reconnus par les lymphocytes CD8 [7]. Les
cytokines favorisent donc l’action des lymphocytes
cytotoxiques [71], et ce, en plus de l’activité cyto-
toxique propre qu’elles possèdent à l’égard des cellules
tumorales [26, 35, 62]. Cette activation des cellules T
par le BCG est indispensable à la réponse antitumorale
et a été démontrée par des travaux sur l’animal de
RATLIFF [59]. Les mycobactéries induisent préférentiel-
lement des cytokines qui correspondent à une réponse
de type Th1 (IL2, IL12, IFN ), réponse favorable au
développement d’une immunité cellulaire [25, 52]. La
réponse Th1 favorise l’expansion et la prolifération des
cellules cytotoxiques et se caractérise par l’expression
de certaines cytokines comme l’IL2 ou l’IFN . Cette
réponse Th1 (IL2, IFN ) est détectée dans les urines
des patients après instillation de BCG endovésicale et
est liée au pronostic de la maladie [19]. De même après
BCG endovésicale il existe une surproduction d’ARN
messager d’IL2 dans les cellules monucléaires périphé-
riques, phénomène qui est corrélé à une bonne réponse
au BCG [39]. Mais cette réponse au BCG n’est proba-
blement pas linéaire, probablement pas uniquement
corrélée aux doses d’instillation, mais plutôt liée au
schéma instillatoire. Trois questions demeurent actuel-
lement sans réponse : quelle est la dose optimum de
BCG par instillation? quel schéma instillatoire ? quel
est le rôle du traitement d’entretien? le nombre de colo-
nies de bacilles vivants nécessaire pour induire une
réponse immunitaire bénéfique reste à définir. Le fait
de disposer de préparation de BCG lyophilisé autori-
sant une plus grande reproductibilité des lots est un
avantage certain pour le contrôle de la dose et devrait
permettre de répondre dans l’avenir à ces questions. En
effet, le nombre de colonies de bacilles vivants influen-
ce probablement l’effet thérapeutique, en modulant le
type de production de cytokine. C’est PAGANO qui, en
1992, a démontré que les demi-doses avaient une effi-
cacité thérapeutique identique ou supérieure aux doses
standards [50]. Certaines expériences chez l’animal
suggèrent que de fortes doses sont capables d’induire
une immunosuppression et des profils de production de
1120
Figure 2. Les phénomènes de présentation antigéniques liés
au contact avec le BCG (APC/lymphocytes T helper).
F. Saint et coll., Progrès en Urologie (2000), 10 1118-1126

cytokines de type Th2 [43]. Expérimentalement, l’aug-
mentation des doses provoque une inversion de la
réponse, associée probablement à une réponse T sup-
pressive Th2 caractérisée par la production d’IL4,
d’IL10, d’IL5, d’IL6, favorable à une réponse immuni-
taire humorale [39, 45]. Ainsi la production d'IL4 pour-
rait favoriser la croissance de lymphocytes B, l'activa-
tion du complément (C3a, C5) et réduire l'expression
de l'IL1 et du TNF . Une étude conduite par notre
équipe a montré que lors des instillations endovésicales
de BCG, la production d’IFN se faisait à partir de la
troisième instillation avec un pic à la quatrième et cin-
quième instillation. La production d’IL10 apparaissait
dès la quatrième instillation pour augmenter jusqu’à la
sixième. Cette production d’IL10 apparaissait réaction-
nelle à celle de l’IFN , avec un aspect suggérant un
rétro contrôle négatif de la production d’IFN , la pro-
duction d’IL2 étant parallèle à celle de l’IFN [52]. La
cinétique des cytokines était différente lors d’une
deuxième cure de BCG avec de l’IL2 principalement
produite lors des 3 premières instillations [63]. Le
maniement de cette immunothérapie pourra certaine-
ment être optimisé par la connaissance des facteurs liés
à l’hôte et par l’utilisation de marqueurs de la réponse
immunitaire comme le dosage des cytokines urinaires.
Les cytokines induites par le BCG commandent ou
régulent une réponse cellulaire à vocation cytotoxique,
partie intégrante de la phase effectrice. Les cellules
cytotoxiques le plus fréquemment décrites dans la paroi
vésicale après instillations endovésicales sont de type
CD8+. Expérimentalement, les lymphocytes (CD4+
et CD8+) sont indispensables au développement d’une
réponse contre les mycobactéries [61]. Les cellules
CD8+ semblent avoir un effet cytotoxique par l’inter-
médiaire de molécules d’adhésion (ICAM1) et/ou par
l’intermédiaire du système Fas présent sur les cellules
cibles tumorales. La population de lymphocytes CD4+
/CD8+ est augmentée dans la vessie après instillations
endovésicales avec une prédominance des CD4+ [57].
Les lymphocytes CD4+ produisent des cytokines
capables d’induire la maturation de lymphocytes cyto-
toxiques [72]. L’activité antitumorale liée au CD4+ est
liée à l'interaction entre Fas, le CD40 et leurs ligands
[77]. En effet, les interactions entre le CD40 (glycopro-
téine membranaire de la famille du récepteur au TNF)
et son ligand semblent jouer un rôle important dans
l’activation des lymphocytes T cytotoxiques et favori-
sent la réponse Th1 [4,23]. L'expression du ligand de
CD40 à la surface des lymphocytes T pourrait augmen-
ter la survie des monocytes en les protégeant des phé-
nomènes apoptotique dans les sites de l'inflammation
[23]. De plus l’expression du CD40 à la surface des cel-
lules tumorales pourrait intervenir comme un substitu-
tif aux cellules présentatrices d’antigène en favorisant
l’apoptose induite par les cellules CD4+ exprimant le
ligand de CD40 à leur surface [9]. De même, les lym-
phocytes CD4+, par l'expression du ligand de Fas à leur
surface seraient capables d'induire l'apoptose des cel-
lules tumorales [49].
Plusieurs autres cellules cytotoxiques ont été mises en
évidence : les polynucléaires neutrophiles, les cellules
NK, BAK, LAK et les lymphocytes gamma delta ( ).
Les polynucléaires neutrophiles sont les cellules les
plus abondantes dans la paroi vésicale après instilla-
tions endovésicales de BCG [9]. Ces cellules sont
capables de produire des cytokines ou des récepteurs
solubles de cytokines comme le récepteur à l’interleu-
kine 1. Le récepteur soluble de l'IL1 est capable de
diminuer la production d’IL1, d’IL8 et de TNF , et par
conséquent, peut probablement diminuer la réponse
immunitaire [9]. D’autres cellules (BAK, LAK) possè-
dent un rôle cytotoxique direct contre les cellules
tumorales urothéliales in vitro [6, 8]. Ces cellules co-
expriment les marqueurs CD8+ et CD56+ à leur surfa-
ce, elles semblent pouvoir être classées dans les
"Natural Killer T cells", avec la possibilité de produire
de l’IL12 et d’initier une réponse antitumorale efficace
[17]. Leur mécanisme d’action pourrait faire intervenir
le système Fas-L/Fas ou Perforine/Granzym A et B
[22]. L’étude in vitro après BCG de l’urothélium nous
a permis de mettre en évidence peu de cellules NK et
nous a conduit à penser que les cellules cytotoxiques
effectrices étaient probablement d’une autre nature
[63]. Ainsi, les lymphocytes , qui sont activés spéci-
fiquement par les mycobactéries et qui ont une activité
cytolytique contre les cellules tumorales urothéliales in
vitro pourraient jouer ce rôle [76]. Ils n’expriment pas
habituellement le phénotype CD4 ni le phénotype CD8
et leur pouvoir de reconnaissance de l’antigène n’est
pas restreint par le CMH. Cette activité cytolytique
semble pouvoir être réactivée lors d’un deuxième
contact avec le BCG et pourrait être impliquée dans la
qualité de la réponse au BCG par un phénomène de
mémoire associé [30]. De plus, ces lymphocytes ont la
capacité de stimuler les autres populations lymphocy-
taires (CD4+, CD8+) en réponse à la stimulation anti-
génique [30]. Une étude par immunohistochimie,
conduite par notre équipe, a montré que l’expression
des lymphocytes T gd dans la paroi vésicale après BCG
était majorée par rapport à la situation pré-BCG, avec
un maximum à 3 mois post BCG [63]. De plus, certains
auteurs ont montré que le BCG était capable d’induire
la maturation des cellules dendritiques à partir de cel-
lules mononucléaires circulantes et de moduler l’ex-
pression de la molécule CD40 à la surface des cellules
urothéliales tumorales [73]. Cette expression du CD40
participerait à l’activation des lymphocytes T helper et
sensibiliserait les cellules tumorales à l’apoptose par
des mécanismes faisant intervenir le système Fas-L/Fas
[14,23]. Cette surexpression du CD40 et l’activation du
système CD40/CD40-L pourraient aussi participer à
l’activation des lymphocytes B et NK [16].
Associés à la production des cytokines, il existe des
1121
F. Saint et coll., Progrès en Urologie (2000), 10 1118-1126

protéines capables d'induire le recrutement de cellules
immunocompétentes comme les lymphocytes T ou les
monocytes : les chémokines [33, 55]. Plusieurs ché-
mokines ont été rapportées: IP10 (interféron inducible
protein 10), MCP-1 ou encore RANTES. Ainsi l'IP10
est induite par la production d'IFN et aurait un effet
antitumoral, antiangiogénique et régulateur de la
réponse immunitaire [55]. Le TNF aurait en synergie
avec l'IFN un effet positif sur la production de l'IP10
[46]. L'IP10 pourrait créer un environnement non favo-
rable à la croissance et à la progression tumorale par
une activité antiangiogénèse [55]. Pour d'autres auteurs
les chémokines (MCP-1 et RANTES) participent au
recrutement des monocytes et seraient liées à la survie
sans récidives après BCG [33]. Le rôle exact de ces
molécules dans les mécanismes d'action du BCG reste
cependant à préciser.
Mais quelle est la spécificité antitumorale de la répon-
se immunitaire créée par le BCG? Il est probable que
les mécanismes d’action du BCG passent par des
mécanismes spécifiques et non spécifiques. La théorie
d’une activité spécifique reste soutenue par la présen-
ce d’antigènes de rejet des tumeurs (TRA), antigènes
dont l’expression serait modulée par les gènes de la
famille MAGE (MAGE 1et 3) [51, 74].
Classiquement, ces antigènes de rejet des tumeurs sont
présentés à la surface de la cellule tumorale par les
antigènes de classe I du CMH et sont reconnus par les
lymphocytes T cytotoxiques CD8+ (CTL) (Figure 3).
Or, le traitement par BCG augmente l’expression des
molécules du CMH de classe I et II sur les cellules uro-
théliales [63] et l’expression des antigènes du CMH de
classe I semble lié à la réponse au BCG [65].
L’association à la présence de nombreux lymphocytes
CD8+ après BCG semble être un argument supplé-
mentaire pour penser qu’il existe une spécificité anti-
génique à la réponse au BCG. Les travaux de ZLOTTA
qui suggère des antigènes croisés entre le BCG et les
tumeurs vésicales renforcent cette théorie [78, 79]. De
plus, la présence de cellules BAK et peut être la décou-
verte prochaine d’anticorps antitumoraux liés aux TRA
pourraient confirmer cette hypothèse. La théorie d’une
réponse non spécifique est, pour sa part, liée à la pré-
sence de nombreux macrophages, polynucléaires neu-
trophiles et à la présence d’IL2 et d’IFN gamma après
BCG.
Le rôle de la tumeur
Après les facteurs génétiques liés au malade et à la qua-
lité de la réponse immunitaire, il existe probablement
des mécanismes de résistance développés par la tumeur
elle même, lui permettant d’échapper à la surveillance
immunitaire de l’hôte mais aussi au traitement par le
BCG (Figure 4). Dans un système immunitaire fonc-
tionnel et capable de détruire les cellules tumorales, les
lymphocytes au potentiel cytotoxique (NK, CTL, CD8,
LAK, CD4) sont capables d'induire l'apoptose des cel-
lules tumorales par l’intermédiaire du système
Perforine granzyme A et B ou par le système Fas-
L/Fas. Ces systèmes sont parfois non fonctionnels.
Ainsi, les lymphocytes cytotoxiques peuvent avoir un
déficit en système Perforine Granzyme A et B ou Fas-
L et ne pas être actifs contre la tumeur [22]. La tumeur
peut aussi échapper à ce système par diminution des
molécules de costimulations (B7) ou d'adhésion
(ICAM1) à sa surface, molécules nécessaires à la pré-
sentation des antigènes tumoraux aux lymphocytes
cytotoxiques. Elle peut aussi échapper à ce système par
la diminution des antigènes du CMH de classe I à sa
surface (anomalie des protéines de transport TAP-1),
privant ainsi les lymphocytes de leur pouvoir cyto-
toxique [13,16]. La perte de la fonction normale de P53
impliquée dans l’apoptose cellulaire et dans la répara-
tion des dommages causés au DNA [41, 56] peut aussi
empêcher les phénomènes normaux d’apoptose initiés
1122
Figure 3. Les différents types d’antigènes associés aux
tumeurs et potentiellement impliqués dans les mécanismes de
cytotoxicité antitumorale.
Figure 4. Mécanismes pouvant expliquer : l’échappement de
la tumeur à la surveillance immunitaire de l’hôte et à l’action
du BCG.
F. Saint et coll., Progrès en Urologie (2000), 10 1118-1126
 6
6
 7
7
 8
8
 9
9
1
/
9
100%