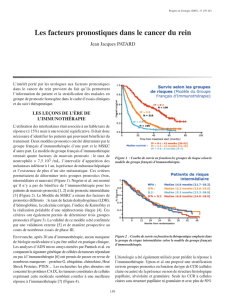
Les traitements du cancer du rein métastasé. Données

RESUME
Le cancer du rein métastasé garde un pronostic
sombre en raison du faible impact des possibili-
tés traditionnelles de traitement de cette
tumeur.
Les quelques survies prolongées obtenues après
chirurgie d'exérèse isolée de la tumeur primiti-
ve ou de ses métastases sont à rapprocher d'une
évolution parfois spontanément imprévisible et
il semble donc que la chirurgie d'exérèse isolée
ne permette pas le plus souvent d'augmenter la
survie des patients.
Parmi les traitements non chirurgicaux, la place
de la radiothérapie reste palliative et l'hormo-
nothérapie a fait la preuve de son inefficacité.
Récemment, de nouvelles approches thérapeu-
tiques se sont développées, qui laissent espére r
une amélioration possible du pronostic du can-
cer du rein métastasé. Parmi celles-ci, une
m e i l l e u re connaissance des mécanismes de chi-
mio-résistance du cancer du rein devrait condui-
re prochainement à l'utilisation de drogues aug-
mentant l'efficacité des chimiothérapies cyto-
toxiques sur cette tumeur. Enfin, les résultats
obtenus avec les nouvelles formes d'immunothé-
rapie font entrevoir de nouvelles possibilités thé-
rapeutiques immuno-chirurgicales.
Progrès en Urologie (1993), 3, 177-186
Le pronostic du cancer du rein métastasé reste
sombre. Moins de 10% des patients sont vivants à
5 ans et seulement 7% des patients sont vivants
sans tumeur (Tableau 1).
Le développement de nouveaux traitements, et
notamment de l’immunothérapie (voir l’article de
S. NÉ G R I E R dans ce numéro) rend nécessaire la
réévaluation des autres possibilités thérapeutiques,
proposées jusqu’à présent en cas de cancer du rein
métastasé.
HISTOIRE NATURELLE DES METASTASES
DU CANCER DU REIN
Pour évaluer l’efficacité des différents traitements
proposés dans le cancer du rein métastasé, il faut
tenir compte de son histoire naturelle parfois
imprévisible.
1. La localisation des métastases est en rapport
avec deux voies de dissémination principales [58]
La voie hématogène est de loin la plus importan-
te, conduisant jusqu’au poumon par l’intermédiaire
de la veine rénale, de la veine cave et de l’oreillette
droite. Environ 40 millions de cellules néopla-
Manuscrit reçu le 15 juin 1992
Adresse pour correspondance: Dr.F.Desgrandchamps, Service
d'Urologie, Hôpital Saint-Louis, 1, avenue Claude Vellefaux, ,
75010 Paris
Progrès en Urologie (1993), 3, 177-186
177
Les traitements du cancer du rein métastasé.
Données actuelles et perspectives
François DESGRANDCHAMPS (1), Olivier CUSSENOT (1) , Jean-Marie MARECHAL (2),
Ariane CORTESSE (1), Pierre TEILLAC (1), Alain LE DUC (1)
(1) Service d'Urologie, Pr.A. Le Duc, Hôpital Saint-Louis, Paris
(2) Service d'Urologie, Pr. J.M. Dubernard, Hôpital Edouard Herriot, Lyon
ARTICLES DE REVUE
Tableau 1. Pronostic global du cancer du rein méta -
stasé.
Nombre de Survie à Survie à Survie à
patients 1 an 2 ans 5 ans
Maldazys [29] 181 48% - 9%
De Kernion [6] 86 43% 26% 13%
Dineen [8] 29 - 41% 13%
Giuliani [14] 50 - - 7%

siques sont libérées par jour dans la veine rénale
pendant en moyenne 180 jours avant la néphrecto-
mie [15].
La voie lymphatique concerne les ganglions
locaux et régionaux, rarement les ganglions à dis-
tance.
Parmi ces voies de dissémination non spéci-
fiques, certaines correspondent à des localisations
métastatiques particulières
- La veine génitale permet la diffusion vers l’uretè-
re et les organes pelviens. Ces localisations corres-
pondent souvent à un cancer du rein gauche [9, 16,
22, 24, 35, 49].
- Les veines vertébrales conduisent préférentielle-
ment à des localisations secondaires vertébrales ou
du système nerveux central.
2. Les localisations secondaires surrénaliennes
sont à part
Le plus souvent ipsilatérales (5,5% des néphrectomies
é l a r gies pour cancer [39, 61]), elles correspondent soit
à des embols tumoraux (artériels, lymphatiques ou
veineux), soit à des extensions tumorales directes. La
fréquence respective de ces deux mécanismes est dis-
cutée [17] selon les séries, mais l’extension directe
semble être le mécanisme prépondérant en cas de
tumeur du pôle supérieur du rein [39].
Beaucoup plus rarement il s’agit de localisations
controlatérales, correspondant alors à une dissémi-
nation hématogène, où les localisations surréna-
liennes ne sont le plus souvent qu’un élément
d’une dissémination générale [19, 26, 62].
3. Les métastases surviennent en cascade
L’analyse des données d’autopsie de 687 cancers
du rein montre qu’en absence de métastase pulmo-
naire, il n’existe aucune autre localisation secon-
daire dans 73% des cas, alors qu’en cas de méta-
stase pulmonaire, une autre localisation est asso-
ciée dans 83% des cas [60].
Il s’agit donc d’une cascade métastatique dans
laquelle les métastases se développent initialement
dans les poumons et ne sont détectées que secon-
dairement dans les autres organes.
Cette étude ne permet pas de déterminer si cette
cascade est anatomique, chaque localisation secon-
daire étant elle-même la métastase d’une métastase
pulmonaire pré-existante, ou temporelle, toutes les
localisations métastatiques étant initiées en même
temps et se développant ensuite avec des vitesses
de croissance différentes.
4. Les sites métastatiques les plus fréquents
Ce sont, par ordre décroissant, les poumons, l’os,
le foie et le système nerveux central (Tableau 2).
Globalement, des métastases à distance sont pré-
sentes dans 23% des cas au moment du diagnostic
[l5].
5. Leur évolution est parfois imprévisible
En effet, des survenues tardives de métastases sont
possibles, même après 25 ans d’évolution [5, 55].
D’autre part, l’évolution des métastases du cancer
du rein n’est pas linéaire, mais ces métastases peu-
vent avoir des périodes spontanées de stabilité, de
régression ou d’accroissement rapide dans 20 à
30% des cas [57].
Enfin, des cas de régression spontanée de méta-
stases du cancer du rein sont décrits. Il s’agit d’une
éventualité rare, estimée à moins de 1% des cas
178
Tableau 2. Localisation des métastases du cancer du rein.
Maldazys [29] Giuliani [14] Pontes [43] De Kernion [6]
Poumon 75% 35% 42% 74%
Os 20% 35% 20% 41%
Foie 18% 9% 3% 10%
SNC* 7% 9% 3% 13%
Nombre de patients 181 50 69 86
* : SNC = Système nerveux central.

[52], qui concerne avant tout des métastases pul-
monaires. Plus de 80 cas de régressions de méta-
stases du cancer du rein ont été rapportés dans la
littérature [23], le plus souvent, cependant, sans
preuve histologique [28].
Néanmoins certains cas sont bien établis [2, 44,
52, 59], mais sont rapportées avec un recul insuffi-
sant (1 à 6 ans), et ne sont donc pas synonymes de
guérison.
L’ensemble de ces données permet de pondérer
l’interprétation de quelques survies prolongées
obtenues dans de courtes séries de traitements de
cancers du rein métastasés.
En effet, certains bons résultats apparents, avec un
recul limité, peuvent n’être que le reflet d’une his-
toire naturelle particulière des métastases du can-
cer du rein, et non l’effet du traitement étudié.
LES TRAITEMENTS DU CANCER
DU REIN METASTASE
1. Les traitements locaux
a) Place de la chirurgie dans le cancer du rein
métastasé
Une néphrectomie isolée, laissant une ou plu-
sieurs métastases en place, n’améliore pas la sur-
vie, qui est dans tous les cas très réduite: 5% de
survie à 3 ans dans une série de 80 patients [40].
Le gain de survie qui a pu être montré par cer-
taines équipes ne l’a été que dans des séries rétros-
pectives, utilisant des scores arbitraires, jamais
confirmés par des études prospectives [38, 40].
Par ailleurs, la nephrectomie n’augmente pas les
chances de régression secondaire des métastases,
et les rares possibilités de régression (0,8% dans
une étude cumulative de 474 patients) sont à com-
parer à la mortalité opératoire (qui est de 2,3 à
11% dans cette même étude) [36].
Plusieurs séries désormais “classiques” font état
d’un gain de survie en cas de chirurgie agressive
traitant à la fois la tumeur primitive et ses méta-
stases.
Après néphrectomie associée à l’exérèse d’une
métastase unique, MIDDLETON [34] sur 59 patients
dont 51 cas de la littérature, SKINNER [50] sur 41
patients, TOLIA et WHITMORE [56] sur 19 patients,
et DEKERNION [6] sur 20 patients, font état d’envi-
ron 30% de survie à 5 ans (Tableau 3).
Il s’agit cependant très rarement d’une survie sans
t u m e u r. La récidive est très fréquente, et survient
le plus souvent au cours de la première année post-
opératoire [6].
D’autres données plus récentes sont moins
encourageantes:
Dans une série de 29 patients traités par néphrecto-
mie et exérèse d’une métastase unique synchrone
ou non, la survie à 5 ans est de 13% des cas, quelle
que soit la localisation de cette métastase [8].
Ces résultats sont à rapprocher de ceux d’une série
complémentaire de 30 patients ayant une survie de
6,6% à 5 ans, sans différence de survie, ni en fonc-
tion de la durée de l’intervalle libre, ni en fonction
du nombre de métastases réséquées [43].
Le bénéfice réel, en terme de survie, d’une atti-
tude chirurgicale agressive isolée, sans traitement
complémentaire associé, reste donc discuté.
D’ailleurs, l’impression de bon pronostic qui peut
se dégager de certaines séries n’est souvent, de
l’avis même des auteurs, que le reflet d’une prése-
lection des patients aptes à être opérés [43].
A part la chirurgie symptomatique palliative:
- L’exérèse d’une tumeur primitive symptoma-
tique peut être justifiée dans certains cas pour
assurer une meilleure qualité de survie.
Cette indication est rare en fait, puisque les
tumeurs primitives symptomatiques sont peu fré-
quentes (28% des cas seulement), et sont le plus
179
Tableau 3. Survie après néphrectomie associée à l'exé -
rèse d'une ou plusieurs métastases, synchrones ou non.
Nb. Métastase
patients unique : U Survie à
multiple : M 5 ans
Middleton [34] 59 U 34%
Skinner [50] 41 U ou M 27%
Tolia [56] 17 U 35%
De Kernion [6] 20 U ou M 20%
Dineen [8] 29 U 13%
Pontes [43] 30 U ou M 6,6%

souvent bien contrôlées médicalement; par ailleurs,
les éventuels symptômes systémiques paranéopla-
siques peuvent être en rapport aussi bien avec la
tumeur primitive qu’avec ses métastases, et donc
ne pas régresser après néphrectomie [36].
- Le traitement chirurgical palliatif de métastases
osseuses, avec fractures pathologiques se justifie
sur un plan fonctionnel, bien que le taux de survie
ne soit que de 58% à 1 an [51].
b) Place de la radiothérapie dans le cancer du
rein métastasé
Les métastases du cancer du rein sont généralement
radiorésistantes .
Néanmoins, la radiothérapie garde quelques indica-
tions essentiellement dans le cadre d’un traitement
palliatif symptomatique.
Des doses cumulées même modérées (30 à 40 G)
peuvent en effet permettre une réduction des dou-
leurs osseuses métastatiques dans 77% des cas et
une réduction des tuméfactions des parties molles
dans 64% des cas. Lorsqu’il survient, cet eff e t
antalgique se maintient le plus souvent jusqu’au
décès du patient [18].
L’irradiation a moins d’effet sur les métastases du
système nerveux central (SNC) ou sur les compres-
sions médullaires: l’effet sur les symptômes est
modéré (moins de 30% d’amélioration), et une
réponse partielle sur le volume tumoral n’est obte-
nue que dans 20 à 30% des cas [18, 30].
L’utilisation d’une irradiation stéréotaxique
(“Gamma knife surgery”) [28], ou l’association à la
radiothérapie conventionnelle de l’exérèse d’une
métastase du SNC [1, 13] peut permettre d’amélio-
rer le pronostic, qui néanmoins reste sombre: mal-
gré un taux de récidive élevé (71%), la survie
moyenne en cas de métastase du SNC est supérieu-
re en cas d’association radio-chirurgicale (66
semaines) qu’en cas d’irradiation seule (13
semaines).
2 . Les traitements généraux du cancer du re i n
métastasé
Compte tenu du peu d’efficacité des traitements
locaux, même agressifs, l’amélioration du pronostic
du cancer du rein métastasé passe nécessairement par
le développement de traitements à visée générale.
a) Les thérapeutiques traditionnelles n’ont que
peu ou pas d'intérêt
L'hormonothérapie
Cette option thérapeutique repose sur les possibili-
tés expérimentales de blocage, par la progestérone,
de tumeurs du rein induites, chez le hamster, par les
oestrogènes.
En dehors de quelques résultats isolés [9], le traite-
ment hormonal par progestérone a fait la preuve de
son inefficacité comme traitement adjuvant dans le
cancer du rein métastasé [20, 41].
La chimiothérapie
Aucune chimiothérapie cytotoxique n’a fait la
preuve, jusqu’à présent, d’une efficacité régulière,
ni en mono, ni en polychimiothérapie [53].
Les efforts actuels tendent à réduire la toxicité des
chimiothérapies connues, ou à tenter d’augmenter
leur efficacité.
La délivrance de la chimiothérapie par l’intermé-
diaire de pompes implantables programmées peut
permettre d’en limiter les effets toxiques [21, 46].
Cette méthode basée sur des principes de chrono-
biologie, a été employée dans le traitement du can-
cer du rein métastasé avec des résultats encoura-
geants: 7,1% de réponse complète et 12,5% de
réponse partielle sur une série de 56 patients éva-
luables traités par perfusion continue systémique de
floxuridine (FUDR), avec peu d’effets secondaires.
Dans cette série, la médiane de survie n’est néan-
moins que de 15 mois [21].
Certaines molécules pourraient être utilisées pour
augmenter la chimiosensibilité du cancer du rein.
La chimiorésistance du cancer du rein entre en effet
dans le cadre des mécanismes de résistance pleio-
tropique, ou résistance multidrogues.
Il s’agit d’une résistance simultanée à diff é r e n t e s
drogues anti-cancéreuses. Cette résistance est due à
la présence d’une protéine portée par les mem-
branes cellulaires (appelée pl70), dont la fonction
est d’augmenter l’efflux actif du médicament,
c’est-à-dire de chasser le médicament hors de la
cellule.
Cette protéine est codée par un gène, mdr l, norma-
lement exprimé par certains tissus.
Le rein normal et 6 cancers du rein sur 8 ont une
180

surexpression de ce gène, ce qui rend probable-
ment compte de la chimiorésistance de cette
t u m e u r, par efflux actif des drogues cytotoxiques
[12]
Certaines molécules inhibent de façon compétitive
l’action de la protéine pl70, et permettent ainsi, in
vitro, une réversion de cette résistance.
Parmi ces molécules, les antagonistes calciques
(verapamil notamment) ont déjà été étudiés et
pourraient permettre d’augmenter la chimio-sensi-
bilité du cancer du rein en inhibant l’efflux actif
des drogues cytotoxiques. Cependant, jusqu’à pré-
sent, leurs effets secondaires en limitent l’utilisa-
tion chez l’homme.
Ainsi, actuellement, compte tenu de la faible effi-
cacité de la chimiothérapie, son utilisation dans le
traitement du cancer du rein métastasé, ne peut être
recommandée en dehors de protocoles d’évaluation
cliniques.
L'immunothérapie "traditionnelle"
L’importance des relations entre l’hôte et sa tumeur
a été soulignée depuis longtemps dans le cancer du
rein, en raison notamment des observations de
régressions spontanées de métastases (Cf. supra).
Ces relations où le système immunitaire semble
tenir une place prépondérante ont permis le déve-
loppement de conceptions thérapeutiques fondées
sur l’immunothérapie.
L’immunothérapie traditionnelle est active, c’est-à-
dire qu’elle stimule de façon exogène le système
immunitaire de l’hôte. Ce type d’immunothérapie
peut être spécifique, dirigée contre un groupe
d’antigènes tumoraux particuliers (“vaccination
tumorale”), ou non spécifique.
Pour augmenter de façon non spécifique les défenses
immunitaires de l’hôte (immunothérapie active nons-
pécifique), plusieurs molécules ont été employées
dans le cadre du cancer du rein métastasé.
Les principaux essais d’immunothérapie active non
spécifique ont surtout employé le BCG [32, 42].
D’autres molécules ayant des actions immunomo-
dulantes ont été utilisées, comme l’acide polynosi-
nic-polycytidilic (polyIC) qui augmente la cyto-
toxicité des lymphocytes en induisant la produc-
tion d'interféron [10], ou l’association de coumari-
ne qui a un effet mitogène sur les lymphocytes, et
de cimetidine qui a un effet inhibiteur des lympho-
cytes T suppresseurs [31].
Les résultats de cette immunothérapie active non
spécifique sont variables en fonction des molécules
utilisées: peu d’effet pour certaines (polyIC), ou
quelques rares réponses pour d’autres (BCG).
De bons résultats ont été obtenus avec l’association
coumadine-cimetidine, avec 3 réponses complètes
et 11 réponses partielles dans une série de 42
patients (soit 33% de réponse globale), mais ces
résultats obtenus au cours de cette étude prélimi-
naire n’ont pas été confirmés par d’autres équipes,
et semblent sans incidence sur la survie, puisque
dans tous les cas, ces régressions tumorales sont
transitoires [31].
L’immunothérapie active spécifique (vaccination
tumorale), est peu efficace.
En effet, des résultats discordants ont été obtenus:
- Un gain de survie significatif avait été montré
dans un groupe de 71 patients ayant eu une
néphrectomie suivie de vaccinations tumorales
répétées (fractions de tumeur autologue réinjectées
au patient), associée à une supplémentation diété-
tique particulière [54].
- Mais ces bons résultats n’ont pas été confirmés,
et plus récemment, d’autres études ont montré
l’inefficacité en terme de survie de l’immunothéra-
pie active spécifique.
Parmi celles-ci, dans une étude regroupant 33
patients recevant des vaccinations tumorales sous la
forme d’injections de cellules tumorales irradiées,
autologues ou non, aucune différence de survie n’a
été montrée entre deux groupes de patients “répon-
deurs” (24% de réponses partielles, aucune réponse
complète), et les patients non-répondeurs [25].
Ainsi, qu’elle soit spécifique ou non spécifique,
l’immunothérapie traditionnelle ne peut être consi-
dérée comme traitement efficace du cancer du rein
métastasé.
b) Les nouveaux développements de l'immuno -
thérapie
Les nouvelles approches de l’immunothérapie du
cancer du rein métastasé utilisent des cytokines,
molécules impliquées dans la régulation du systè-
me immunitaire.
181
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%