Lire l'article complet

9
La Lettre du Sénologue - n° 31 - janvier/février/mars 2006
altération des fonctions cognitives dans les suites d’un
cancer du sein et/ou de son traitement a longtemps été
un sujet “négligé”. Cependant, compte tenu de la fré-
quence de cette pathologie (une femme sur dix concernée dans
les pays occidentaux), des possibilités de rémission à long terme
et du retentissement de cette atteinte sur la qualité de vie, à
moyen et long terme, cet aspect est de plus en plus discuté à
l’heure actuelle. Les mécanismes physiopathologiques sous-ten-
dant cette atteinte sont loin d’être élucidés. Plusieurs hypothèses,
potentiellement intriquées, peuvent être discutées. Schématique-
ment, les troubles cognitifs peuvent être liés à la pathologie cancé-
reuse elle-même ou à son traitement, chimiothérapie et/ou hor-
monothérapie. La survenue de ces troubles pourrait, par ailleurs,
être favorisée par la susceptibilité de certaines patientes (prédis-
position génétique, statut hormonal…).
ÉVALUATION ET CARACTÉRISTIQUES
DES TROUBLES COGNITIFS
Une des premières difficultés est de préciser la définition et
l’ampleur de cette atteinte cognitive qui peut être faussée par le
ressenti psychologique des patientes (dû au type de pathologie,
aux contraintes thérapeutiques…) ou par la fatigue. De façon
schématique, on peut distinguer deux types d’altérations :
•
•Les altérations subjectives : elles sont fréquemment rappor-
tées par les patientes (jusqu’à 80% des cas après traitement sys-
témique dans certaines études). Les patientes se plaignent géné-
ralement de difficultés de concentration, mnésique et
attentionnelle. Cependant, la plupart des études montrent que
ces troubles subjectifs ne sont pas corrélés de façon statistique-
ment significative à une atteinte cognitive objective, ce qui
plaide plus en faveur de facteurs de stress psychologique que
d’une réelle atteinte cognitive.
•
•Les altérations objectives : elles sont identifiées à l’issue de
tests neuropsychologiques et sont retrouvées chez 16 à 50 %
des patientes selon les études.
La notion d’atteinte cognitive objective recouvre elle-même des
troubles très variés (troubles mnésiques, phasiques, attention-
nels, atteinte des fonctions exécutives, altération du raisonne-
ment…). Les localisations anatomiques et les circuits concernés
sont complexes, impliquant les zones corticales mais aussi les
circuits sous-corticaux et les noyaux gris centraux. On peut
schématiquement souligner l’importance de certains circuits
anatomiques tels que le système limbique, le circuit de Papez
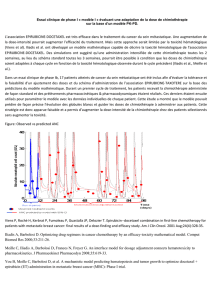
(figures 1 et 2) impliqués dans les fonctions mnésiques et com-
portementales, et le cortex préfrontal.
La caractérisation de l’atteinte cognitive lors du cancer du sein
reste difficile. La plupart des études sont en effet très hétéro-
gènes et souffrent de nombreux biais méthodologiques.
L’absence de consensus sur la méthode d’évaluation de ces
troubles constitue une première difficulté. Une évaluation com-
plète des fonctions cognitives passe par une batterie de tests
nécessitant un examinateur entraîné et peut prendre plusieurs
heures. Or, le nombre et le type de tests utilisés diffèrent sou-
vent d’une étude à l’autre, ce qui rend la synthèse délicate. Le
choix du groupe contrôle constitue également une source de
biais. Certaines études comparent les résultats obtenus à des
valeurs standard, d’autres utilisent comme groupe contrôle des
sujets sains ou des patientes suivies pour des cancer du sein,
mais traitées de façon différente. Enfin, il faut souligner que la
plupart des études publiées se fondent sur des effectifs de
patientes relativement faibles et hétérogènes.
Il ressort cependant de ces études que 16 à 50 % des patientes
présentent des troubles cognitifs objectifs généralement décrits
comme modérés semblant prédominer sur les fonctions mné-
siques (mémoire verbale notamment), l’apprentissage et les
fonctions psychomotrices.
TROUBLES COGNITIFS LIÉS DIRECTEMENT
AU CANCER DU SEIN
La pathologie cancéreuse en elle-même peut expliquer certains
troubles. De façon évidente, une dissémination cancéreuse
(méningée ou dans le parenchyme cérébral) ou une altération
métabolique secondaire au cancer (hypercalcémie…) peuvent
occasionner des troubles cognitifs. Ceux-ci s’intègrent en géné-
ral dans un contexte évocateur du diagnostic, leur physiopatho-
logie est connue et ne sera pas discutée plus avant.
Des troubles cognitifs (généralement sévères) peuvent égale-
ment survenir dans le contexte d’une encéphalite paranéopla-
sique, cependant ce tableau clinique est relativement rare dans
le cancer du sein. L’encéphalite limbique, typiquement associée
aux anticorps anti-Hu (1, 2), est généralement associée au can-
Physiopathologie des troubles cognitifs survenant
au cours et au décours de la prise en charge
d’un cancer du sein
Physiopathology of the cognitive disorders occurring after breast cancer treatment
●A. Amiel-Benouaich*
* Neurologue, service de neuro-oncologie, Pitié-Salpêtrière, Paris.
L
‘

DOSSIER
10
La Lettre du Sénologue - n° 31 - janvier/février/mars 2006
cer du poumon et n’a été qu’exceptionnellement décrite dans le
cancer du sein (3). Le syndrome paranéoplasique à anticorps
anti-Yo, typique d’un cancer gynécologique (ovaire ou sein) est
caractérisé cliniquement par une dégénérescence cérébelleuse,
mais l’association à des troubles cognitifs a été rapportée (4).
Des tableaux d’encéphalite paranéoplasique ont également été
décrits dans des cancers du sein associés à des anticorps anti-
Ma-2, anti-amphyphisine.
La physiopathologie des syndromes paranéoplasiques repose
sur une atteinte auto-immune (réaction antigénique croisée
entre antigènes tumoral et neuronal) ; la présence d’auto-anti-
corps antineuronaux est d’ailleurs un des critères diagnostiques,
bien que leur rôle pathogène reste débattu (5).
Une altération cognitive peut également survenir en dehors de ce
contexte. Peu d’études ont évalué les fonctions cognitives chez les
patientes avant traitement adjuvant mais celles-ci semblent modé-
rément altérées dans 12 à 36% des cas (6, 7) (mémoire verbale et
apprentissage). Dans l’étude de Wefel et al., portant sur 84
patientes, l’atteinte cognitive semble plus fréquente chez les
patientes en postménopause mais sans atteindre le seuil de signifi-
cativité (7).
L’implication des cytokines produites par la tumeur pourrait être
discutée (7, 8). Les cytokines produites en périphérie semblent, en
effet, avoir une action sur le système nerveux central. Des modifi-
cations du comportement ont pu être observées chez l’animal,
suite à une agression inflammatoire ou provoquées par l’adminis-
tration d’IL1 (léthargie, modifications du comportement d’explo-
ration…) (9). Chez l’homme plusieurs études, réalisées sur volon-
taires sains, montrent que l’induction de réaction de défense
impliquant l’IL6 et le TNFαentraîne une altération de l’humeur et
une diminution des performances mnésiques (10, 11).
TROUBLES COGNITIFS LIÉS À LA CHIMIOTHÉRAPIE
La chimiothérapie adjuvante est largement employée dans le
cancer du sein et son implication dans la survenue des troubles
cognitifs (phénomène parfois appelé chemobrain) est de plus en
plus étudiée sur le plan clinique et physiopathologique. La plu-
part des études souffrent des biais méthodologiques décrits pré-
cédemment (hétérogénéité thérapeutique, absence d’évaluation
pré- et post-thérapeutique, choix du groupe contrôle…) et sont
d’analyse discutable. Malgré ces réserves, plusieurs données
peuvent en être retenues :
•
•Malgré quelques travaux contradictoires (12), la plupart des
études retrouvent une atteinte cognitive objective et significa-
tive chez les patientes traitées par chimiothérapie (13-16).
D’après une étude de Wefel et al, comparant les performances
cognitives des patientes avant et après la chimiothérapie, 60%
des patientes souffrent d’une altération cognitive à un mois du
traitement (persistant à un an dans la moitié des cas) (6). Le
risque de développer des troubles cognitifs après chimiothéra-
pie haute dose adjuvante serait par ailleurs 8 fois plus élevé
qu’après un traitement locorégional (17).
•
•La constatation de troubles objectifs lors des tests neuropsy-
chologiques n’est souvent pas corrélée avec les plaintes fonc-
tionnelles des patientes (14, 17, 18).
•
•L’atteinte observée est généralement modérée. Elle concerne
principalement les fonctions mnésiques, verbales, visuo-spa-
tiales et, à un degré moindre, les fonctions exécutives, motrices
et d’apprentissage (15, 19-21).
•
•La survenue de ces troubles semble liée à l’intensité de la dose
reçue (32 % de troubles cognitifs à l’issue d’une chimiothérapie
haute dose versus 17 % après chimiothérapie conventionnelle et
9% dans le groupe de patientes sans traitement systémique) (17).
•
•Le caractère transitoire de l’altération cognitive est suggéré
par quelques études de suivi montrant une amélioration des per-
formances à distance du traitement (2 à 4 ans) (22-24).
Cependant, certaines patientes semblent souffrir d’une atteinte
cognitive durable, ainsi Ahles et al. retrouvent une altération
cognitive 5 à 10 ans après la chimiothérapie adjuvante (versus
traitement locorégional) (18).
Les techniques d’imagerie (conventionnelle ou métabolique)
Fornix
Hippocampe
Aire
entorhinale
Corps
mamillaire
Thalamus
Gyrus cingulaire
Figure 2. Schéma simplifié du circuit de Papez impliqué dans la
mémoire. Les neurones de l’hippocampe sont en communication via le
fornix, avec le tubercule mamillaire qui se projette sur le thalamus. Le
thalamus est connecté au gyrus cingulaire lui-même relié à l’aire ento-
rhinale et à l’hippocampe.
Figure 1. Anatomie simplifiée du système limbique. Le système limbique est
une formation anatomique impliquée dans la mémoire et dans le contrôle
des émotions. Il comprend notamment le gyrus cingulaire, la circonvolution
parahippocampique, l’hippocampe et l’amygdale, l’appareil olfactif (bulbe
olfactif, tractus olfactif).

11
La Lettre du Sénologue - n° 31 - janvier/février/mars 2006
ainsi que d’électrophysiologie ont été utilisées pour tenter de
mieux comprendre les altérations cognitives.
Plusieurs travaux mettent en évidence des modifications du paren-
chyme cérébral liées à la chimiothérapie touchant principalement
la substance blanche (25) mais également, dans certaines études, la
substance grise. En parallèle à ces modifications morphologiques,
le taux de N-Acétyl-Aspartate (marqueur d’intégrité neuronale
évalué en spectro-IRM) est altéré de façon modéré et transitoire ce
qui suggère des dommages neuronaux limités (26).
La chimiothérapie semble altérer de façon préférentielle certaines
zones cérébrales, notamment le cortex frontal et préfrontal ainsi
que les circuits de la mémoire. Ainsi lors de la réalisation d’une
tache mnésique, l’IRM fonctionnelle retrouve une augmentation de
l’activation de l’aire cingulaire (impliquée dans le circuit mnésique
de Papez) chez les patients traités par chimiothérapie. Par
ailleurs, la chimiothérapie provoque une diminution de l’acti-
vité métabolique (évaluée en PET-FDG) dans le gyrus préfron-
tal et dans l’aire de Broca, cette altération étant corrélée avec
des moindres performances mnésiques (27). Dans cette même
étude, le débit cérébral a été évalué lors de la réalisation de
tache mnésique (en utilisant de l’eau marquée). Celui-ci est
anormal chez les patientes traitées (versus le groupe contrôle
sain) notamment dans l’aire de Broca (9).
Les données d’électrophysiologie (EEG) suggèrent également un
retentissement cérébral de la chimiothérapie. Le temps de réponse
enregistré en EEG lors de l’exécution d’une tache est diminué chez
les patientes traitées par chimiothérapie (versus groupe contrôle
non traité) (28). Par ailleurs, Schagen et al. ont mis en évidence des
différences dans le rythme alpha mesuré entre les patientes traitées
par chimiothérapie conventionnelle, chimiothérapie haute dose et
groupe témoin (29) (sans corrélations franches avec les troubles
cognitifs observés cependant). La physiopathologie de cette
atteinte neurocognitive reste mal comprise et différents méca-
nismes probablement intriqués peuvent être discutés (30).
Neurotoxicité directe de la chimiothérapie
Celle-ci dépend probablement du type de chimiothérapie, de sa
capacité à franchir la barrière hémato-encéphalique et de la
dose administrée. L’atteinte cognitive semble plus importante à
l’issue de chimiothérapies utilisant le cyclophosphamide, le
méthotrexate et le 5-FU que de celles à base d’antracyclines.
Plusieurs drogues utilisées dans le cancer du sein sont effective-
ment connues pour leur potentielle neurotoxicité, notamment le
méthotrexate à forte dose. Des troubles cognitifs ont été rappor-
tés associé au 5-FU (liés à une leuco-encéphalopathie) (31, 32)
et au paclitaxel (33), mais le tableau clinique est généralement
plus sévère. Les effets vasculaires de la chimiothérapie pour-
raient également être impliqués. On sait, en effet, que la chi-
miothérapie peut altérer l’endothélium des vaisseaux sanguins
et entraîner des micro-infarctus cérébraux. De façon plus indi-
recte, l’atteinte vasculaire pourrait agir sur les fonctions cogni-
tives via une augmentation du taux d’IL1 et de cyclo-oxygé-
nase. Le rôle de l’aspirine comme neuro-protecteur chez ces
patientes est ainsi discuté par certains auteurs.
Mécanisme indirect lié aux conséquences hormonales
de la chimiothérapie
Les conséquences hormonales de la chimiothérapie sont fré-
quentes (ménopause induite chez la quasi-totalité des femmes à
l’issue d’une chimiothérapie haute dose et chez plus de 90 % des
femmes après une chimiothérapie conventionnelle [15]).
Mécanisme indirect lié à l’anémie chimio-induite
La délivrance d’O2 est fondamentale, car le tissu cérébral
dépend d’un métabolisme aérobie. Jacobsen et al. ont pu mon-
trer que l’anémie entraînait une altération des fonctions cogni-
tives (troubles mnésiques et de la concentration) (34). L’asso-
ciation de l’anémie à la fatigue, elle-même susceptible de
modifier les performances cognitives rend cependant l’analyse
de ces résultats difficile.
Plusieurs équipes se sont intéressées à l’impact positif de l’ery-
tropoiétine (susceptible de traverser la BHE) sur les fonctions
cognitives. Des études récentes suggèrent que son effet n’est
pas limitée à son action sur le taux d’hémoglobine. Il existe des
récepteurs cérébraux de l’érythropoéitine (35), exprimé par les
neurones, les astrocytes et les cellules endothéliales, principale-
ment au niveau du cortex frontal et de l’hippocampe. L’érythro-
poéitine aurait un rôle neuroprotecteur (36) (probablement en
bloquant l’apoptose) également contre des agressions diverses
(ischémie cérébrale, encéphalomyélite auto-immune et comitia-
lité induite par une neurotoxine, le kainaite). Se fondant sur ces
données, O’Shaughnessy et al. (37) ont comparé les perfor-
mances cognitives de 94 patientes recevant une chimiothérapie
adjuvante (antracycline) pour cancer du sein selon l’administra-
tion d’érytropoiétine versus placebo. Les performances cogni-
tives sont meilleures dans le groupe traité par l’érytropoéitine,
mais cette différence s’estompe dans les 6 mois suivant la fin
de la chimiothérapie, ce qui suggère une action réelle, mais
transitoire, de l’anémie sur les fonctions cognitives.
Terrain favorisant la survenue
des troubles neuropsychologiques
L’impact de certains facteurs génétiques, responsables d’une
vulnérabilité individuelle, est suspecté dans la survenue des
troubles cognitifs. Ainsi l’allèle e4 de l’apolipoprotéine E est
associé à une risque accru de démence dans la population géné-
rale et son implication dans la survenue des troubles cognitifs
postchimiothérapie a été évoquée par certaines équipes. Ahles
et al. ont ainsi montré que les patients porteurs de cet allèle et
traités par chimiothérapie (pour lymphome ou cancer du sein)
avaient des capacités cognitives moindres que ceux portant un
autre allèle de l’apolipoprotéine E (38). Il est vraisemblable que
d’autres facteurs individuels (concernant le métabolisme des
drogues, les capacités de réparation après une agression céré-
brale, les transporteurs de la barrière hémato-encéphalique…)
soient impliqués.
TROUBLES COGNITIFS LIÉS À L’HORMONOTHÉRAPIE
Action des estrogènes sur la cognition
L’impact neuroprotecteur des estrogènes sur les fonctions cogni-
tives est suggéré par de nombreux travaux (8, 19, 39), mais le
mécanisme d’action reste mal connu. Les estrogènes pourraient
être impliqués indirectement (effet préventif des AVC, modifica-
tion du profil lipidique) mais aussi directement. La plupart des
études ont été menées sur modèle animal et démontre l’existence
de récepteurs aux estrogènes (RE) dans le cerveau (les récepteurs

DOSSIER
12
La Lettre du Sénologue - n° 31 - janvier/février/mars 2006
REαet REβ) (40) notamment dans des zones impliquées dans les
taches cognitives (hippocampe, amygdale…) (8, 41).
Plusieurs études suggèrent que les estrogènes améliorent les
fonctions cognitives en agissant sur les neurotransmetteurs (33).
Les estrogènes semblent augmenter la densité des récepteurs
sérotoninergiques 5HT1 et moduler l’activité cholinergique
(41, 42). Ainsi sur modèle de rats ovariectomisés, le traitement
par estradiol permet une augmentation du taux d’acétylcholine
(43-45), du taux de récepteurs sérotoninergique 5HT2A et de
meilleures performances mnésiques (46, 47). Par ailleurs, les
estrogènes semblent exercer un effet positif sur les cellules hip-
pocampiques et favoriser la production de synapses (48, 49).
Chez la femme ménopausée, plusieurs études soulignent le rôle
positif du traitement hormonal substitutif sur les performances
cognitives et sur le risque de démence type Alzheimer mais cet
impact reste cependant controversé (40, 50-52).
Tamoxifène et troubles cognitifs
Le tamoxifène est un modulateur sélectif des récepteurs aux
estrogènes pouvant être à la fois antagoniste (REαet REβ)
mais aussi agoniste (récepteurs ERα) (40, 47) et son action sur
le fonctionnement cérébral est complexe. L’analyse de ce reten-
tissement est d’autant plus difficile qu’on dispose de peu
d’études (la plupart souffrant de biais méthodologiques) dont
les résultats sont contradictoires (40).
Pour certains auteurs, le tamoxifène n’a aucun impact sur la sur-
venue de troubles cognitifs (53, 54). D’autres études retrouvent un
rôle neuroprotecteur. Des données de spectro IRM sont en faveur
d’une action estrogene-like neuroprotectrice du tamoxifène (53)
(le tamoxifène, comme le traitement hormonal substitutif (THS)
provoque une diminution du taux de myo inositol). Dans l’étude
de Breuer (55), les patientes traitées par tamoxifène ont un risque
plus faible de maladie d’Alzheimer et de meilleures performances
cognitives que celles non traitées. Au contraire, Paganini-Hill et
al., en évaluant les fonctions cognitives de 1163 patientes (dont
710 traitées par tamoxifène) montrent que les troubles mnésiques
sont plus fréquents chez ces dernières mais s’améliorent à l’issue
du traitement (56). Le tamoxifène pourrait agir en bloquant l’effet
positif des estrogènes sur les récepteurs sérotoninergiques 5HT2A
(45), notamment concernant les cellules de l’hippocampe, ce qui
expliquerait les troubles mnésiques. Le tamoxifène semble égale-
ment agir dans les régions frontales où il entraîne une diminution
du métabolisme glucidique (évalué en PETscan) associée à des
altérations mnésiques (39).
Inhibiteur de l’aromatase et troubles cognitifs
L’aromatase est exprimée par les cellules neuronales chez plu-
sieurs espèces. Elle est notamment produite par les astrocytes en
réponse à une agression cérébrale et semble avoir un rôle dans la
réparation des atteintes cérébrales (57, 58). Les effets secondaires
des anti-aromatases semblent moins sévères que ceux du tamoxi-
fène, notamment sur le plan vasculaire, avec un risque moindre
d’AVC (59). Il existe peu de données sur le retentissement cogni-
tif de ce traitement (60). mais une étude de Weinfurt et al. rap-
porte une amélioration des fonctions cognitives chez les patientes
traitées par létrozole (61). L’impact de l’hormonothérapie sur les
fonctions cognitives, évalué lors de l’essai ATAC, retrouve
effectivement une amélioration de la mémoire verbale mais sans
que l’on puisse déterminer si cet effet est lié au tamoxifène et/ou
l’anastrozole (62). L’essai thérapeutique IBIS II, en cours actuel-
lement, comparant anastrozole versus tamoxifène, comporte une
évaluation neuropsychologique, ce qui devrait permettre de
mieux évaluer l’impact iatrogène de ce traitement.
CONCLUSION
La survenue de troubles cognitifs au cours du suivi du cancer
du sein est objectivée par de nombreuses équipes. Leurs carac-
téristiques et leur physiopathologie restent très imprécises,
notamment en raison de la grande hétérogénéité des études.
L’impact de la chimiothérapie est reconnu par la plupart des
auteurs (sans qu’un mécanisme précis puisse être avancé) alors
que l’implication de l’hormonothérapie (que ce soit en tant que
facteur protecteur ou aggravant) reste très controversée. Le
“flou” qui entoure cette atteinte est préjudiciable aux patientes,
en effet bien que généralement modérée, l’atteinte cognitive
peut potentiellement retentir sur leur qualité de vie à moyen et
long terme. À ce titre, les troubles cognitifs devraient pouvoir
être pris en considération lors des choix thérapeutiques, ce qui,
compte tenu de l’absence de consensus actuel, reste difficile.
Il semble donc important d’inclure ces considérations dans les
essais thérapeutiques randomisés, en utilisant des batteries de tests
neuropsychologiques plus consensuelles et plus uniformes.
■
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Graus F, Delattre JY, Antoine JC et al. Recommended diagnostic criteria for paraneo-
plastic neurological syndromes. J Neurol Neurosurg Psychiatry 2004; 75(8):1135-40.
2. Antoine JC, Honnorat J. Anti-neuronal antibodies and central nervous system diseases:
contribution to diagnosis and pathophysiology. Rev Neurol (Paris) 2000;156(1):23-33.
3. Rojas-Marcos I, Rousseau A, Keime-Guibert F et al. Spectrum of paraneoplastic neu-
rologic disorders in women with breast and gynecologic cancer. Medicine (Baltimore)
2003;82(3):216-23.
4. Gatti et al. Paraneoplastic neurological disorders in breast cancer. The Breast
2003;12:203-7
Cas pratique : exemple 1
Une patiente de 51 ans traitée pour cancer du sein par chi-
miothérapie (protocole FEC) consulte pour des difficultés
mnésiques et attentionnelles décrites comme modérées et peu
évolutives. L’examen neurologique est sans particularité.
L’ensemble du bilan est négatif : IRM cérébrale normale
(absence de métastases et d’atteinte de la substance blanche
notamment) bilan biologique et étude du LCR normale. Le
bilan neuropsychologique ne retrouve pas de déficit cognitif
objectif. Devant le caractère modéré de la plainte et
l’absence d’évolutivité, un suivi simple est décidé. L’examen
restant inchangé à 2 ans, l’hypothèse d’une atteinte pure-
ment subjective a été retenue chez cette patiente.
Cas pratique : exemple 2 (31)
Une patiente de 37 ans, traitée pour cancer du sein par chi-
miothérapie (5 FU, cyclophosphamide, épirubicine et carmo-
fur) développe dans les semaines suivant le début du traite-
ment une atteinte cognitive : troubles mnésiques, s’aggravant
progressivement puis apparition d’un syndrome frontal et
dégradation globale (mini-mental-status ou MMS évalué à
9/30). L’IRM montre alors un important hypersignal de la
substance blanche périventriculaire. La chimiothérapie est
arrêtée et un traitement empirique par méthylprednisolone IV
est adminitré. Une nette amélioration est obtenue en un mois
avec un MMS évalué à 29/30 et une disparition des lésions de
la substance blanche sur l’IRM de contrôle.

13
La Lettre du Sénologue - n° 31 - janvier/février/mars 2006
5. Sutton I. Paraneoplastic neurological syndromes. Curr Opin Neurol 2002;15(6):685-
90.
6. Wefel JS, Lenzi R, Theriault RL et al. The cognitive sequelae of standard-dose adjuvant
chemotherapy in women with breast carcinoma: results of a prospective, randomized, lon-
gitudinal trial. Cancer 2004;100(11):2292-9.
7. Wefel JS, Lenzi R, Theriault R et al. Chemobrain in breast carcinoma: a prologue.
Cancer 2004;101(3):466-75.
8. Minisini A, Atalay G, Bottomley A et al. What is the effect of systemic anticancer treat-
ment on cognitive function? Lancet Oncol 2004;5(5):273-82.
9. Tannock IF, Ahles TA, Ganz PA et al. Cognitive impairment associated with chemothe-
rapy for cancer: report of a workshop. J Clin Oncol 2004;22(11):2233-9.
10. Pollmacher T, Haack M, Schuld A et al. Low levels of circulating inflammatory cyto-
kines-do they affect human brain functions? Brain Behav Immun 2002; 16(5):525-32.
11. Reichenberg A, Yirmiya R, Schuld A et al. Cytokine-associated emotional and cogni-
tive disturbances in humans. Arch Gen Psychiatry 2001;58(5):445-52.
12. Donovan KA, Small BJ, Andrykowski MA et al. Cognitive functioning after adjuvant
chemotherapy and/or radiotherapy for early-stage breast carcinoma. Cancer
2005;104(11):2499-507.
13. Brezden CB, Phillips KA, Abdolell M et al. Cognitive function in breast cancer
patients receiving adjuvant chemotherapy. J Clin Oncol 2000;18(14):2695-701.
14. Schagen SB, van Dam FS, Muller MJ et al. Cognitive deficits after postoperative adju-
vant chemotherapy for breast carcinoma. Cancer 1999;85(3):640-50.
15. Falleti MG, Sanfilippo A, Maruff A et al. The nature and severity of cognitive impair-
ment associated with adjuvant chemotherapy in women with breast cancer: a meta-analy-
sis of the current literature. Brain Cogn 2005;59(1):60-70.
16. Tchen N, Juffs HG, Downie FP et al. Cognitive function, fatigue, and menopausal
symptoms in women receiving adjuvant chemotherapy for breast cancer. J Clin Oncol
2003;21(22):4175-83.
17. van Dam FS, Schagen SB, Muller MJ et al. Impairment of cognitive function in women
receiving adjuvant treatment for high-risk breast cancer: high-dose versus standard-dose
chemotherapy. J Natl Cancer Inst 1998;90(3)210-8.
18. Ahles T, Saykin AJ, Furstenberg CT et al. Neuropsychologic impact of standard-dose
systemic chemotherapy in long-term survivors of breast cancer and lymphoma. J Clin
Oncol 2002;20(2):485-93.
19. Phillips KA, Bernhard J. Adjuvant breast cancer treatment and cognitive function:
current knowledge and research directions. J Natl Cancer Inst 2003; 95(3):190-7.
20. Anderson-Hanley C, Sherman ML, Riggs R et al. Neuropsychological effects of treat-
ments for adults with cancer: a meta-analysis and review of the literature. J Int Neuropsy-
chol Soc 2003;9(7):967-82.
21. Jansen CE, Miaskowski C, Dodd M et al. A metaanalysis of studies of the effects of
cancer chemotherapy on various domains of cognitive function. Cancer
2005;104(10):2222-33.
22. Schagen SB, Hamburger HL, Muller MJ et al. Neurophysiological evaluation of late
effects of adjuvant high-dose chemotherapy on cognitive function. J Neurooncol
2001;51(2):159-65.
23. Schagen SB, Muller MJ, Boogerd W et al. Late effects of adjuvant chemotherapy on
cognitive function: a follow-up study in breast cancer patients. Ann Oncol
2002;13(9):1387-97.
24. Fan HG, Houede-Tchen N, Yi QL et al. Fatigue, menopausal symptoms, and cognitive
function in women after adjuvant chemotherapy for breast cancer: 1- and 2-year follow-
up of a prospective controlled study. J Clin Oncol 2005;23(31):8025-32.
25. Stemmer SM, Stears JC, Burton BS et al. White matter changes in patients with breast
cancer treated with high-dose chemotherapy and autologous bone marrow support. AJNR
Am J Neuroradiol 1994;15(7):1267-73.
26. Brown MS, Stemmer SM, Simon JH et al. White matter disease induced by high-dose
chemotherapy: longitudinal study with MR imaging and proton spectroscopy. AJNR Am J
Neuroradiol 1998;19(2):217-21.
27. Silverman DH, Castellon SA, Abraham L. Abnormal regional brain metabolism in
breast cancer survivors after adjuvant chemotherapy is associated with cognitive changes.
ASCO Annual Meeting Abstract n° 47, 2003.
28. Kreukels BP, Schagen SB, Ridderinkhof KR et al. Electrophysiological correlates of
information processing in breast-cancer patients treated with adjuvant chemotherapy.
Breast Cancer Res Treat 2005;94(1):53-61.
29. Schagen SB, Hamburger HL, Muller MJ et al. Neurophysiological evaluation of late
effects of adjuvant high-dose chemotherapy on cognitive function. J Neurooncol
2001;51(2):159-65.
30. Saykin AJ, Ahles TA, McDonald BC. Mechanisms of chemotherapy-induced cognitive
disorders: neuropsychological, pathophysiological, and neuroimaging perspectives.
Semin Clin Neuropsychiatry 2003;8(4):201-16.
31. Takimoto C, Lu ZH, Zhang R et al. Severe neurotoxicity following 5-fluorouracil-
based chemotherapy in a patient with dihydropyrimidine dehydrogenase deficiency. Clin
Cancer Res 1996;2(3):477-81.
32. Choi SM, Lee SH, Yan YS et al. 5-fluorouracil-induced leukoencephalopathy in
patients with breast cancer. J Korean Med Sci 2001;16(3):328-34.
33. Nieto Y, Cagnoni PJ, Bearman SI et al. Acute encephalopathy: a new toxicity associa-
ted with high-dose paclitaxel. Clin Cancer Res 1999;5(3):501-6.
34. Jacobsen PB, Thors CL, Cawley M et al. Relation of decline in hemoglobin to cogni-
tive functioning and fatigue during chemotherapy treatment. ASCO Annual Meeting Abs-
tract 1542, 2002.
35. Lewis LD. Preclinical and clinical studies: a preview of potential future applications
of erythropoietic agents. Semin Hematol 2004;41(4 Suppl 7):17-25.
36. Henry DH. The evolving role of epoetin alfa in cancer therapy. Oncologist
2004;9(1):97-107.
37. O’Shaughnessy JA, Vukelja SJ, Holmes FA et al. Feasibility of quantifying the effects
of epoetin alfa therapy on cognitive function in women with breast cancer undergoing
adjuvant or neoadjuvant chemotherapy. Clin Breast Cancer 2005;5(6):439-46.
38. Ahles TA, Saykin AJ, Noll WW et al. The relationship of APOE genotype to neuropsy-
chological performance in long-term cancer survivors treated with standard dose chemo-
therapy. Psychooncology 2003;12(6):612-9.
39. Eberling JL, Wu C, Tong-Turnbeaugh R et al. Estrogen – and tamoxifen – associated
effects on brain structure and function. Neuroimage 2004;21(1): 364-71.
40. Angelopoulos N, Barbounis V, Livadas S et al. Effects of estrogen deprivation due to
breast cancer treatment. Endocr Relat Cancer 2004;11(3):523-35.
41. McEwen BS, Alves SE. Estrogen actions in the central nervous system. Endocr Rev
1999;20(3):279-307.
42. Horwath. Neuroscience 2002.
43. Luine VN. Estradiol increases choline acetyltransferase activity in specific basal fore-
brain nuclei and projection areas of female rats. Exp Neurol 1985;89(2):484-90.
44. O’Malley DM, Sandell JH, Masland RH. Co-release of acetylcholine and GABA by
the starburst amacrine cells. J Neurosci 1992;12(4):1394-408.
45. Singh. 1994.
46. O’Neal MF, Means LW, Poole MC, Hamm RJ. Estrogen affects performance of ova-
riectomized rats in a two-choice water-escape working memory task. Psychoneuroendo-
crinology 1996;21(1):51-65.
47. Sumner BE, Grant KE, Rosie R et al. Effects of tamoxifen on serotonin transporter and
5-hydroxytryptamine(2A) receptor binding sites and mRNA levels in the brain of ovariec-
tomized rats with or without acute estradiol replacement. Brain Res Mol 1999;73(1-
2):119-28.
48. Tanapat P, Hastings NB, Reeves AJ et al. Estrogen stimulates a transient increase in
the number of new neurons in the dentate gyrus of the adult female rat. J Neurosci
1999;19(14):5792-801.
49. McEwen BS, Tanapat P, Weiland NG. Inhibition of dendritic spine induction on hip-
pocampal CA1 pyramidal neurons by a nonsteroidal estrogen antagonist in female rats.
Endocrinology 1999;140(3):1044-7.
50. Hormone therapy for the prevention of chronic conditions in postmenopausal women:
recommendations from the US Preventive Services Task Force. Ann Intern Med
2005;142(10):855-60.
51. Yaffe K, Krueger K, Sarkar S et al. Cognitive function in postmenopausal women trea-
ted with raloxifene. N Engl J Med 2001;344(16):1207-13.
52. Shilling V, Jenkins V, Fallowfield L et al. The effects of oestrogens and anti-estrogens
on cognition. Breast 2001;10(6):484-91.
53. Ernst T, Chang L, Cooray D et al. The effects of tamoxifen and estrogen on brain
metabolism in elderly women. J Natl Cancer Inst 2002;94(8):592-7.
54. Azcoitia I, Sierra A, Veiga S et al. Aromatase expression by reactive astroglia is neu-
roprotective. Ann N Y Acad Sci 2003;1007:298-305.
55. Breuer B, Anderson R. The relationship of tamoxifen with dementia, depression, and
dependence in activities of daily living in elderly nursing home residents. Women Health
2000;31(1):71-85.
56. Paganini-Hill A, Clark LJ. Preliminary assessment of cognitive function in breast can-
cer patients treated with tamoxifen. Breast Cancer Res Treat 2000;64(2):165-76.
57. Van Dam FS, Schagen SB, Muller MJ et al. Impairment of cognitive function in
women receiving adjuvant treatment for high-risk breast cancer: high-dose versus stan-
dard-dose chemotherapy. J Natl Cancer Inst 1998;4,90(3):210-8.
58. Garcia-Segura LM, Wozniak A, Azcoitia I et al. Aromatase expression by astrocytes
after brain injury: implications for local estrogen formation in brain repair. Neuroscience
1999;89(2):567-78.
59. Winer EP, Hudis C, Burstein HJ et al. American Society of Clinical Oncology techno-
logy assessment on the use of aromatase inhibitors as adjuvant therapy for postmenopau-
sal women with hormone receptor-positive breast cancer: status report 2004. J Clin
Oncol 2005;23(3):619-29.
60. Howell A, Cuzick J. Vascular effects of aromatase inhibitors: data from clinical trials.
J Steroid Biochem Mol Biol 2005;95(1-5):143-9.
61. Weinfurt K, Wait SL, Boyko W, Schulman KA.Psycosocial quality of life in a phase III
trial of letrozole (abstract 417). Proc Asco 1998;17:108a.
62. Shilling V, Jenkins V, Fallowfield L et al. The effects of hormone therapy on
cognition in breast cancer. J Steroid Biochem Mol Biol 2003;86(3-5):405-12.
1
/
5
100%