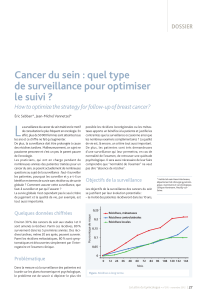
Facteurs pronostiques et résultats du traitement

39
La Lettre du Gynécologue - n° 313 - juin 2006
es récidives locales (RL) de cancer du col représen-
tent la majorité des causes de décès (59 %) et sur-
viennent pour plus de 80 % dans les 2 ans après le
traitement initial. Seulement 15% environ seront accessibles à
une résection chirurgicale à visée curative. Les survies à 5 ans
se situent entre 3 et 40%. Le but de cette étude a été d’évaluer
les résultats de 74 résections à visée curative de RL entre 1980
et 2004.
MATÉRIEL
Nous avons analysé de manière rétrospective toutes les
patientes présentant une récidive pelvienne isolée de cancer du
col utérin traité initialement par chirurgie et/ou curiethérapie
et/ou radiothérapie ou radio-chimiothérapie concomitante. Le
diagnostic de récidive a été porté sur les données cliniques,
échographiques, de tomodensitométries, des marqueurs tumo-
raux ou de biopsie. Toutes les patientes ont été explorées par
un examen clinique sous anesthésie générale associé à des
échographies par voie endovaginale et endorectale avec une
cystoscopie. La taille de la récidive et sa localisation ont été
précisées sur les données cliniques, échographiques et de
tomodensitométrie ou IRM pelvienne. Le bilan d’extension a
comporté une tomodensitométrie thoraco-abdomino-pelvienne
et une scintigraphie osseuse. Dans la dernière période,
quelques patientes ont également bénéficié d’un examen PET-
TDM. Seules les patientes ayant subi une exérèse à visée cura-
tive sur les constatations peropératoires ont été incluses. Ont
été exclues les patientes présentant une métastase viscérale ou
osseuse, une carcinose péritonéale, une tumeur jugée non résé-
cable en peropératoire ou une indication de chirurgie pelvienne
de sauvetage pour complication locale.
Les taux de mortalité et de morbidité ont été évalués sur la
période des 90 jours postopératoires. Les calculs de survie glo-
bale et sans récidive ont été réalisés à partir de la date de chi-
rurgie pour la récidive.
POPULATION
L’âge médian était de 51 ans (23-76). La majorité des tumeurs
était de type épidermoïde (78%) et dans 20% des cas, un adé-
nocarcinome. Le stade initial n’était pas précisé dans 19% des
cas (14 fois), correspondait à un stade limité (Tis-IIA) dans
47% des cas et à un stade avancé dans 34% des cas (IB2, IIA
supérieur à 4 cm, IIB, III et IVA) (tableau I).
Le traitement initial avait comporté une radiothérapie exclu-
sive dans 15 % des cas (11 fois), une chirurgie exclusive dans
11 % des cas (8 fois), et la combinaison des deux dans 74 %
des cas (55 fois). Le délai d’apparition des RL était de 15,5 mois
(5-195), dans 35 % des cas avec un délai inférieur ou égal à
12 mois, dans 29 % des cas avec un délai de 12 à 24 mois,
dans 16% des cas avec un délai de 24 à 60 mois et dans 20%
des cas avec un délai de plus de 60 mois. Le diagnostic a été
porté dans 64% des cas du fait de l’apparition de symptômes
cliniques : douleur pelvienne, saignements, œdème des
membres inférieurs, urétéro-hydronéphrose. Dans 27 % des
cas, la récidive était asymptomatique et a été diagnostiquée
devant une augmentation du marqueur tumoral SCC ou ACE,
ou sur un examen systématique de surveillance (échographie
ou tomodensitométrie). Une confirmation anatomopatholo-
gique de la récidive a été obtenue dans 64,9 % des cas (48 fois) ;
chez 8 patientes la biopsie était négative (8/56 : 14,3 %) et
chez 18 patientes il n’a pas été possible d’obtenir une confir-
mation par biopsie du diagnostic de récidive (18/74 : 24,3%).
La localisation des récidives était centropelvienne dans 45%
Facteurs pronostiques et résultats du traitement
chirurgical à visée curative des récidives de cancer du col
●G. Houvenaeghel*, E. Grégoire*, M.Buttarelli*, L. Lelièvre*, J. Jacquemier**, L. Gonzague-Casabianca*
Pronostic factors and results of surgical resection with curative intent
for locoregional recurrence of cervical cancer
* Service de chirurgie oncologique. ** Services d’anatomopathologie et de
radiothérapie, Institut Paoli-Calmettes, 232, bd Sainte-Marguerite, 13273
Marseille Cedex.
L
DOSSIER
Caractéristiques des patientes n %
Âge médian (extrêmes) 51 (23-76)
Type histologique
épidermoïde 58 78,4
adénocarcinome 14 18,9
carcinome adénosquameux 2 2,7
Stade initial au diagnostic
Tis 1 1,4
I 26 35,1
IIA 8 10,8
IIB 14 18,9
IIIA 3 4,1
IIIB 4 5,4
IVA 4 5,4
TX 14 18,9
Traitement initial
Radiothérapie 11 14,9
Chirurgie 8 10,8
Chirurgie + radiothérapie 55 74,3
Tableau I. Caractéristiques des patientes.

40
DOSSIER
La Lettre du Gynécologue - n° 313 - juin 2006
des cas (33 fois), panpelvienne dans 38 % des cas (28 fois) et
latéropelvienne 12 fois. L’exérèse a nécessité une exentération
pelvienne (EP) pour la majorité des patientes (82 %) et 30 %
des patientes ont bénéficié d’une irradiation de la RL. L’exé-
rèse a été considérée comme curative dans 66 % des cas (49 fois)
et palliative dans 34 % des cas (25 fois) soit du fait de marges
d’exérèse non saines du point de vue anatomopathologique,
malgré des marges chirurgicales macroscopiquement saines
(22 patientes) soit du fait d’une cytologie péritonéale posi-
tive (3 patientes). Le suivi médian a été de 57 mois (6-212).
RÉSULTATS
La mortalité à 90 jours postopératoire a été de 6,8% (5/74), les
décès étant survenus à la suite de complications médicales et
durant la première période de 1980 à 1990. Le taux de compli-
cations postopératoires immédiates (90 jours) a été de 55 %
(41/74): 39% de complications médicales, 37% de complica-
tions chirurgicales et 24% de complications combinées médi-
cales et chirurgicales. Soixante-dix pour cent des complica-
tions après EP ont été traitées médicalement et 30 % ont
nécessité une réintervention. La durée d’hospitalisation a été
de 29 jours (6-96).
Les survies actuarielles à 2 et 5 ans ont été de 53 et 34%, avec
une médiane de 27 mois (1-164). Les taux de survie à 2 et 5 ans
étaient significativement différents en fonction du caractère cura-
tif ou palliatif de l’exérèse (p < 10-4), respectivement 68 et 44%
versus 18 et 9% (figure 1). Nous avons identifié en étude multi-
variée après résection macroscopiquement saine les facteurs pro-
nostiques suivants : résection microscopique saine, localisation
centropelvienne de la RL, taille de la récidive inférieure à 30 mm
et le délai de survenue de la récidive. L’âge, le stade initial, le type
de chirurgie initiale n’étaient pas significatifs.
Les taux de survie en fonction de la localisation de la récidive
étaient significativement différents (figure 2) (p < 10-4),
sachant que le taux de résection curative était significative-
ment corrélé à la localisation de la récidive. Les survies en
fonction de la taille de la récidive et de sa localisation, deux
facteurs qui sont déterminés en préopératoire, sont rapportées
dans la figure 3, avec des différences de survie très significa-
tives en fonction des groupes. La répartition des groupes à
risque élevé, intermédiaire et faible, ainsi que le caractère
curatif de l’exérèse et les survies à 5 ans, en fonction du délai
de récidive, de la taille et de la localisation est rapportée dans
le tableau II, en comparaison avec l’étude de Shingleton et al.
(1) ayant utilisé les mêmes facteurs pronostiques.
DISCUSSION
Fréquence des récidives locorégionales
Les récidives locorégionales des cancers du col utérin s’obser-
vent dans 6 à 50% des cas, en fonction des séries, du stade ini-
tial et des traitements réalisés. Après traitement de radiothéra-
pie exclusive, ces taux ont été de 75 à 80 % pour les stades
IVA, de 22 à 40% pour les stades IIIB, de 20 à 30% pour les
stades IIB, de 23 à 40 % pour les stades IB2 ou IIA de gros
volume (2, 3). Les progrès thérapeutiques ont cependant per-
mis de diminuer le taux d’échecs pelviens, en particulier pour
les stades localement avancés, grâce à la radio-chimiothérapie
en comparaison avec la radiothérapie sans chimiothérapie
concomitante : 19 % (versus 20 %) avec un suivi médian de
35 mois (4), 24,9% (versus 30,4%) avec un suivi médian des
patientes vivantes de 8,7 ans (5), 17% (versus 34,9%) avec un
suivi médian des patientes vivantes de 6,6 ans (6) et 8,7 %
% cas par groupe (nb) % cas curatif (nb) Survie à 5 ans
IPC Shingleton IPC Shingleton IPC Shingleton
Risque % 12,2 23,3 100 87 58,3 82
faible (9) (31) (9/9) (27/31)
Risque % 79,7 72,2 61 83,3 31,6 46
intermé- (59) (96) (36/59) (80/96)
diaire
Risque % 8,1 4,5 66,7 66,7 44 0
élevé (6) (6) (4/6) (4/6)
Risque faible : délai > 1 an et récidive < 3 cm et récidive centropelvienne ou sans
fixation. Risque élevé : délai < 1 an et récidive > 3 cm et récidive fixée ou avec
une extension latéropelvienne. Risque intermédiaire : autres combinaisons.
Tableau II. Résultats des résections des récidives locorégionales de can-
cer du col en fonction des principaux facteurs pronostiques.
Figure 1.
Figure 2.

41
La Lettre du Gynécologue - n° 313 - juin 2006
DOSSIER
(versus 20,9%) avec un suivi médian de 36 mois de patientes
de stade IB avec une hystérectomie en fin de traitement (7).
Dans notre expérience de radio-chimiothérapie concomitante
et de résection chirurgicale pour des cancers localement avancés
(stades IVA, III, IIB, IIA de gros volume et IB2), ces taux ont été
de 5,9% (6/102) et respectivement de 7,1% (1/14), 5,3% (1/19),
8,7% (4/46) et 0% (0/23) pour les stades IVA, III, IIB et IB2.
Les récidives locorégionales des cancers du col à un stade de
début traités par curiethérapie utérovaginale et résection chirurgi-
cale sont survenues dans 3,1% des cas (6/192) de manière isolée
et trois fois associées à une évolution métastatique avec un taux
global de 4,6% (9/192) (8). Ces taux de récidive étaient de 0%
(0/28) pour les stades IA2, de 3,5% (5/144) pour les stades IB1
(2 récidives centropelviennes et 3 récidives ganglionnaires
iliaques), de 5 % (1 récidive latéropelvienne sur 20) pour les
stades IIA.
Les récidives locorégionales des cancers du col utérin survien-
nent pour les deux tiers dans les deux ans après la fin du traite-
ment initial et dans 90% des cas dans les trois ans.
Diagnostic et bilan des récidives locorégionales
Mode de diagnostic. Les récidives locorégionales sont le plus
souvent diagnostiquées devant l’apparition de symptômes cli-
niques (87%) (9) : saignements, œdème ou phlébite ou throm-
bose veineuse des membres inférieurs, douleur pelvienne, urétéro-
hydronéphrose. Les examens cliniques et paracliniques
systématiques (IRM ou TDM et marqueurs tumoraux) permet-
tent de détecter des récidives asymptomatiques. La confirmation
histologique de la récidive n’est pas obtenue dans tous les cas
(environ 70%), du fait de biopsies parfois négatives ou non réali-
sables. La réalisation d’une tomographie à émission de positons
(TEP) couplée à des images de tomodensitométrie permet de dia-
gnostiquer une récidive asymptomatique avec une bonne sensibi-
lité (80 à 90%) et une spécificité de 76% (10).
Bilan d’extension à distance. L’objectif de ce bilan est de pré-
ciser les récidives pelviennes isolées, sans métastases : 55 %
des récidives pelviennes rapportées par Eifel et al. (6). Ce bilan
comporte habituellement une tomodensitométrie abdominopel-
vienne et thoracique ainsi qu’une scintigraphie osseuse. La
réalisation d’une TEP permet également de détecter des locali-
sations métastatiques avec une bonne sensibilité et de modifier
la stratégie thérapeutique une fois sur deux (11). Bien sûr, la
présence d’une adénopathie sus-claviculaire doit faire l’objet
d’une confirmation histologique de son envahissement, et pour
certains une biopsie systématique pré-scalénique pour les réci-
dives de cancer du col est envisagée.
Bilan locorégional. A priori, son objectif est de déterminer la
résécabilité de la récidive et l’importance de l’exérèse en fonc-
tion de l’extension locale. Un examen sous anesthésie générale
apparaît indispensable et pourra être complété dans le même
temps par des échographies endocavitaires qui permettent
d’apprécier de manière fiable l’extension aux organes adja-
cents et aux cloisons, ainsi que la taille de la récidive dans les
trois axes (12). L’IRM pelvienne reste pour la plupart l’exa-
men de référence.
Stratégie thérapeutique en fonction des traitements initiaux
La réalisation d’une curiethérapie, d’une radiothérapie éven-
tuellement combinée à une chimiothérapie, d’une exérèse
chirurgicale lors du traitement initial conditionne la stratégie
thérapeutique qui peut être envisagée. Lorsqu’une irradiation
exclusive éventuellement associée à une chimiothérapie a
été réalisée initialement, la seule thérapeutique à visée cura-
tive réalisable est une exérèse chirurgicale. Une réirradiation
est, en effet, rarement possible du fait du risque très élevé de
complications. En cas de curiethérapie et/ou d’exérèse chi-
rurgicale initiale, une radiothérapie ou radio-chimiothérapie
doit être envisagée et discutée avant la proposition de résec-
tion chirurgicale.
Type d’exérèse et indications
La résection chirurgicale des récidives des cancers du col
nécessite le plus souvent une exentération pelvienne. Le pre-
mier temps opératoire comporte une exploration abdominale
complète qui peut aboutir à une contre-indication d’exérèse, en
particulier s’il existe une carcinose. Les taux d’une telle
contre-indication peropératoire à une exentération pelvienne
vont jusqu’à 40, voire 63 % (9), sachant qu’avec les progrès
actuels de l’imagerie, ces taux sont maintenant plus faibles. Le
type d’exentération pelvienne se définit, d’une part, par l’exé-
rèse viscérale nécessaire, avec les exentérations antérieures,
postérieures et totales, comportant systématiquement une cel-
lulectomie jusqu’aux parois pelviennes et, d’autre part, par
l’exérèse en hauteur comportant une colpectomie partielle ou
totale et l’exérèse ou la conservation du plancher des releveurs
de l’anus (type I ou II) (9). Une exentération de type III com-
portant une exérèse vulvovaginale et périnéale postérieure est
plus rarement nécessaire dans ces indications.
Une résection plus conservatrice (colpectomie, colpo-hystérec-
tomie, résection latéropelvienne unilatérale) est plus rarement
possible.
L’extension latéropelvienne de ces récidives, uni- ou bilaté-
rale, représente un facteur limitatif majeur des possibilités de
résection en marges saines (R0), en particulier lorsqu’il existe
une fixation latérale clinique de la récidive. C’est dans ces cas que
Figure 3.

43
La Lettre du Gynécologue - n° 313 - juin 2006
DOSSIER
la résection pourra être considérée comme insuffisante du fait des
constatations peropératoires (R2), ou du fait de marges insuffi-
santes sur les résultats anatomopathologiques définitifs (R1). Un
élargissement de l’exérèse peut être envisagé et prévu, pour ces
récidives avec extension latéropelvienne, nécessitant une dissec-
tion des racines sacrées, une résection musculo-aponévrotique
latéropelvienne et parfois une résection vasculaire. La réalisation
d’un pontage vasculaire s’impose en cas de résection artérielle, ce
qui est exceptionnel, et en cas de résection veineuse lorsqu’il
n’existe pas de thrombose au préalable. L’amélioration du
contrôle local peut être obtenu en complétant l’exérèse par une
radiothérapie per opératoire ou par une curiethérapie à haut ou bas
débit de dose, soit en peropératoire, soit en postopératoire précoce
à travers les guides vecteurs laissés en place (13-16). Il est cepen-
dant reconnu que l’importance du résidu, macroscopique (R2) ou
microscopique (R1), a un impact majeur sur les possibilités de
contrôle local de la maladie et sur la survie (13). De ce fait, la pré-
sence d’une symptomatologie de sciatalgie, de thrombose vei-
neuse iliaque par un envahissement latéral avec un œdème du
membre inférieur, représente une contre-indication classique à ce
type d’exérèse à visée curative, d’autant plus que ces symptômes
sont associés. Les taux de résécabilité et de résections curatives
(R0) sont donc étroitement liés aux indications et contre-indica-
tions retenues par les différentes équipes : 10 à 20% de taux de
résection pour Hogan et al. (17), 34% de résection non in sano
dans notre expérience où les seules contre-indications absolues
ont été la présence d’une carcinose et/ou de métastases.
Les indications doivent également tenir compte du bilan géné-
ral d’opérabilité et de l’acceptation de ce type de chirurgie
avec ses conséquences fonctionnelles et psychosociales.
La réalisation d’exentération palliative, en cas de fistule(s), de
nécrose tumorale souvent purulente, d’hémorragie, garde
quelques indications qui doivent être discutées au cas par cas,
avec pour objectif principal l’amélioration du confort de survie.
Les progrès des techniques chirurgicales et particulièrement de
la prise en charge de l’anesthésie-réanimation ont permis de
diminuer les taux de mortalité opératoire des exentérations pel-
viennes de 18 à 25% dans les séries les plus anciennes à moins
de 10%, et moins de 5% dans les séries les plus récentes (18,
19-23). Le taux de mortalité dans les 3 mois postopératoires
après chirurgie d’exérèse à visée curative de récidives de can-
cer du col utérin a été dans notre expérience de 6,8% (5/74),
dans tout les cas à la suite de complications médicales et dans
la première période d’expérience avant 1990.
La morbidité postopératoire reste cependant très élevée après
exentération pelvienne de 38 à 65 % (18, 19, 21-25). Dans
notre expérience, la morbidité, toutes complications observées
après exentération pour cancer du col utérin, a été de 50 %
(57/113), en observant une diminution significative au cours
de la dernière période : 38 % (8/21) de 1996 à 2000 et 52 à
56% au cours des périodes de 5 ans de 1980 à 95 (49/102). La
morbidité a été de 55 % après exentération pour récidive de
cancer du col avec un taux de 30 % de réinterventions. Les
taux de morbidité chirurgicale majeure ont été de 38% (26), 43%
(27), 58% (28) et 33% (22) avec des taux respectifs de réinter-
vention de 33, 40, 36 et 22%. Cependant, le taux de morbidité
varie en fonction du type d’exentération pelvienne, des procé-
dures de reconstruction utilisées et de la localisation de la réci-
dive (23) (45,6% de complications pour les récidives centro-
pelviennes et latéropelviennes, 21/46 versus 71,4 % pour les
récidives panpelviennes, 20/28 dans notre expérience).
Les résultats en termes de survie après résection chirurgicale des
cancers du col utérin sont étroitement liés à la sélection des
patientes et donc aux principaux facteurs pronostiques. La possi-
bilité de réaliser une résection curative (R0) apparaît être le fac-
teur déterminant (1, 16, 20) : une résection R0 sera d’autant plus
fréquemment obtenue que la récidive reste localisée en centropel-
vien par rapport aux récidives latéro- et panpelviennes (respecti-
vement 97, 58 et 32% dans notre expérience : p < 0,0001) (1, 20,
21, 29). La taille de la récidive est également un facteur significa-
tif important (1, 21, 30, 31) qui est cependant fréquemment cor-
rélé à la localisation de la RLR, les récidives latéro- et panpel-
viennes étant plus volumineuses : les tailles moyennes des
récidives étaient de 38,7 mm en centropelvien, 45,3 mm en latéro-
pelvien et 57,8 mm pour les récidives panpelviennes. Les autres
facteurs pronostiques le plus souvent retrouvés dans les séries de
la littérature sont : le délai de récidive (1, 21, 30), l’âge et le stade
initial (29, 30). Les principaux facteurs pronostiques (localisation,
taille et délai de la RLR) peuvent être déterminés en préthérapeu-
tique, permettant de prévoir les chances de résection curative et de
survie (1, 30) (tableau II). Dans notre expérience, la taille et la
localisation, sans tenir compte du délai, étaient plus discrimi-
nantes (figure 1). Les survies à 5 ans sont donc étroitement liées à
ces facteurs, avec des taux de 24 à 55% pour des récidives vagi-
nales ou essentiellement vaginales (26, 28, 29), 22 à 60% pour
des récidives centropelviennes (20, 21, 27, 29) et 0 à 10% pour
des récidives latéro- ou panpelviennes (1, 20). Cependant, des
exérèses latérales élargies (14, 22, 32, 33) et éventuellement asso-
ciées à une réirradiation focalisée, ou à une irradiation peropéra-
toire, ou à une curiethérapie peropératoire (13-15), sont suscep-
tibles d’améliorer le contrôle local et la survie, avec des résultats
encourageants qui ont pu atteindre, dans ces situations, des taux
de 41% de contrôle local et de 44% de survie à 5 ans (22).
CONCLUSION
Les progrès de l’anesthésie-réanimation et des techniques chi-
rurgicales, c’est-à-dire de reconstruction, ont permis de réduire
les taux de mortalité et de morbidité après 1990. L’utilisation
de radiothérapie complémentaire ou curiethérapie per- ou post-
opératoire précoce permet d’améliorer le contrôle local, en
particulier en cas de résection sans marge pour les récidives
avec une extension latéropelvienne. Une meilleure sélection
des patientes à opérer peut être envisagée en ayant recours à
une cœlioscopie et/ou à une TEP-FDG. ■
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Shingleton HM, Soong SJ, Gelder MS et al. Clinical and histopathologic factors
predicting recurrence and survival after pelvic exenteration for cancer of the cervix.
Obstet Gynecol 1989;73:1027-34.
2. Resbeut M, Fondrinier E, Fervers B et al. Standards, options and recommenda-
tions for the management of invasive cervical cancer patients (non metastastic). Bull
Cancer 2003;90,4:333-46.
3. Logsdon MD, Eifel PJ. Figo IIIB squamous cell carcinoma of the cervix: an analy-

45
DOSSIER
sis of prognostic factors emphasizing the balance between external beam and intra-
cavitary radiation therapy. Int J Radiat Oncol Biol Phys 1999;43,4: 763-75.
4. Rose PG, Bundy BN, Watkins EB et al. Concurrent cisplatin-based radiotherapy
and chemotherapy for locally advanced cervical cancer. N Engl I Med
1999;340:1144-53.
5. Withney CW, Sause W, Bundy BN et al. Randomized comparison of fluorouracil plus
cisplatin versus hydroxyurea as an adjunct to radiation therapy in stage IIB-IVA carci-
noma of the cervix with negative para-aortic lymph nodes: a Gynecologic Oncology
Group and Southwest Oncology Group study. J Clin Oncol 1999;17:1339-48.
6. Eifel PJ, Winter K, Morris M et al. Pelvic irradiation with concurrent chemothe-
rapy versus pelvic and para-aortic irradiation for high-risk cervical cancer: an
update of radiation therapy oncology group trial (RTOG) 90-01. J Clin Oncol
2004;22,5:872-80.
7. Keys HM, Bundy B, Stehman FB et al. Weekly cisplatin chemotherapy during irra-
diation improves survival and reduces relapses for patients with bulky stage IB cervi-
cal cancer treated with irradiation and adjuvant hysterectomy: results of a randomi-
zed gynecologic oncology group trial. N Engl J Med 1999;340: 1154-61.
8. Resbeut MR, Alzieu C, Gonzague-Casabianca L et al. Combined brachytherapy
and surgery for early carcinoma of the uterine cervix: analysis of extent of surgery on
outcome. Int Journal Radiat Oncol Biol Phys 2001;50,4:873-81.
9. Selman AE, Copeland LJ. Surgical management of recurrent cervical cancer.
Yonsei Med J 2002;43,6:754-62.
10. Unger JBIJJ, Connor P, Charrier A et al. Detection of recurrent cervical cancer
by whole-body FDG PET scan in asymptomatic and symptomatic women. Gynecol
Oncol 2004;94,1:212-6.
11. Lai CH, Huang KG, See LC et al. Restaging of recurrent cervical carcinoma with
dual-phase [18F] fluoro-2-deoxy-D-glucose positron emission tomography. Cancer
2004;100,3:544-52.
12. Houvenaeghel G, Martino M, Resbeut M et al. Pelvic staging of advanced and
recurrent gynecologic cancers: contribution of endosonography. Gynecol Oncol
1994;55:393-400.
13. Garton GR, Gunderson LL, Webb MJ. Intraoperative radiation therapy in gyne-
cologic cancer: the Mayo Clinic experience. Gynecol Oncol 1993;48:328-32.
14. Höckel M, Schlenger K, Hamm H et al. Five-year experience with combined ope-
rative and radiotherapeutic treatment of recurrent gynecologic tumors infiltrating the
pelvic wall. Cancer 1996;77,9:1918-33.
15. Hannoun-Levi JM, Cowen D, Houvenaeghel G et al. Preliminary results of a
phase I/II study of post-operative high-dose rate brachytherapy for advanced or
recurrent pelvic tumours. Eur J Surg Oncol 1997;23:532-7.
16. Beitler J, Anderson PS, Wadler S et al. Pelvic exenteration for cervix cancer:
would additional intraoperative interstitial brachytherapy improve survival? Int. J.
Radiat Oncol Biol Phys 1997;38:143-8.
17. Hogan WM, Boente MP. The role of surgery in the management of recurrent
gynecologic cancer. Seminars in Oncology 1993;20,5:462-72.
18. Crowe PJ, Temple WJ, Lopez MJ et al. Pelvic exenteration for advanced pelvic
malignancy. Semin Surg Oncol 1999;17,3:152-60.
19. Bladou F, Houvenaeghel G, Delpero JR et al. Incidence and management of
major urinary complications after pelvic exenteration for gynecological malignan-
cies. J Surg Oncol 1995;58:91-6.
20. Moutardier V, Houvenaeghel G, Martino M et al. Surgical resection of locally
recurrent cervical cancer: a single institutional 70 patient series. Int J Gynecol
Cancer 2004;14,5:846-51.
21. Morley G, Hokins M, Lindenauer S et al. Pelvic exenteration, 100 patients at
5 years. Obstet Gynecol 1989;74:934-42.
22. Höckel M. Laterally extended endopelvic resection. Novel surgical treatment of
locally recurrent cervical carcinoma involving the pelvic side Gyn Oncol
2003;91:369-77.
23. Soper JT, Berchuck A, Creasman WT et al. Pelvic exenteration: factors associa-
ted with major surgical morbidity. Gynecol Oncol 1989;35:93-8.
24. Anthropoulos AP, Manetta A, Larson JE et al. Pelvic exenteration : a morbidity
and mortality analysis of a seven-year experience. Gynecol Oncol 1989;35: 219-23.
25. Jakowatz JG, Porudominsky D, Riihimaki DU et al. Complications of pelvic
exenteration. Arch Surg 1985;120:1261-5.
26. Rutledge S, Carey MS, Prichard H et al. Conservative surgery for recurrent or
persistent carcinoma of the cervix following irradiation: is exenteration always
necessary? Gynecol Oncol 1994;52:353-9.
27. Ibsen TB, Sorensen BL, Knudsen JB et al. Operative treatment of recurrent
cancer of the uterine cervix after radiotherapy. Acta Obstet Gynecol Scand
1988;67:389-93.
28. Coleman RL, Keeney ED, Freedman RS et al. Radical hysterectomy for recurrent
carcinoma of the uterine cervix after radiotherapy. Gynecol Oncol 1994;55:29-35.
29. Wang CJ, Lai CH, Huang HJ et al. Recurrent cervical carcinoma after primary
radical surgery. Am J Obstet Gynecol 1999;181:518-24.
30. Martino M, Houvenaeghel G, Hardwigsen J et al. Pelvic recurrence of cancers of
the uterine cervix. A study of a series of 49 cases. Ann Chir 1997;51,1: 36-45.
31. Virostek LJ, Kim RY, Spencer SA. Postsurgical recurrent carcinoma of the cervix:
reassessment and results of radiation therapy options. Radiology 1996; 201,2:559-63.
32. Hockel M, Baussmann E, Mitze M et al. Are pelvic side-wall recurrences of cervi-
cal cancer biologically different from central relapses? Cancer 1994;74,2: 648-55.
33. Hockel M. Laterally extended endopelvic resection: surgical treatment of infrai-
liac pelvic wall recurrences of gynecologic malignancies. Am J Obstet Gynecol
1999;180,2:306-12.
La Lettre du Gynécologue - n° 313 - juin 2006
La Lettre du Gynécologue
vous souhaite un bel été et vous remercie
de la fidélité de votre engagement
1
/
5
100%