SELECTIVITE EN CHIMIE ORGANIQUE

SELECTIVITE EN CHIMIE ORGANIQUE
1. REACTIF CHIMIOSELECTIF ET REACTION SELECTIVE
Une espèce polyfonctionnelle appartient à plusieurs classes fonctionnelles ou possède plusieurs groupes caractéristiques identiques.
Un réactif chimiosélectif est un réactif qui transforme un ou plusieurs groupes caractéristiques (et éventuellement les doubles liaisons
carbone-carbone C=C) d’une espèce polyfonctionnelle sans modifier les autres.
Lors d’une réaction sélective, une espèce polyfonctionnelle réagit avec un réactif chimiosélectif.
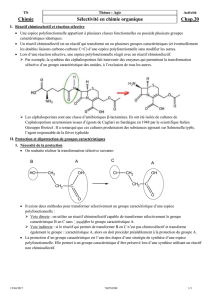
Les céphalosporines sont une classe d’antibiotiques ß-lactamines. Ils ont été isolées de cultures de Cephalosporium acremonium
issues d’égouts de Cagliari en Sardaigne en 1948 par le scientifique Italien Giuseppe Brotzu1. Il a remarqué que ces cultures produi-
saient des substances agissant sur Salmonella typhi, l’agent responsable de la fièvre typhoïde
Par exemple, la synthèse des céphalosporines fait intervenir des enzymes qui permettnt la transformation sélective d’un groupe
caractéristique des amides, à l’exclusion de tous les autres.
2. PROTECTION ET DEPROTECTION DE GROUPES CARACTERISTIQUES
2.1. NECESSITE DE LA PROTECTION
On souhaite réaliser la transformation sélective suivante:
Il existe deux méthodes pour transformer sélectivement un groupe caractéristique d’une espèce polyfonctionnelle:
voie directe: on utilise un réactif chimioselectif capable de transformer sélectivement le groupe caractéristique B en C sans
modifier le groupe caractéristique A;
voie indirecte: si le réactif qui permet de transformer B en C n’est pas chimioselectif et transforme également le groupe
caractéristique A, alors on doit procéder préalablement à la protection du groupe A.
La protection d’un groupe caractéristique est l’une des étapes d’une stratégie de synthèse d’une espèce polyfonctionnelle. Elle permet
à un groupe caractéristique d’être préservé lors d’une synthèse utilisant un réactif non chimiosélectif.
2.2. STRATEGIE EN TROIS ETAPES.
Pour obtenir la produit attendu, on doit d’abord effectuer la protection du groupe caractéristique A. Cette voie indirecte se fait en trois
étapes:
Protection du groupe A
Un réactif chimiosélectif noté P transforme sélectivement le groupe A. Le nouveau groupe A-P est appelé groupe protégé, il
s’agit d’un groupe d’atomes qui peuvent contenir plusieurs groupes caractéristiques.

Transformation du groupe B en groupe C
Le nouveau groupe A-P est inerte vis-à-vis de SOCl2, alors que le groupe caractéristique A ne l’est pas.
Déprotection du groupe A-P.
Pour obtenir le groupe attendu, porteur des groupes caractéristiques C et A, il faut déprotéger le groupe A-P en utilisant un
réactif chimiosélectif ne modifiant pas le groupe C. Le groupe A se retrouve à la fin des trois étapes.
Remarques, cette stratégie permet de contourner le problème de la non-chimiosélectivité d’un réactif vis-à-vis de deux groupes
caractéristiques. Cependant pour qu’elle soit efficace:
chacune des étapes doit se faire avec un bon rendement;
chacune des étapes doit être sélective.
Cette stratégie présente des inconvénients:
le rendement global de la synthèse est en général plus petit que l’on utilise des réactifs chimiosélectifs;
un grand nombre d’atomes n’apparaissant pas dans le produit final doivent être utilisés, ce qui est contraire aux principes
de la chimie durable.
La liaison qui se forme est appelée liaison peptidique et il apparaît le groupe caractéristique des amides.
3.2. SYNTHESE PEPTIDIQUE DE ALA-GLY.
Or chaque acide aminé possède un groupe amino et un groupe carboxyle. La réaction entre deux acides aminés conduit donc à la
formation de quatre dipeptides distincts. Pour obtenir le dipeptide souhaité, il faut qu’un seul groupe amino (de l’acide aminé 1)
réagisse avec un seul groupe carboxyle (de l’acide aminé 2). Les deux autres groupes (carboxyle de l’acide aminé 1 et amino de
l’acide aminé 2) doivent être au préalable protégés.
3. EXEMPLE: SYNTHESE D’UN DIPEPTIDE
3.1. ACIDES -AMINES ET LIAISON PEPTIDIQUE
Les acides aminés possèdent à la fois la fonction acide carboxylique -COOH et la fonction
amine - NH2.
On distingue les acides aminés, où la fonction acide carboxylique -COOH et la fonction
amine - NH2 sont portées par le même carbone:
Deux acides aminés peuvent réagir entre eux: le groupe carboxyle - COOH d’un acide aminé 1 va former une liaison ave le groupe
amino -NH2 d’un acide aminé 2, schématisé par:

Il faut donc:
protéger le groupe amino d’un acide aminé et protéger le groupe carboxyle de l’autre acide aminé;
effectuer le couplage entre les groupes amino et carboxyle non protégés;
déprotéger le groupe amino et le groupe carboxyle protégés lors de la première étape.
Prenons le cas concret de la synthèse du dipeptide Ala - Gly à partir de l’alanine et de la glycine
Or trois autres dipeptides non souhaités peuvent se former:
La solution est la protection des fonctions
Remarque: Qu’est ce qu’un bon groupe protecteur ?
Réagit de manière sélective avec la fonction à protéger;
Doit être stable lors des réactions suivantes;
Doit pouvoir être clivé facilement et de manière sélective;
Les étapes de protection et de déprotection doivent avoir lieu avec de très bons rendements

Exemple. Le Dipeptiven est utilisé en milieu hospitalier lors d’une nutrition parentérale(1) pour des parents en réanimation.
Les étapes permettant de synthétiser ce dipeptide sont représentées
(1) La nutrition parentérale est le fait de suppléer artificiellement à l'alimentation d'un patient par voie intraveineuse en évitant ainsi
le circuit habituel de l'alimentation et de la digestion. Lorsque la voie entérale(2) n'est pas utilisée de manière concommitante, on
parle alors de "nutrition parentérale totale" (TPN). Les solutions contiennent généralement du glucose, des acides aminés, des
minéraux et des lipides. En fonction des besoins, il peut être additionné des vitamines, des électrolytes et des oligo-éléments. Il
existe des solutions prêtes à l'emploi fournies par l'industrie pharmaceutique, mais il arrive souvent que des mélanges spécifiques
aux besoins du patient soient préparés et ce, notamment, pour les enfants et les supplémentations à long terme.
(2) Quand l’alimentation par la bouche (voie orale) est impossible ou insuffisante, le médecin peut proposer une nutrition entérale.
La nutrition entérale est une technique d'alimentation artificielle, qui permet d’administrer l’alimentation sans passer par la bouche.
Elle est mise en place dans le but de pallier une fonction orale défectueuse et/ou de maintenir un apport alimentaire suffisant pour
le patient.
La synthèse de ALA-GLY se fait selon le mécanisme suivant:

Remarques.
Les groupes d’atomes R1 et R1 des acides -aminés peuvent aussi posséder des groupes caractéristiques, qu’il faut alors
également protéger.
En 1951 on réalise la synthèse d’une hormone, l’insuline, constitué de 51 acides -aminés.
La méthode présentée ici est en fait peu utilisable pour la synthèse des protéines car le nombre d’étapes est trop élevé. On
privilégie aujourd’hui des synthèses enzymatiques hautement sélectives.
Elle permet donc de lutter contre la dénutrition et la déshydratation du patient à la foi de manière préventive mais aussi curative.
Elle apporte à l'organisme les macronutriments (protéines, lipides et glucides) et micronutriments (vitamines et minéraux) dont il a
besoin, directement dans l'estomac ou l'intestin par le biais d’une sonde.
Cette forme d'alimentation préserve les fonctions du tube digestif et des organes associés (foie, pancréas et vésicule biliaire),
contrairement à la nutrition par perfusion.
Le but de la nutrition entérale est d’aider le malade à mieux récupérer grâce à un apport de nutriments adaptés et de pouvoir envisa-
ger un retour à une alimentation normale quand cela est possible. Dans certains cas, le patient peut continuer à s’alimenter par la
bouche tout en ayant une nutrition entérale en place, ce qui permet de garder le plaisir des repas.
1
/
5
100%