DETECTION ET CARACTERISATION DES THROMBI DU VG PAR IRM O.FAVELLE (1), P.OMOUMI(1),

DETECTION ET
CARACTERISATION DES THROMBI
DU VG PAR IRM
O.FAVELLE (1), P.OMOUMI(1),
O GENEE(2), M.COUCHOT(1), D.ALISON(1).
(1) Pôle Imagerie
(2) Pôle Thorax Vasculaire Hémostase
CHU de Tours
Université François Rabelais de Tours

PLAN
1. GENERALITES
a) Introduction
b) Etiologies
c) Incidence
d) Enjeux diagnostiques
2. INTERET DE L’IRM DANS LA DETECTION ET
CARACTERISATION DU THROMBUS
a) Intérêt de l’IRM par rapport à l’échographie
b) Protocole IRM et intérêt respectif des différentes séquences
IRM
c) caractéristiques sémiologiques du thrombus
3. INTERET DE L’IRM DANS LE DIAGNOSTIC ETIOLOGIQUE DU
THROMBUS
4. DIAGNOSTICS DIFFERENTIELS
5. CONCLUSION

GENERALITES

Introduction
Le THROMBUS du ventricule gauche est une complication
fréquente des infarctus du myocarde et des myocardiopathies
dilatées grevant le pronostic de ces deux affections par un risque
d’embolie systémique.
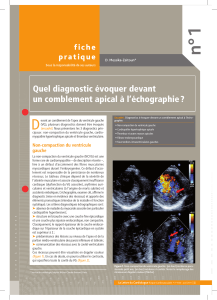
Son dépistage est réalisé en première intention par l’échographie
transthoracique, cependant cette technique présente deux
inconvénients, une trop faible sensibilité et spécificité (en raison
de problèmes inhérents à la technique échographique…),
générant de nombreux faux négatifs et faux positifs, et d’autre part
elle ne permet le plus souvent qu’un diagnostic étiologique limité
de cette thrombose.
Actuellement l’IRM cardiaque s’impose en seconde intention
lorsque les performances diagnostiques de l’échocardiographie
transthoracique sont prises en défaut.

Etiologies
Les thrombi du ventricule gauche se forment la plupart du temps en
regard d’un myocarde akinétique ou dyskinétique.
Les deux principales étiologies par ordre de fréquence sont :
-l’INFARCTUS DU MYOCARDE : surtout en cas d’infarctus antérieur et d’
anévrisme de la paroi ventriculaire.
-les CARDIOMYOPATHIES DILATEES.
-les autre étiologies sont beaucoup plus rares et concernent des
pathologies entrainant des troubles de la cinétique segmentaire du
VG ou des lésions de l’endocarde (non compaction partielle du VG,
fibrose endomyocardique…..)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
1
/
33
100%