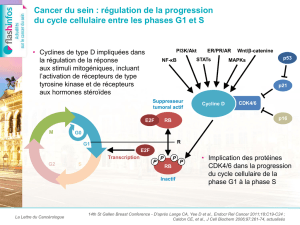
L Leess iinnhhiibbiitteeuurrss ddee ll’’aarroom maattaassee.. É

MISE AU POINT
56
La Lettre du Cancérologue - volume X - n° 2 - mars/avril 2001
es traitements hormonaux représentent un ensemble
d’armes thérapeutiques majeures dans la prise en
charge des cancers du sein, aussi bien à la phase pré-
coce qu’à la phase avancée et/ou métastatique. Les inhibiteurs
de l’aromatase forment une des classes médicamenteuses qui
se sont le plus enrichies ces dernières années. Nous rappelons
ici la base de leurs mécanismes d’action ainsi que les résultats
cliniques les plus récents.
BBAASSEESS MMOOLLÉÉCCUULLAAIIRREESS
La source majeure d’estrogènes chez la femme non méno-
pausée est l’ovaire. Il persiste chez la femme ayant subi une
ablation ovarienne et chez la femme ménopausée une biosyn-
thèse d’estrogènes dite “périphérique”, dans le tissu adipeux,
la peau, le muscle et le tissu tumoral mammaire (1) (figure 1).
La dernière étape de la synthèse des estrogènes est l’aromatisa-
tion, qui convertit les androgènes en estrogènes. L’aromatase
réalise une hydroxylation des androgènes et utilise un cyto-
chrome P450 spécifique responsable du transfert électronique.
Son inhibition peut intervenir soit par compétition avec le sub-
strat au site de liaison (inhibition de type I), soit par interfé-
rence avec le noyau héminique du cytochrome P450 (inhibi-
tion de type II). Les inhibiteurs de type I sont essentiellement
stéroïdiens, parfois “suicidaires” car dégradés par l’enzyme en
métabolites qui se lient de manière irréversible. Les inhibiteurs
de type II sont des composés azolés non stéroïdiens, d’action
réversible et moins spécifique, d’autres hydroxylases des sté-
roïdes contenant des noyaux héminiques. Plusieurs générations
de ces inhibiteurs ont été développées (figure 2) (2).
La mesure de l’activité aromatase est un facteur prédictif
potentiel de l’efficacité des inhibiteurs. Elle peut se faire par
méthode biochimique, en mesurant le taux de conversion
d’androgènes marqués administrés à doses fixées, soit dans le
plasma, soit dans le tissu tumoral (3). Dans ce dernier, d’autres
méthodes (RT-PCR, immuno-histochimie) sont en cours
d’étude (4). Il a été montré sur un échantillon de plus de
1 000 patientes que le niveau d’expression de l’aromatase
mesuré par méthode Taq-Man était indépendant de l’âge, du
statut ménopausique et du niveau d’expression du récepteur
aux estrogènes. Un haut niveau d’expression était par ailleurs
corrélé à un risque accru de rechute (p < 0,05) et de décès
(p < 0,005) (5). La mesure d’activité de l’aromatase peut être
effectuée avant et après l’exposition aux inhibiteurs, ce qui
LLeess iinnhhiibbiitteeuurrss ddee ll’’aarroommaattaassee.. ÉÉttaatt ddeess lliieeuuxx
●P.-H. Cottu*
* Centre des maladies du sein et service d’oncologie médicale, hôpital Saint-
Louis, 1, av. Claude-Vellefaux, 75475 Paris Cedex 10.
L
Figure 2. Inhibiteurs de l’aromatase.
NH2
NO
O
Première génération : aminoglutéthimide
Deuxième génération :
N
on stéroïdien : fadrozole
Troisième génération :
N
on stéroïdiens : anastrozole létrozole Stéroïdien : exemestane
Stéroïdien : formestane
N
N
CN
O
OH
O
CH2
N
N
N
CN
NC
O
O
N
NN
NC CN
Figure 1. Synthèse des estrogènes.
1. P450 scc (side-chain cleavage). 2. 17ß hydroxylase.
3. 3ß hydroxystéroïde déshydrogénase. 4. 17ß hydroxystéroïde déshydrogénase
Cholestérol
Prégnénolone
17-OH-prégnénolone 17-OH-progestérone
DHEA Androstènedione E1
Testostérone E2
A
R
O
M
A
T
A
S
E
1
2
23
344
2

permet d’établir leur puissance relative et leur efficacité in
vitro sur le tissu mammaire et en périphérie (figure 3) (3).
DDÉÉVVEELLOOPPPPEEMMEENNTT CCLLIINNIIQQUUEE
Trois générations d’inhibiteurs de l’aromatase sont distinguées
(figure 2). La première génération est représentée par l’amino-
glutéthimide (Orimétène®), inhibiteur non spécifique de l’aro-
matase et initialement développé comme antiépileptique. La
deuxième génération comprend le formestane (type I, stéroï-
dien, Lentaron®), et le fadrozole (type II, azolé, non commer-
cialisé en France) qui a également des propriétés antiminéralo-
corticoïdes (6). Le formestane est administré par voie
intramusculaire (250 mg tous les 14 jours), ce qui est parfois
utile, mais les résultats cliniques restent décevants (6). La troi-
sième génération comprend le vorozole (non commercialisé en
France), le létrozole (Fémara®) et l’anastrozole (Arimidex®),
inhibiteurs non stéroïdiens de type II, enfin, l’exemestane
(Aromasine®), inhibiteur stéroïdien de type I qualifié d’“inacti-
vateur” de l’aromatase. Nous rapportons ici les principaux
résultats obtenus avec ces trois derniers composés au cours des
essais de phase III.
DDeeuuxxiièèmmee lliiggnnee mmééttaassttaattiiqquuee
Ces trois médicaments ont été comparés en deuxième ligne
métastatique à l’acétate de mégestrol (Mégace®) (7-9). Les
principaux résultats sont présentés dans les tableaux I et II.
Trois types de données sont à analyser et comparer pour cha-
cun de ces essais.
57
La Lettre du Cancérologue - volume X - n° 2 - mars/avril 2001
Figure 3. Démonstration de l’inhibition de l’aromatase périphérique et
intramammaire. Exemple de l’exemestane : pour chaque graphique est
indiquée l’activité aromatase mesurée par métabolisme de l’estrone mar-
quée.
40
35
30
25
20
15
10
5
0
Activité aromatase
Prétraitement
Inhibition périphérique
Inhibition périphérique
Post-traitement
Prétraitement Post-traitement
Activité aromatase
40
35
30
25
20
15
10
5
0
n Indication du RE + RP+ RE+ RH
tamoxifène ou RP+ inconnus
Adjuvant Métastatique
Exemestane 769 39,6 66,4 67 32
Létrozole 551 33 66 35 21 44
Anastrozole 764 42 58 75 25
Tableau Ia. Résultats des études comparant un inhibiteur de l’aroma-
tase de troisième génération à l’acétate de mégestrol après échec du
tamoxifène. Les résultats sont indiqués en pourcentages sauf pour le
temps jusqu’à progression (TTP).
Tableau Ib.
Schéma de l’étude Viscères Cible mesurable
Exemestane équivalence 56,6 78,4
RO, TTP
Létrozole RO, TTP 40 NR
Anastrozole essais poolés 44 71
RO, TTP
Exemestane Létrozole Anastrozole Acétate
de mégestrol
0,5 2,5 1 10
Tous événements 39 78,2 85 NR 45,8-89,9
confondus
Asthénie 7,5 5,9 10,9 18 18 10-20
Bouffées 12,6 5,9 5,7 13 11 3,7-8
de chaleur
Prise 7,6 2,1 2,3 3 4 8,5-17,1
de poids
Nausées 9,2 19,1 10,9 18 22 5-23
Vomissements 2,8 8 7,5 10 12 0,8-5,3
Céphalées NR 13,3 12,6 14 20 9-11
Tableau II. Effets secondaires des inhibiteurs de l’aromatase com-
parés à l’acétate de mégestrol (en pourcentages).
Tableau Ic.
RO : réponse objective. TTP : temps jusqu’à progression. BC : bénéfice
clinique (RO + stabilisation
⭓
24 semaines). AM : acétate de mégestrol.
NR : non rapporté. NS : non significatif.
RO BC TTP (mois)
Exemestane E : 15 E : 37,4 E : 4,5
AM : 12,4 NS AM : 34,6 NS AM : 3,7 p = 0,037
Létrozole 0,5 : 13 0,5 : 27 0,5 : 5,1
p = 0,004 p = 0,02
2,5 : 23,6 p = 0,11 2,5 : 35 NS 2,5 : 5,6 p = 0,8
p = 0,04 p = 0,07
AM : 16,4 AM : 32 AM : 5,5
Anastrozole 1 : 12,6 1 : 42,3 1 : 4,8
10 : 12,5 NS 10 : 39,9 NS 10 : 5,3 NR
AM : 12,2 AM : 40,3 AM : 4,6

MISE AU POINT
58
La Lettre du Cancérologue - volume X - n° 2 - mars/avril 2001
Méthodologie
Les trois essais étaient randomisés, multicentriques, internatio-
naux et en double aveugle ; ils comparaient, après échec du
tamoxifène, à l’acétate de mégestrol, un inhibiteur de l’aroma-
tase, qui était administré soit en situation adjuvante (33 à 42 %
des patientes), soit en situation métastatique (58 à 66 % des
patientes). Ces trois essais avaient pour objectif principal le
taux de réponses objectives (RO) et le temps jusqu’à progres-
sion (TTP). Seul M. Kaufman précise que le but recherché
était de montrer l’équivalence de l’exemestane et de l’acétate
de mégestrol (9). Le taux de patientes avec des récepteurs
inconnus et des métastases viscérales diffère notablement
d’une étude à l’autre. Les études consacrées aux inhibiteurs
non stéroïdiens comprennent également deux dosages, 0,5 et
2,5 mg/jour pour le létrozole (8), 1 et 10 mg/jour pour l’anas-
trozole (7). Enfin, les résultats présentés pour l’anastrozole
proviennent de données poolées de deux études “jumelles”,
États-Unis et Europe-Australie-Afrique du Sud (7).
Résultats
Les trois études démontrent une très discrète tendance à la
supériorité de l’inhibiteur étudié, en particulier en termes de
TTP. Les comparaisons de doses pour le létrozole semblent
montrer une supériorité de 2,5 mg par rapport à 0,5 mg, alors
que 1 mg/j semble équivalent à 10 mg pour l’anastrozole.
L’analyse de la survie globale à 2 ans montre une tendance à la
supériorité pour l’anastrozole (84-85 % versus 70 %).
Effets secondaires
Les principaux effets secondaires observés sont indiqués dans
le tableau II. Aucune différence n’apparaît nettement, ni en
faveur ni en défaveur des inhibiteurs de l’aromatase, à l’excep-
tion de la prise de poids qu’ils entraînent. Les patientes traitées
par exemestane subissaient une prise de poids indésirable de
grade 3-4 dans 7,6 % des cas, versus 17,1 % dans le bras acé-
tate de mégestrol (p = 0,001). Après 8 mois de traitement, le
gain moyen de poids était dans ce bras de 3 kg. Des données
tout à fait similaires sont rapportées pour l’anastrozole (7). Les
auteurs de l’étude létrozole rapportent un nombre plus élevé
d’événements cardiovasculaires dans le bras acétate de méges-
trol (20 % versus 10-11 %, p = 0,02) (8).
IInnhhiibbiitteeuurrss ssttéérrooïïddiieennss eenn rreellaaiiss ddeess iinnhhiibbiitteeuurrss nnoonn ssttéérrooïïddiieennss
Une étude de phase II multicentrique a testé l’efficacité de
l’exemestane à 25 mg/j en relais d’un traitement par inhibiteur
azolé ou par aminoglutéthimide (10). La dose était augmentée
à 100 mg/j lors de la progression sous exemestane. Un taux de
réponses de 6,6 % a été observé chez 241 patientes (8,1 %
après aminoglutéthimide ; 4,8 % après inhibiteur azolé). Cin-
quante-huit patientes ont reçu de l’exemestane à 100 mg, pour
une réponse partielle (1,7 %). Une chute significative de
l’estradiolémie a pu être montrée chez les patientes antérieure-
ment sous aminoglutéthimide. Une stabilisation de la maladie
a été observée pendant, respectivement, 35,9 et 34,3 semaines.
Le TTP moyen était de 14,7 et 8,7 semaines.
PPrreemmiièèrree lliiggnnee mmééttaassttaattiiqquuee
Létrozole
Le létrozole (2,5 mg/j) a été testé comme première ligne d’hor-
monothérapie, comparé au tamoxifène dans un essai de phase
III, randomisé, multicentrique, international et en double
aveugle, plusieurs fois présenté, mais non encore publié inté-
gralement (11). Les principales données figurent sur le
tableau III et semblent indiquer une supériorité du létrozole
sur le tamoxifène. Nous ne disposons pas encore d’informa-
tions sur le détail de la population traitée, ni sur la toxicité, ce
qui rend l’interprétation fine de cette étude encore délicate.
n Tamoxifène adjuvant RE+RP+ RE+ ou RP+ RH inconnus Os Foie Viscères Tissus mous Masse mesurable
Anastrozole 353 40 65 24 11 A : 65 A : 7 A : 48,5 A : 10 A : 68,4
États-Unis T : 53 T : 16 T : 47,8 T : 18 T : 76,9
Anastrozole (Europe) 668 30 25 20 55 A : 45 A : 9,4 A : 30 A : 37 A : 88,5
T : 48 T : 9,5 T : 37 T : 32 T : 87,2
Létrozole 907 19 65 35 L : 32 NR L : 43 NR NR
T : 29 T : 46
Tableau IIIa. Résultats des études comparant un inhibiteur de l’aromatase de troisième génération au tamoxifène. Les résultats sont indiqués en
pourcentages sauf pour le TTP.
Tableau IIIb.
RO BC TTP (mois)
Anastrozole (États-Unis) A : 21 A : 59 A : 11
T : 17 NS T : 46 p = 0,0098 T : 5,6 p = 0,005
Anastrozole (Europe) A : 32,9 A : 56 A : 8
T : 32,6 NS T : 55 NS T : 8 NS
Létrozole L : 30 L : 49 L : 9,4
T : 20 p = 0,001 T : 38 p = 0,0001 T : 5,9 p = 0,0001

Anastrozole
Les résultats des deux essais jumeaux, nord-américain et
européen, comparant l’anastrozole 1 mg/j au tamoxifène en
première ligne de traitement hormonal en situation métasta-
tique et/ou localement avancée, ont été publiés récemment (12,
13). Les données principales sont présentés dans les
tableaux III et IV. Les premiers objectifs étaient le TTP et la
RO, avec une visée d’équivalence. Les caractéristiques des
patientes diffèrent entre les deux essais, les patientes nord-
américaines présentant plus fréquemment une expression des
récepteurs hormonaux que les patientes européennes (89 %
versus 45 %), mais aussi, plus souvent, des métastases viscé-
rales (47 % versus 30-37 %). C’est dans l’essai nord-américain
qu’est observée une tendance à la supériorité de l’anastrozole,
en termes de TTP et de bénéfices cliniques (réponse objective
+ stabilisation ⭓24 semaines).
Exemestane
Les résultats les plus récents, présentés et non encore publiés,
proviennent d’une étude de phase II randomisée, comparant
exemestane 25 mg/j à tamoxifène 20 mg/j en première ligne
métastatique (14) (tableau V). La population de patientes
incluses ne diffère pas des autres études (RE+ et/ou RP+ :
90 % ; métastases viscérales : 57,5 %). Les taux de réponses
observés étaient de 44,6 % dans le bras exemestane et 14,3 %
dans le bras tamoxifène. Le bénéfice clinique était respective-
ment de 55,3 % et 39,3 %. Les principaux effets secondaires
des patientes sous exemestane ne diffèrent pas non plus de
ceux observés avec les inhibiteurs non stéroïdiens (asthénie
11,7 % ; nausées 3,3 % ; bouffées de chaleur 3,3 %). Cette
étude de phase II a été transformée en étude de phase III ran-
domisée, dont les résultats sont attendus.
PPEERRSSPPEECCTTIIVVEESS
Les inhibiteurs de l’aromatase se sont clairement positionnés
en deuxième ligne thérapeutique, étant au minimum aussi effi-
caces que l’acétate de mégestrol, et globalement mieux tolérés.
Les résultats précoces de la comparaison directe au tamoxifène
en première intention thérapeutique dans des situations de can-
cer du sein localement avancé et/ou métastatique laissent pré-
sager, là aussi au minimum, une efficacité similaire, voire
supérieure. Il faut toutefois noter que le différentiel espéré en
termes d’effets secondaires n’est pas au rendez-vous. Ces
résultats ont conduit à la mise en place de larges essais adju-
vants, parfois testant une combinaison tamoxifène-inhibiteur
alors que nous ne disposons pas de données d’association à la
phase avancée. L’essai ATAC (anastrozole versus tamoxifène,
versus la combinaison des deux) est clos. Le groupe BIG mène
les essais comparant létrozole et tamoxifène. L’exemestane est
testé par les groupes PEGASE et ICCG. Sans préjuger des
résultats de ces différentes études, les inhibiteurs de l’aroma-
tase de troisième génération figurent déjà parmi les outils thé-
rapeutiques supplémentaires majeurs à la disposition des clini-
ciens.
Sur le plan fondamental, un gros effort est fait pour caractéri-
ser l’aromatase (régulation transcriptionnelle, expression diffé-
rentielle, iso-enzymes, etc.). Nul doute que les années qui
viennent verront se préciser, à l’instar des récepteurs aux hor-
mones stéroïdes pour le tamoxifène, les facteurs biologiques
prédictifs d’efficacité des inhibiteurs de l’aromatase. ■
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Clemons M, Goss P. Estrogen and the risk of breast cancer. N Engl J Med
2001 ; 344 : 276-85.
2. De Cremoux P. Les inhibiteurs de l’aromatase : aspects pharmacologiques.
Bull Cancer 2000 : numéro spécial, décembre 2000 : 23-9.
3. Miller W, Dixon J. Antiaromatase agents : preclinical data and neoadjuvant
therapy. Clin Breast Cancer 2000 ; (suppl. 1) : S9-S14.
59
La Lettre du Cancérologue - volume X - n° 2 - mars/avril 2001
Létrozole Tamoxifène Anastrozole Tamoxifène Anastrozole Tamoxifène
États-Unis Europe
Bouffées de chaleur 16 13 36,5 24,2 19,6 18,8
Nausées 6 6 30,6 34,1 12,5 13,4
Maladie thrombo-embolique 1 2 4,1 8 ,2 4,8 7,3
Thrombose veineuse profonde NR 1,2 2,2 0,6 3
Asthénie 11 11 31,8 35,7 8,6 4,9
Tableau IV. Effets secondaires du létrozole et de l’anastrozole comparés au tamoxifène.
NR : non rapporté.
Exemestane Tamoxifène
n 61 59
RE + RP + 44 49
RE + ou RP + 48 39
Viscères 54 59
Tamoxifène adjuvant 18 19
RO 44,6 14,3
BC 55,3 39,3
Asthénie 11,7 13,3
Bouffées de chaleur 3,3 13,3
Nausées 3,3 8,3
Prise de poids 5 6,7
Tableau V. Principaux résultats de l’étude de phase II randomisée
comparant exemestane à tamoxifène en première ligne métastatique.
Les résultats sont indiqués en pourcentages (sauf n).

MISE AU POINT
4. Sasano H, Suzuki T, Moriya T. Immunohistochemistry of aromatase : a
recent next development. In: Miller W, Santen R, eds. Aromatase inhibition and
breast cancer. New York : Marcel Dekker, 2001 : 191-8.
5. Eppenberger U, Levano S, Schoumacher F, Müller H, Eppenberger-Castori
S, Evans D. Molecular epidemiology of aromatase expression in 1 182 primary
breast cancer. In : Miller W, Santen R, eds. Aromatase inhibition and breast
cancer. New York : Marcel Dekker, 2001 : 199-212.
6. Kerbrat P, Lefeuvre C. Antiaromatase : revue des résultats cliniques. Bull
Cancer 2000 ; numéro spécial, décembre 2000.
7. Buzdar AU, Jonat W, Howell A et al. Anastrozole versus megestrol ace-
tate in the treatment of postmenopausal women with advanced breast carci-
noma : results of a survival update based on a combined analysis of data
from two mature phase III trials. Arimidex®Study Group. Cancer 1998 ; 83 :
1142-52.
8. Dombernowsky P, Smith I, Falkson G et al. Letrozole, a new oral aromatase
inhibitor for advanced breast cancer : double-blind randomized trial showing a
dose effect and improved efficacy and tolerability compared with megestrol ace-
tate. J Clin Oncol 1998 ; 16 : 453-61.
9. Kaufmann M, Bajetta E, Dirix LY et al. Exemestane is superior to megestrol
acetate after tamoxifen failure in postmenopausal women with advanced breast
cancer : results of a phase III randomized double-blind trial. The Exemestane
Study Group. J Clin Oncol 2000 ; 18 : 1399-411.
10. Lonning PE, Bajetta E, Murray R et al. Activity of exemestane in metastatic
breast cancer after failure of nonsteroidal aromatase inhibitors : a phase II
trial. J Clin Oncol 2000 ; 18 : 2234-44.
11. Mouridsen H, Gershanovich M, Monnier A et al. Letrozole is superior to
tamoxifen as first-line hormonal treatment of postmenopausal women with
locally advanced or metastatic breast cancer. Ann Oncol 2000 ; 11 : 155
(abstr. 709).
12. Bonneterre J, Thurlimann B, Robertson JF et al. Anastrozole versus
tamoxifen as first-line therapy for advanced breast cancer in 668 postmenopau-
sal women : results of the Tamoxifen or Arimidex®Randomized Group Efficacy
and Tolerability Study. J Clin Oncol 2000 ; 18 : 3748-57.
13. Nabholtz JM, Buzdar A, Pollak M et al. Anastrozole is superior to tamoxi-
fen as first-line therapy for advanced breast cancer in postmenopausal women :
results of a north-american multicenter randomized trial. Arimidex®Study
Group. J Clin Oncol 2000 ; 18 : 3758-67.
14. Paridaens R, pour EORTC-BG-IDBBC. Exemestane as Initial Therapy for
MBC : randomized EORTC phase II/III trial, 23rd San Antonio Breast Cancer
Symposium, San Antonio, 2000.
1
/
5
100%