Réponse tumorale et biothérapie : quelles nouveautés ? Actualités

160 | La Lettre du Cancérologue • Vol. XXIII - n° 5 - mai 2014
Actualités
à la 25e JFCD
Réponse tumorale
et biothérapie :
quelles nouveautés ?
Tumoral response and biotherapy: what’s new?
C. Dromain*
* Service de radiologie diagnostique,
hôpital Gustave-Roussy-Grand Paris,
Villejuif.
Limites des critères
RECIST pour l’évaluation
des biothérapies
Les critères RECIST, utilisés pour évaluer la réponse
tumorale, présentent plusieurs limitations (1). La
première est l’absence d’objectivité lorsqu’il n’y a
aucune lésion cible mesurable, ce qui est particu-
lièrement le cas des lésions osseuses isolées, des
carcinoses péritonéales ou des miliaires pulmonaires.
La deuxième limitation majeure dans l’évaluation de
l’effet du traitement sur la cinétique de la croissance
tumorale est l’absence d’évaluation de la croissance
tumorale avant le début du traitement. Enfi n, dans
les traitements à effet cytostatique non cytotoxiques,
la réponse au traitement ne s’accompagne pas
toujours d’une diminution de la taille des tumeurs.
Nouveaux critères adaptés
de l’évaluation RECIST
Profondeur de la réponse
et du taux de réponse précoce
Les critères RECIST permettent de classer la maladie
selon 4 catégories de réponse (réponse complète,
stabilisation de la maladie, réponse partielle et
progression) en fonction d’un seuil de diminution
ou de progression défi ni de façon arbitraire (−30 %
par rapport à l’inclusion pour défi nir une réponse
partielle, −20 % par rapport à la meilleure réponse
ou au nadir pour défi nir la progression). Des études
récentes ont montré que le taux de réponse calculé
selon les principes RECIST et utilisé comme une
variable continue pourrait constituer un para-
mètre de réponse mieux corrélé à la survie globale
que l’utilisation des catégories RECIST. Dans une
étude reprenant les données des études randomi-
sées CRYSTAL et OPUS, qui évaluaient l’apport du
cétuximab en association avec le FOLFIRI (irinotécan,
acide folique, 5-FU) dans le cancer colorectal méta-
statique, la valeur du taux de réponse 8 semaines
après le début du traitement (réponse précoce)
permettait une meilleure prédiction de la survie
globale chez les patients traités par cétuximab en
première ligne thérapeutique (2). Plus le taux de
réponse était élevé, plus la survie était prolongée.
Par ailleurs, ce taux de réponse permettait de mettre
en évidence un effet de réponse plus important dans
le groupe des patients traités par une association
cétuximab + chimiothérapie que chez les patients
traités par chimiothérapie seule. Un seuil de réponse
précoce de 20 % a été proposé pour distinguer les
bons répondeurs précoces des mauvais.
◆Taux de croissance tumorale
Le taux de croissance tumorale correspond au taux
d’augmentation du volume tumoral sur une durée de
1 mois. La croissance tumorale est habituellement
évaluée à partir des mesures du plus grand diamètre
des lésions cibles défi ni selon les critères RECIST
transformé en volume.
3 log
(
Dt
)
Croissance tumorale = D0 ,
t
où D correspond à la somme des plus longs
diamètres. Ce chiffre est ensuite converti en un taux
de croissance sur 1 mois.
Taux de croissance tumorale = 100TC–1
La comparaison des taux de croissance tumorale
avant et après l’instauration du traitement permet
une meilleure évaluation des effets induits par le trai-
tement indépendamment de la croissance naturelle
de la tumeur que la classifi cation les critères RECIST.
En effet, une tumeur à croissance rapide au moment
de l’inclusion a plus de chance d’être classée stable
ou progressive selon les critères RECIST, quelle que
soit l’activité antitumorale de la molécule testée.

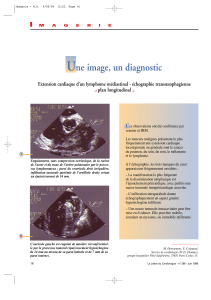
Figure 1. Patiente suivie pour un cancer du rein droit à cellules claires traitée par sunitinib. Le scanner de surveillance (b)
semble montrer l’apparition d’une lésion hépatique très hypodense, mais il s’agit en fait de la nécrose d’une lésion
qui était déjà présente, à la limite de la visibilité (a).
ba
La Lettre du Cancérologue • Vol. XXIII - n° 5 - mai 2014 | 161
Résumé
Les critères radiologiques communément utilisés pour évaluer la réponse tumorale au traitement en
cancérologie sont les critères morphologiques RECIST1.1, basés sur des mesures de la taille des tumeurs
(1)
.
L’utilisation de ces critères est cependant souvent limitée dans l’évaluation précoce des thérapies ciblées,
notamment celles visant l’angiogenèse tumorale, car ils ne permettent pas une analyse du contenu intra-
lésionnel des tumeurs. L’objectif de cet article est de décrire les critères d’évaluation récemment développés
pour l’évaluation des biothérapies.
Mots-clés
Imagerie
Scanner
Métastases
hépatiques
Évaluation
Biothérapie
Summary
Imaging criteria commonly
used to assess tumor response
to treatment in oncology are
morphological RECIST1.1
criteria based on tumor size
measurements (1). These
criteria are however often
limited in the early evalua-
tion of antiangiogenic drugs
because they do not allow an
intratumoral content analysis.
The objective of this paper is
to describe the new criteria
that have been recently deve-
loped for the assessment of
bio therapeutic drugs.
Keywords
Imaging
Scan
Hepatic metastasis
Evaluation
Biotherapy
À l’inverse, une tumeur d’évolution très lente aura
une forte probabilité d’être classée stable même en
l’absence d’effi cacité thérapeutique.
Une étude récente a comparé les taux de croissance
tumorale avant le traitement et au moment de la
première évaluation chez 201 patients traités en
phase I (3). Le taux avait diminué chez 82 % des
patients RECIST stables et chez 65 % des patients
RECIST progressant. Le taux de croissance tumorale
était la seule variable indépendante corrélée à la
survie sans progression. Une autre étude, réalisée
dans le cancer rénal métastatique, a également
montré que, contrairement à la réponse RECIST,
le taux de croissance tumorale était corrélé à la
survie sans progression et à la survie globale (4). Par
ailleurs, l’évaluation du taux de croissance tumorale
permettait de révéler différents profi ls de progression
entre les groupes traités par sorafénib ou évérolimus.
Dans le groupe des patients traités par sorafénib,
contrairement à ceux traités par évérolimus, le taux
de croissance tumorale durant le dernier cycle avant
la progression restait inférieur au taux mesuré avant
le début du traitement et à celui retrouvé après
l’arrêt du traitement pour progression.
Nouveaux critères pour l’évaluation
des agents antiangiogéniques
Les nouvelles biothérapies peuvent induire des modi-
fi cations de la perfusion tumorale, ce qui entraîne des
modifi cations de la densité des tumeurs au scanner
sans qu’il n’y ait une diminution de la taille. Il en
résulte, le plus souvent, une stabilisation selon les
critères RECIST alors même que le patient répond
au traitement. De plus, cette diminution de taille,
lorsqu’elle survient, peut avoir lieu très tard après le
début du traitement. L’apparition de cette nécrose
intratumorale peut être à l’origine d’images pièges,
telles qu’une augmentation paradoxale de la taille
des tumeurs ou la fausse apparition de nouvelles
lésions difficilement détectables sur l’examen
d’inclusion et qui deviennent très clairement visibles
sur l’examen de suivi en raison de leur forte hypo-
densité (fi gure 1).
Plusieurs études cliniques évaluant les traitements
antiangiogéniques ont montré une mauvaise
corrélation entre le taux de réponse (réponses
complètes et réponses partielles) selon les critères
RECIST et la survie sans progression : les réponses
partielles sont rares, alors que les taux de stabili-
sation sont en progression. De nouveaux critères,
basés sur l’analyse du contenu intralésionnel, ont
été développés.
H. Choi et al. (5) ont proposé de mesurer la densité
des lésions dans les métastases hépatiques de
tumeurs stromales gastro-intestinales (GIST) traitées
par imatinib et ont défi ni de nouveaux critères de
réponse : une diminution du diamètre tumoral
supérieure à 10 % ou une diminution de la densité
supérieure à 15 %. L’utilisation de ces critères dans
les métastases de cancers du rein traités par sunitinib

Figure 2. Métastases hépatiques d’un cancer du côlon avant traitement (a) et après 4 cycles de FOLFOX + bévaci-
zumab (b). Les images de scanner réalisées à la phase veineuse portale ne montrent pas de régression de la taille des
lésions hépatiques mais une diminution de la densité, une disparition de la prise de contraste périphérique et une
interface foie/lésion à limite nette correspondant à une réponse vasculaire.
ba
162 | La Lettre du Cancérologue • Vol. XXIII - n° 5 - mai 2014
Réponse tumorale etbiothérapie : quellesnouveautés ?
Actualités
à la 25e JFCD
a montré une meilleure corrélation à la survie sans
progression et à la survie globale que les critères
RECIST, avec un taux de réponse partielle évalué
à 7 (critères RECIST) versus 36 (critères de Choi)
patients sur 55 (6).
Y.S. Chun et al. (7) ont proposé, pour les métastases
d’un cancer du côlon traitées par bévacizumab, une
classifi cation en 3 catégories basée sur la densité,
l’interface foie/lésion et la présence ou l’absence d’un
rehaussement périphérique ; les lésions devenues
hypodenses et homogènes dont les contours sont
très bien limités sans rehaussement périphérique
peuvent être considérées en “réponse optimale”
(fi gure 2).
Une version modifiée des critères RECIST a été
proposée dans les carcinomes hépatocellulaires.
La mesure de la tumeur y est remplacée par celle de
la tumeur viable, défi nie par la tumeur présentant
une prise de contraste artérielle (8).
Nouveaux critères
pour l’évaluation des molécules
immunothérapeutiques
De nouveaux critères de réponse IrRC (Immuno-
related Response Criteria) ont également été
proposés afi n de prendre en compte les différences,
dans la cinétique de la réponse tumorale, entre les
agents cytotoxiques et les molécules immuno-
thérapeutiques (9). Ces critères ont initialement
été développés au cours d’essais cliniques chez des
patients atteints de mélanomes avancés traités
par ipilimumab (anticorps monoclonal humain
bloquant les lymphocytes T cytotoxiques associés
à l’antigène 4).
En effet, lors de ce type de traitement, la réponse
pourrait être atteinte après une augmentation
initiale et paradoxale du volume tumoral corres-
pondant au recrutement des cellules T activées qui
viennent infi ltrer la tumeur.
Ces critères sont basés sur ceux de l’OMS compre-
nant la mesure bidimensionnelle de lésions cibles
(10 lésions viscérales + 5 lésions cutanées), avec
2 différences majeures :
➤
l’apparition d’une nouvelle lésion sur un examen
de suivi n’implique pas forcément la progression ;
la surface de cette nouvelle lésion doit être addi-
tionnée à la somme des surfaces des lésions cibles
précédemment décrites ;
➤
afi n d’éviter de classer à tort un patient en progres-
sion, il est nécessaire, en l’absence de détérioration
clinique ou biologique, de confi rmer la progression
après 4 semaines au minimum.
Place de l’imagerie fonctionnelle
Une des perspectives est l’utilisation de l’imagerie fonc-
tionnelle comme facteur pronostique, facteur prédictif
de la réponse ou marqueur précoce de réponse.
La première approche utilisée est l’imagerie de
perfusion, qui peut être réalisée en échographie,
en tomodensitométrie (TDM) et en IRM. Le prin-
cipe repose sur l’injection intraveineuse en bolus
d’un produit de contraste et la mesure des modi-
fi cations du rehaussement des tissus au cours du
temps permettant la quantifi cation de paramètres
de perfusion (aire sous la courbe de rehaussement en
échographie, volume et fl ux sanguins à la TDM, aire
sous la courbe de la concentration de gadolinium,

La Lettre du Cancérologue • Vol. XXIII - n° 5 - mai 2014 | 163
Actualités
à la 25e JFCD
Ktrans et Kep en IRM). Actuellement, il n’y a que peu de
standardisation des protocoles d’acquisition et des
logiciels de traitement d’images, ce qui rend diffi cile
la généralisation des résultats et limite l’utilité de
ce type d’imagerie en routine clinique.
L’utilisation de la DCE-US (Dynamic Contrast-
Enhanced UltraSonography) vient d’être intégrée
dans les recommandations européennes pour le
monitoring des traitements antiangiogéniques, avec
un niveau de preuve A 1b selon les recommandations
d’Oxford utilisées par le groupe d’experts (10). La
technique a également été proposée dans les recom-
mandations de l’ESMO pour les GIST (11). En scanner
de perfusion, une récente étude clinique réalisée chez
51 patients ayant un cancer du rein métastatique
traités par antiangiogéniques (sorafénib ou sunitinib)
a montré que les paramètres de perfusion avant
traitement (fl ux et volumes sanguins) avaient des
valeurs plus élevées chez les patients répondeurs
que chez les non- répondeurs, ce qui suggère qu’une
tumeur initialement richement vascularisée est plus
sensible au traitement (12). Ces paramètres initiaux,
qui pourraient être prédictifs de la réponse théra-
peutique, n’étaient cependant pas signifi cativement
corrélés à la survie.
Pendant le traitement antiangiogénique, le scanner
de perfusion montrait par ailleurs, au premier cycle
du traitement, une diminution signifi cative des fl ux
et des volumes sanguins.
L’autre approche fonctionnelle actuellement en
cours d’évaluation est l’IRM de diffusion. C’est un
marqueur indirect de la densité cellulaire quanti-
fi able par la mesure de l’ADC (Apparent Diffusion
Coeffi cient). Une étude réalisée dans l’évaluation de
métastases d’origine colorectale a montré que, avant
le traitement, un ADC bas (forte densité cellulaire)
était un facteur prédictif de bonne réponse (13). Ce
biomarqueur pourrait également être utilisé comme
facteur substitutif de réponse en cours de traite-
ment : ainsi, on observe, dès les premiers jours de
traitement, une augmentation de l’ADC moyen en
cas de bonne réponse (14).
Conclusion
La connaissance et l’utilisation des critères RECIST
restent fondamentales pour l’évaluation des trai-
tements en oncologie permettant une analyse
objective, reproductible et internationale facilitant
la comparaison des études cliniques. Cependant,
l’arrivée des nouvelles biothérapies doit inciter à
l’adaptation de ces critères ou à l’ajout de nouveaux
critères d’évaluation, basés notamment sur l’ana-
lyse du contenu intralésionnel. L’imagerie fonc-
tionnelle est prometteuse dans la détermination
de nouveaux facteurs pronostiques et prédictifs de
la réponse. ■
1. Therasse P, Arbuck SG, Eisenhauer EA et al.; European
Organization for Research and Treatment of Cancer,
National Cancer Institute of the United States, National
Cancer Institute of Canada. New guidelines to evaluate
the response to treatment in solid tumors. J Natl Cancer
Inst 2000;92(3):205-16.
2. Piessevaux H, Buyse M, Schlichting M et al. Use of early
tumor shrinkage to predict long-term outcome in meta-
static colorectal cancer treated with cetuximab. J Clin Oncol
2013;31(30):3764-75.
3. Ferté C, Fernandez M, Hollebecque A et al. Tumor growth
rate is an early indicator of antitumor drug activity in phase I
clinical trials. Clin Cancer Res 2014;20(1):246-52.
4. Ferté C, Koscielny S, Albiges L et al. Tumor growth rate
provides useful information to evaluate sorafenib and evero-
limus treatment in metastatic renal cell carcinoma patients:
an integrated analysis of the TARGET and RECORD phase 3
trial data. Eur Urol 2014;65(4):713-20.
5. Choi H, Charnsangavej C, Faria SC et al. Correlation of
computed tomography and positron emission tomography
in patients with metastatic gastrointestinal stromal tumor
treated at a single institution with imatinib mesylate:
proposal of new computed tomography response criteria.
J Clin Oncol 2007;25(13):1753-9.
6. Van der Veldt AA, Meijerink MR, Van den Eertwegh AJ,
Haanen JB, Boven E. CHOI response criteria for early
prediction of clinical outcome in patients with meta-
static renal cell cancer treated with sunitinib. Br J Cancer
2010;102(5):803-9.
7. Chun YS, Vauthey JN, Boonsirikamchai P et al. Asso-
ciation of computed tomography morphologic criteria
with pathologic response and survival in patients treated
with bevacizumab for colorectal liver metastases. JAMA
2009;302(21):2338-44.
8. Llovet JM, Di Bisceglie AM, Bruix J et al.; Panel of Experts
in HCC-Design Clinical Trials. Design and endpoints of
clinical trials in hepatocellular carcinoma. J Natl Cancer
Inst 2008;100(10):698-711.
9. Wolchok JD, Hoos A, O’Day S et al. Guidelines for the
evaluation of immune therapy activity in solid tumors:
immune-related response criteria. Clin Cancer Res
2009;15(23):7412-20.
10. Piscaglia F, Nolsøe C, Dietrich CF et al. The EFSUMB
Guidelines and Recommendations on the Clinical Practice of
Contrast Enhanced Ultrasound (CEUS): update 2011 on non-
hepatic applications. Ultraschall Med 2012;33(1):33-59.
11. Casali PG, Blay JY; ESMO/CONTICANET/EUROBONET
Consensus Panel of Experts. Gastrointestinal stromal
tumours: ESMO Clinical Practice Guidelines for diagnosis,
treatment and follow-up. Ann Oncol 2010;21(Suppl. 5):
v98-102.
12. Fournier LS, Oudard S, Thiam R et al. Metastatic
renal carcinoma: evaluation of antiangiogenic therapy
with dynamic contrast-enhanced CT. Radiology 2010;
256(2):511-8.
13. Cui Y, Zhang XP, Sun YS, Tang L, Shen L. Apparent diffu-
sion coeffi cient: potential imaging biomarker for prediction
and early detection of response to chemotherapy in hepatic
metastases. Radiology 2008;248(3):894-900.
14. Koh DM, Scurr E, Collins D et al. Predicting response
of colorectal hepatic metastasis: value of pretreatment
apparent diffusion coefficients. AJR Am J Roentgenol
2007;188(4):1001-8.
Références bibliographiques
C.Dromain déclare
ne pas avoir deliensd’intérêts.
1
/
4
100%